Beregning af pH-virkningen af fortynding:En praktisk vejledning
Af Claire Gillespie
Opdateret 30. august 2022
Fortynding er en rutinemæssig laboratorieteknik, som videnskabsstuderende bruger til at opnå præcise koncentrationer. Det sker også i hverdagen - at tilføje vand til kaffe eller vin efter smag. Det er vigtigt, at fortynding ændrer pH-værdien af en opløsning, hvilket enten gør den mindre sur eller mindre basisk, afhængigt af udgangsmaterialet.
TL;DR
Når du fortynder en sur opløsning, bevæger dens pH sig mod 7 (mere neutral). Fortynding af en basisk opløsning skubber dens pH mod 7 fra den alkaliske side. Beregn effekten ved at konvertere den oprindelige pH-værdi til hydrogen-ion-koncentration, justere denne koncentration for det nye volumen og konvertere tilbage til pH.
Hvad er fortynding?
Tilsætning af opløsningsmiddel - sædvanligvis vand - til en opløsning øger andelen af opløsningsmidlet i forhold til det opløste stof. Mængden af opløst stof forbliver den samme, men volumenet vokser, så hver molær koncentration falder med forholdet mellem det nye volumen og det oprindelige volumen.
Forstå pH
pH-skalaen, der går fra 0 til 14, kvantificerer surhedsgrad eller alkalinitet. En pH på 7 er neutral. Under 7 er opløsningen sur; over 7 er det grundlæggende. Skalaen er logaritmisk:hver heltalændring repræsenterer en ti gange forskel i hydrogen-ion-koncentration. For eksempel er pH 3 ti gange surere end pH 4 og hundrede gange surere end pH 5.
pH er defineret som pH =–log[H⁺] , hvor [H+] er molariteten af hydrogenioner. Omarrangering giver [H⁺] =10 –pH .
Fortynding af en syre
Syrer (f.eks. citronsaft, batterisyre, kaffe) indeholder H⁺-ioner. Tilsætning af vand reducerer [H⁺], hvilket hæver pH-værdien mod 7. Fordi det tilsatte vand er neutralt, kan pH-værdien af en sur opløsning aldrig stige over 7.
Fortynding af en base
Baser (f.eks. ammoniak, blegemiddel, bagepulver) indeholder OH⁻-ioner. Vand fortynder OH⁻, hvilket sænker pH-værdien mod 7. En basisk opløsnings pH-værdi kan aldrig falde til under 7, når den fortyndes med neutralt vand.
Trin-for-trin-beregning
1. Konverter den oprindelige pH-værdi til hydrogen-ion-koncentration. For en pH6-opløsning er [H⁺] =10 –6 M.
2. Bestem fortyndingsfaktoren. Hvis det endelige volumen er fire gange det oprindelige, divideres koncentrationen med fire.
3. Beregn den nye [H⁺]. Ved at bruge eksemplet ovenfor:[H⁺]new =(10 –6 M) ÷ 4 =2,5 × 10 –7 M.
4. Konverter tilbage til pH. pHnew =–log(2,5 × 10 –7 ) ≈ 6,60.
En firedobbelt fortynding af en pH6-syre hæver således pH-værdien til ca. 6,6 og flytter den tættere på neutralitet.
Praktiske tips
- Brug altid et kalibreret pH-meter til præcise målinger.
- For stærke syrer eller baser, overvej ionstyrkens effekt på pH.
- Husk, at fortynding ikke kan krydse neutralpunktet (pH 7), når du bruger rent vand.
 Varme artikler
Varme artikler
-
 Øjne blinker på en chipDen nye hornhinde-på-en-chip-enhed kan gengive trykket fra bevægelige tårer inde i et blinkende øjenlåg, og kan mere præcist teste virkningerne af lægemidler på det menneskelige øje. Kredit:Mindy Taka
Øjne blinker på en chipDen nye hornhinde-på-en-chip-enhed kan gengive trykket fra bevægelige tårer inde i et blinkende øjenlåg, og kan mere præcist teste virkningerne af lægemidler på det menneskelige øje. Kredit:Mindy Taka -
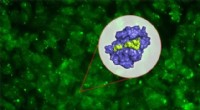 Biologers nye peptid kan bekæmpe mange kræftformerMIT-biologer har designet et nyt peptid, der kan forstyrre et nøgleprotein, som mange typer kræftformer, herunder nogle former for lymfom, leukæmi, og brystkræft, brug for at overleve. Kredit:Chelsea
Biologers nye peptid kan bekæmpe mange kræftformerMIT-biologer har designet et nyt peptid, der kan forstyrre et nøgleprotein, som mange typer kræftformer, herunder nogle former for lymfom, leukæmi, og brystkræft, brug for at overleve. Kredit:Chelsea -
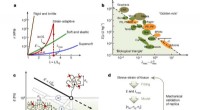 Kode til finjustering af elastomerer for at efterligne biologiske materialerProgrammering af mekanisk ydeevne. en, Den mekaniske mangfoldighed af biologiske og syntetiske materialer er illustreret ved enaksede trækspænding-deformationskurver, som afslører kombinationer af ege
Kode til finjustering af elastomerer for at efterligne biologiske materialerProgrammering af mekanisk ydeevne. en, Den mekaniske mangfoldighed af biologiske og syntetiske materialer er illustreret ved enaksede trækspænding-deformationskurver, som afslører kombinationer af ege -
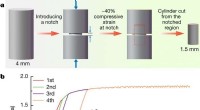 Foryngende metallisk glas for at forhindre brudForyngelse og deformation af en MG. Kredit: Natur (2020). DOI:10.1038/s41586-020-2016-3 Et team af forskere fra det kinesiske videnskabsakademi og University of Cambridge har fundet en måde at fo
Foryngende metallisk glas for at forhindre brudForyngelse og deformation af en MG. Kredit: Natur (2020). DOI:10.1038/s41586-020-2016-3 Et team af forskere fra det kinesiske videnskabsakademi og University of Cambridge har fundet en måde at fo
- Comet U1 NEOWISE—en mulig kikkertkomet?
- Hvordan kan hastigheden af et bevægende objekt ændre sig?
- Hvad kaldes det, når målet på afstand, hvorpå et objekt eller lys kan ses tydeligt?
- NASA finder, at den tropiske storm Jeruto udvikler sig i det sydlige Indiske Ocean
- Plasmoniske pixels kan bruges til at lave ikke-falmende maling
- Hvilken pladetektonisk er Santorini -vulkanen?


