Beregning af mol af enhver kemisk forbindelse:En praktisk vejledning
Af Michael Judge | Opdateret 30. august 2022
I kemi er en muldvarp den enhed, der forbinder massen af et stof til antallet af molekyler eller atomer, det indeholder. Én mol er lig med 6,022×10²³ enheder – Avogadros tal – hvilket gør det til et vigtigt værktøj til kvantitativ analyse.
Trin 1 – Identificer den molekylære formel
Start med den nøjagtige molekylformel for forbindelsen. Formlen fortæller dig, hvor mange atomer af hvert grundstof er til stede i et molekyle. For eksempel er vand H₂O, hvilket betyder, at hvert molekyle indeholder to hydrogenatomer og et oxygenatom.
Trin 2 – Hent atomvægte
Se et periodisk system for at finde atomvægten (også kaldet atommasse) af hvert grundstof i formlen. Typiske værdier er 1,008 g/mol for brint og 16,00 g/mol for oxygen.
Trin 3 – Beregn molmassen
Multiplicer hvert elements atomvægt med antallet af atomer i det element, og summer derefter resultaterne:
(2×1,008)+(1×16,00)=18,016g/mol
Denne total, udtrykt i gram pr. mol, er den molære masse af forbindelsen.
Trin 4 – Konverter masse til mol
Divider prøvens masse (i gram) med molmassen for at få antallet af mol:
25gH₂O÷18,016g/mol≈1,39mol
Værktøjer, du skal bruge
- Periodisk tabel (print eller digital)
- Videnskabelig lommeregner
Følg disse trin for at beregne mol for ethvert kemikalie, uanset om du arbejder i et laboratorium eller studerer kemikurser.
At mestre muldvarpeberegninger låser op for muligheden for at udføre nøjagtige støkiometriske beregninger, designe eksperimenter og fortolke analytiske data.
 Varme artikler
Varme artikler
-
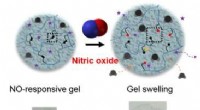 Forskere udvikler potentielt terapeutisk gel, som detekterer nitrogenoxid, absorberer overskydende v…IBS-forskere udviklede en hydrogel lavet af polymert akrylamid (blå spaghetti) forbundet med tværbindere (sort), som kan rumme lægemiddelmolekyler (lilla stjerner) inden for dets net (grå). I nærværel
Forskere udvikler potentielt terapeutisk gel, som detekterer nitrogenoxid, absorberer overskydende v…IBS-forskere udviklede en hydrogel lavet af polymert akrylamid (blå spaghetti) forbundet med tværbindere (sort), som kan rumme lægemiddelmolekyler (lilla stjerner) inden for dets net (grå). I nærværel -
 Spilde bønnerne på kaffens sande identitetKredit:Pixabay/CC0 Public Domain Folk verden over ønsker, at deres kaffe både er tilfredsstillende og til en rimelig pris. For at opfylde disse standarder, ristemaskiner bruger typisk en blanding
Spilde bønnerne på kaffens sande identitetKredit:Pixabay/CC0 Public Domain Folk verden over ønsker, at deres kaffe både er tilfredsstillende og til en rimelig pris. For at opfylde disse standarder, ristemaskiner bruger typisk en blanding -
 Elektrokemi åbner ny adgang til vigtige klasser af stofferEn ung forsker i professor Waldvogels team, der bruger et screeningsapparat til parallel elektrolyseoptimering. Kredit:Alexander Sell Elektrokemi har gennemgået en renæssance i de seneste år, og m
Elektrokemi åbner ny adgang til vigtige klasser af stofferEn ung forsker i professor Waldvogels team, der bruger et screeningsapparat til parallel elektrolyseoptimering. Kredit:Alexander Sell Elektrokemi har gennemgået en renæssance i de seneste år, og m -
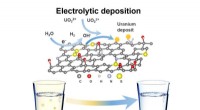 Brug af grafenskum til at filtrere toksiner fra drikkevandEt genanvendeligt 3D-funktionaliseret reduceret grafenoxidskum (3D-FrGOF) bruges som en in situ elektrolytisk aflejringselektrode til at udvinde uran fra forurenet vand. Kredit:MIT Nogle former fo
Brug af grafenskum til at filtrere toksiner fra drikkevandEt genanvendeligt 3D-funktionaliseret reduceret grafenoxidskum (3D-FrGOF) bruges som en in situ elektrolytisk aflejringselektrode til at udvinde uran fra forurenet vand. Kredit:MIT Nogle former fo
- Forskere udvikler en ny model til at forudsige overfladeatomspredning
- Filippinsk bosættelse nedsænket af dæmning dukker op igen på grund af tørke
- Hvordan mænd kan være allierede for kvinder lige nu
- Hvordan dannede Wre -organer?
- Største britiske undersøgelse nogensinde om kropsformer og størrelser
- La Niña vil give os en våd sommer. Det er godt vejr for myg


