Trin-for-trin guide til at bestemme en molekylær formel
Molekylformlen viser det nøjagtige antal af hvert atom i et molekyle af en forbindelse, hvorimod den empiriske formel giver det enkleste heltalsforhold mellem atomer. For mange forbindelser er de to formler forskellige. At forstå den molekylære formel er afgørende for nøjagtig støkiometri, materialesyntese og kemisk analyse.
Hurtig oversigt
1. Bestem den empiriske formel. 2. Beregn dens empiriske masse ved hjælp af et periodisk system. 3. Divider den kendte molekylmasse med den empiriske masse for at finde n. 4. Gang hvert sænket skrift i den empiriske formel med n for at få den molekylære formel.
1. Identificer den empiriske formel
Få eller beregn den empiriske formel ved at analysere grundstofsammensætningen (f.eks. via massespektrometri eller forbrændingsanalyse). Hvis du har den procentvise sammensætning, skal du konvertere til mol og reducere til det enkleste hele-talsforhold.
2. Beregn den empiriske masse
Sum atommasserne af alle atomer i den empiriske formel, idet der tages højde for subscripts. Dette giver massen af én empirisk enhed.
3. Find den empiriske enhedstal (n)
Brug n =molekylær masse ÷ empirisk masse . Det resulterende heltal (eller en simpel fraktion, der kan skaleres) angiver, hvor mange empiriske enheder der er i et molekyle.
4. Udled den molekylære formel
Gang hvert sænket skrift i den empiriske formel med n. Hvis et element mangler et underskrift, skal du behandle det som 1. Produktet er den molekylære formel, der afslører den sande atomare sammensætning af molekylet.
Ved at følge disse trin kan både kemikere og studerende pålideligt konvertere empiriske data til præcise molekylære formler, hvilket sikrer nøjagtige forudsigelser af reaktivitet, fysiske egenskaber og dosisberegninger.
 Varme artikler
Varme artikler
-
 ROSINA spektrale målinger vækker komets kemi til liveArbejdshestinstrument ROSINA-DFMS (Rosetta Orbiter Sensor til Ion- og Neutral Analysis-Double Focusing Mass Spectrometer). Kredit:University of Bern Lanceret marts 2004 og efter en 10-årig rejse o
ROSINA spektrale målinger vækker komets kemi til liveArbejdshestinstrument ROSINA-DFMS (Rosetta Orbiter Sensor til Ion- og Neutral Analysis-Double Focusing Mass Spectrometer). Kredit:University of Bern Lanceret marts 2004 og efter en 10-årig rejse o -
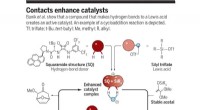 Brug af katalysatorer som en pincet til at vælge en enkelt enantiomer fra et spejlet parBanik et al. viser, at en forbindelse, der laver hydrogenbindinger til en Lewis-syre, danner en aktiv katalysator. Et eksempel på en cycloadditionsreaktion er afbildet. Tf, triflate; t-Bu, tert-butyl;
Brug af katalysatorer som en pincet til at vælge en enkelt enantiomer fra et spejlet parBanik et al. viser, at en forbindelse, der laver hydrogenbindinger til en Lewis-syre, danner en aktiv katalysator. Et eksempel på en cycloadditionsreaktion er afbildet. Tf, triflate; t-Bu, tert-butyl; -
 Video:Hollywood-blodbadenes kemiFalsk blod er en fast bestanddel af Halloween-gyserfilmoplevelsen, men der er ikke én opskrift, der passer til enhver filmskabers behov. Kemien for falsk blod er altid blevet justeret for at skabe den
Video:Hollywood-blodbadenes kemiFalsk blod er en fast bestanddel af Halloween-gyserfilmoplevelsen, men der er ikke én opskrift, der passer til enhver filmskabers behov. Kemien for falsk blod er altid blevet justeret for at skabe den -
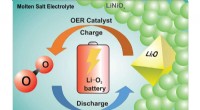 Kemikere får gennembrud på vejen til at skabe et genopladeligt lithium-oxygen-batteriEn fire-elektron redoxproces i en Li-oxygencelle elektrokatalyseres af en bifunktionel lithieret nikkeloxid-smeltet saltkompositkatode ved forhøjet temperatur til dannelse af Li2O. Det udvikler ilt ve
Kemikere får gennembrud på vejen til at skabe et genopladeligt lithium-oxygen-batteriEn fire-elektron redoxproces i en Li-oxygencelle elektrokatalyseres af en bifunktionel lithieret nikkeloxid-smeltet saltkompositkatode ved forhøjet temperatur til dannelse af Li2O. Det udvikler ilt ve
- Energigiganter brugte 1 mia. USD på klimalobbying, PR siden Paris:vagthund
- Analyserer de underliggende årsager til fødevarekrisen i Gaza
- Hvilket objekt er den bedste elektriske leder?
- Hvad er et vådområde? En økolog forklarer
- Hvad måles som et produkt af den anvendte kraft og afstanden flyttes?
- Hvordan ændres den elektriske kraft mellem to ladede partikler, hvis en ladning øges med en faktor…


