Hvordan ioniske og kovalente forbindelser opfører sig i vand:dissociation vs. opløselighed
Af Claire Gillespie | Opdateret 30. august 2022
TL;DR
Når et ionisk salt opløses, spaltes det til frie ioner og bliver til en elektrolyt, der leder elektricitet. De fleste kovalente molekyler forbliver uopløste i vand og danner i stedet et separat lag; kun polære kovalente stoffer som sukker opløses, men de ioniseres ikke.
Ioniske vs. kovalente forbindelser
Ioniske forbindelser består af positivt og negativt ladede ioner, der holdes sammen af elektrostatiske kræfter. Kovalente forbindelser er lavet af atomer, der deler elektroner, typisk danner diskrete molekyler. Ioniske faste stoffer udviser normalt høje smelte- og kogepunkter, fordi der kræves en stor mængde energi for at bryde det stærke ioniske gitter. Kovalente faste stoffer, der er samlinger af individuelle molekyler, har lavere smelte- og kogepunkter og kan adskilles lettere. Almindelige ioniske eksempler omfatter natriumbromid, calciumchlorid og magnesiumoxid, mens ethanol, ozon, brint og kuldioxid er klassiske kovalente stoffer.
Ioniske forbindelser i vand
Når en ionforbindelse kommer i kontakt med vand, tiltrækker de polære vandmolekyler kationerne og anionerne og trækker dem fra hinanden - en proces kendt som dissociation. De adskilte ioner bliver solvatiseret af skaller af vandmolekyler, som stabiliserer dem og forhindrer rekombination. Den resulterende opløsning indeholder fritgående ioner, hvilket gør den til en elektrolyt, der kan lede elektrisk strøm.
Kovalente forbindelser i vand
Kovalente molekyler ioniserer generelt ikke i vand, fordi de mangler ladede fragmenter. Vands polaritet betyder, at det interagerer stærkt med polære molekyler, men dårligt med ikke-polære. Følgelig forbliver de fleste kovalente stoffer uopløste og danner et separat lag på væskeoverfladen. Sukker, en polær kovalent forbindelse, er en undtagelse - det opløses i vand som intakte molekyler, men alligevel bryder det aldrig til ioner. Ikke-polære kovalente stoffer såsom olie modstår fuldstændig opløsning.
 Varme artikler
Varme artikler
-
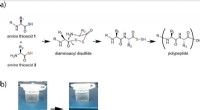 Dannelse af kunstig peptidbinding giver spor til skabelse af liv på JordenPolypeptiddannelse ved den oxidative reaktion af aminosyrer. (a) Amino thioacids 1 og 2 kobles via et diaminoacyldisulfid-mellemprodukt, og efterfølgende intramolekylær amiddannelse genererer en alfa-
Dannelse af kunstig peptidbinding giver spor til skabelse af liv på JordenPolypeptiddannelse ved den oxidative reaktion af aminosyrer. (a) Amino thioacids 1 og 2 kobles via et diaminoacyldisulfid-mellemprodukt, og efterfølgende intramolekylær amiddannelse genererer en alfa- -
 Forskning finder alvorlige problemer med retsmedicinsk softwareKredit:CC0 Public Domain Ny forskning fra North Carolina State University og University of South Florida finder betydelige fejl i nyligt frigivet retsmedicinsk software designet til at vurdere ind
Forskning finder alvorlige problemer med retsmedicinsk softwareKredit:CC0 Public Domain Ny forskning fra North Carolina State University og University of South Florida finder betydelige fejl i nyligt frigivet retsmedicinsk software designet til at vurdere ind -
 Forskning i ren luft omdanner giftig luftforurening til industrikemikalieMFM-520. Kredit:University of Manchester Et giftigt forurenende stof produceret ved afbrænding af fossile brændstoffer kan opsamles fra udstødningsgasstrømmen og omdannes til nyttige industrielle
Forskning i ren luft omdanner giftig luftforurening til industrikemikalieMFM-520. Kredit:University of Manchester Et giftigt forurenende stof produceret ved afbrænding af fossile brændstoffer kan opsamles fra udstødningsgasstrømmen og omdannes til nyttige industrielle -
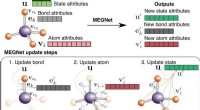 Ingeniører bruger grafnetværk til nøjagtigt at forudsige egenskaber af molekyler og krystallerSkematisk illustration af MEGNet-modeller. Kredit:Chi Chen/Materials Virtual Lab Nanoingeniører ved University of California San Diego har udviklet nye deep learning-modeller, der præcist kan foru
Ingeniører bruger grafnetværk til nøjagtigt at forudsige egenskaber af molekyler og krystallerSkematisk illustration af MEGNet-modeller. Kredit:Chi Chen/Materials Virtual Lab Nanoingeniører ved University of California San Diego har udviklet nye deep learning-modeller, der præcist kan foru
- Hvilken struktur transporterer protein?
- Styr ioner til kvanteberegning og sensing via fiberoptik på chip
- Sjældent gasfund løser gåden i det sydlige Afrikas skyhøje landskab
- Nyt papir viser fordelene ved kystrestaurering i Louisiana til kulstofbinding i jorden
- Topudgiverteams med topproducent af tosprogede materialer
- Regnskabsprocedureloven ændrer, hvordan udenlandske virksomheder konvergerer mod amerikanske regler…


