Ammoniumchlorid:sure egenskaber, sammensætning og praktiske anvendelser
Ammoniumchlorid:sure egenskaber, sammensætning og praktiske anvendelser
Af Sushil Khadka – Opdateret 30. august 2022
kirisa99/iStock/GettyImages
Ammoniumchlorid (NH4 Cl), almindeligvis kaldet sal ammoniak, er et hvidt krystallinsk salt dannet ved reaktionen af ammoniak (NH3 ) med saltsyre (HCl). Det er meget opløseligt i vand og danner, når det er opløst, en opløsning, der er let sur.
TL;DR
Ammoniumchlorid er et vandopløseligt salt af ammoniak, der giver en let sur opløsning. I vand danner chloridioner H⁺, mens ammoniumioner producerer OH⁻ gennem ligevægt med ammoniak.
Vandigt ammoniumchlorid
Opløser NH4 Cl-krystaller i vand initierer en række ligevægte:
NH4Cl(s) ⇌ NH4⁺(aq) + Cl⁻(aq) NH4⁺(aq) + H2O(l) ⇌ NH3(aq) + H3O⁺(aq) H3O⁺(aq) + OH⁻(aq) ⇌ 2 H2O(l)
Disse reaktioner viser, at saltet spaltes i dets bestanddele, og ammoniumionen kan fungere som en svag base, mens chloridionen kan bidrage til surhedsgraden via dannelsen af HCl i opløsning.
Sur komponent
I vandig opløsning associeres chloridioner med vand for at danne saltsyre:
Cl⁻(aq) + H2O(l) ⇌ HCl(aq) ⇌ H⁺(aq) + Cl⁻(aq)
Fordi HCl er en stærk syre, har den samlede opløsning en let sur karakter.
Grundlæggende komponent
Ammoniumioner ækvilibrerer med vand for at generere ammoniak og hydroxid:
NH4⁺(aq) + H2O(l) ⇌ NH3(aq) + OH⁻(aq)
Denne svage base modvirker surhedsgraden, men neutraliserer den ikke fuldstændigt, hvilket efterlader opløsningen let sur.
Sur natur og anvendelser
Den beskedne surhedsgrad af ammoniumchlorid kan bekræftes med et pH-meter, der typisk falder mellem 5,5 og 6,5. Dens praktiske anvendelser omfatter:
- Gødning: Giver let tilgængelig ammoniak til afgrøder som majs, hvede, byg og ris.
- Snebehandling: Anvendes på skiløjper over 0°C (32°F) for at hærde sne og forbedre trækkraften.
Dens rolle inden for landbrug og vintersport viser dens alsidighed og betydning i dagligdagens kemi.
 Varme artikler
Varme artikler
-
 Forskere opdager tilgang til at aktivere inerte gasserKredit:CC0 Public Domain Inerte gasser som argon danner typisk ikke kemiske bindinger undtagen under ekstreme forhold, såsom isens kolde kulde i det ydre rum. Som delt i Proceedings of the Nationa
Forskere opdager tilgang til at aktivere inerte gasserKredit:CC0 Public Domain Inerte gasser som argon danner typisk ikke kemiske bindinger undtagen under ekstreme forhold, såsom isens kolde kulde i det ydre rum. Som delt i Proceedings of the Nationa -
 Beskyttelsesmembran til pacemakere forhindrer opbygning af fibrotisk vævEn cellulosemembran til beskyttelse af pacemakere. Kredit:Hylomorph En beskyttende membran til pacemakere udviklet ved ETH Zürich har vist sig vellykket i dyreforsøg med at reducere den uønskede o
Beskyttelsesmembran til pacemakere forhindrer opbygning af fibrotisk vævEn cellulosemembran til beskyttelse af pacemakere. Kredit:Hylomorph En beskyttende membran til pacemakere udviklet ved ETH Zürich har vist sig vellykket i dyreforsøg med at reducere den uønskede o -
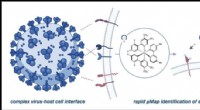 Forskere identificerer flere mulige indgangspunkter for COVID-spidsproteinVærtscelle- og virusgrænsefladen kan være kompleks og involvere mange proteiner, men µMap muliggør direkte undersøgelse af funktionelt vigtige interaktioner. Kredit:Saori Suzuki et al., Journal of the
Forskere identificerer flere mulige indgangspunkter for COVID-spidsproteinVærtscelle- og virusgrænsefladen kan være kompleks og involvere mange proteiner, men µMap muliggør direkte undersøgelse af funktionelt vigtige interaktioner. Kredit:Saori Suzuki et al., Journal of the -
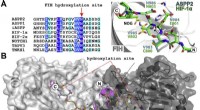 Hydroxyleringen af ASPP2 og andre ankyrin-gentagelsesdomæneproteinerUdsigter fra krystalstrukturer af FIH i kompleks med ASPP-afledte peptider. En (venstre) sekvensjustering af ASPP-proteiner med rapporterede FIH-substrater. (Højre) Overlejring af krystalstrukturafled
Hydroxyleringen af ASPP2 og andre ankyrin-gentagelsesdomæneproteinerUdsigter fra krystalstrukturer af FIH i kompleks med ASPP-afledte peptider. En (venstre) sekvensjustering af ASPP-proteiner med rapporterede FIH-substrater. (Højre) Overlejring af krystalstrukturafled
- Hvad udgør en nukleinsyre?
- Hvor lang tid tog det at nå månen i Apollo 11?
- Hvordan kan fossiler bruges til at datere klipper?
- Plastfantastiske eller naturbaserede legepladser:Hvilken er bedst for børns udvikling?
- Miami kemis gennembrudsteknik muliggør design i grænsefladen mellem kemi og biologi
- Slaveskibsmodel bringer en rystende historie til live i 3D


