Hvad er tallet før en kemisk formel kaldet i en reaktionsligning?
I en kemisk reaktionsligning kaldes et tal, der vises før en kemisk formel en koefficient . Koefficienter bruges til at afbalancere ligningen, hvilket sikrer, at det samme antal atomer af hvert element vises på både reaktant- og produktsiden. Denne praksis følger loven om bevarelse af masse, som siger, at masse ikke kan skabes eller ødelægges i en kemisk reaktion.
Tallet, der vises til højre for et elementsymbol i en formel, er et nedskrevet . Nedskrevne angiver antallet af atomer af det element i forbindelsen og er faste; de kan ikke ændres ved afbalancering af en ligning.
Afbalancering af en simpel reaktion:Brint og ilt til dannelse af vand
Ubalanceret ligning:H2 + O2 → H2 O
Trin 1 – Juster produktsiden:H2 + O2 → 2H2 O
Trin 2 – Balancer hydrogenatomer:2H2 + O2 → 2H2 O
Resultat:Fire brintatomer og to oxygenatomer på begge sider, så ligningen er afbalanceret.
Generelle trin til afbalancering af kemiske ligninger
1. Identificer den mest komplekse forbindelse
Vælg et element, der optræder i en enkelt forbindelse på den ene side af ligningen. Tilføj en koefficient til den forbindelse for at udligne antallet af atomer i det element på begge sider.
2. Balancer polyatomiske ioner som hele enheder
Behold ioner som NO3 - eller CO3 2- intakt. For eksempel:
Ubalanceret:Ca + HNO3 → H2 + Ca(NEJ3 )2
Balanceret:Ca + 2HNO3 → H2 + Ca(NO3 )2
3. Balancere resterende elementer
Efter håndtering af de komplekse arter skal du justere koefficienter for eventuelle resterende elementer. Til forbrænding af heptan:
Ubalanceret:C7 H16 + O2 → CO2 + H2 O
Balanceret:C7 H16 + 11O2 → 7CO2 + 8H2 O
4. Bekræft dit arbejde
Tæl hvert element på begge sider for at bekræfte lighed. For komplekse ligninger, overvej at oprette en tabel til at spore atomantal.
kivitimof/iStock/GettyImages
 Varme artikler
Varme artikler
-
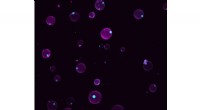 Kunstige celler reagerer på miljøændringerSyntetiske celler med rum. Magenta viser lipidmembranen, cyan viser de fluorescensmærkede membranfrie underrum. Kredit:MPI-CBG/ Love et al. Celler er den grundlæggende enhed i livet. De giver et m
Kunstige celler reagerer på miljøændringerSyntetiske celler med rum. Magenta viser lipidmembranen, cyan viser de fluorescensmærkede membranfrie underrum. Kredit:MPI-CBG/ Love et al. Celler er den grundlæggende enhed i livet. De giver et m -
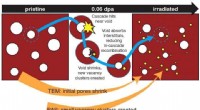 Ikke-destruktive positronstråler sondeskade, understøtte sikkerhedsfremskridt i strålingsmiljøerEn kombination af positron-annihilationsspektroskopi og transmissionselektronmikroskopi afslører ny indsigt i, hvordan skader dannes i bestrålede materialer, foreslår en mekanisme, hvor store huller i
Ikke-destruktive positronstråler sondeskade, understøtte sikkerhedsfremskridt i strålingsmiljøerEn kombination af positron-annihilationsspektroskopi og transmissionselektronmikroskopi afslører ny indsigt i, hvordan skader dannes i bestrålede materialer, foreslår en mekanisme, hvor store huller i -
 Tilbereder en måde at fjerne mikroplastik fra spildevandet – med okra, aloeKredit:Pixabay/CC0 Public Domain I mange køkkener fungerer okra som en mester fortykningsmiddel af gryderetter og supper. Smulden fra den frugt og andre planter, såsom aloe, kaktus og psyllium, kan
Tilbereder en måde at fjerne mikroplastik fra spildevandet – med okra, aloeKredit:Pixabay/CC0 Public Domain I mange køkkener fungerer okra som en mester fortykningsmiddel af gryderetter og supper. Smulden fra den frugt og andre planter, såsom aloe, kaktus og psyllium, kan -
 Mælkeprotein kan hjælpe med at øge blåbærs sundhedEn modnende Polaris blåbær (Vaccinium corymbosum) Kredit:Public Domain At parre blåbærtærte med en kugle is er en dejlig sommeroplevelse. Udover at være velsmagende, denne kombination kan også hjæ
Mælkeprotein kan hjælpe med at øge blåbærs sundhedEn modnende Polaris blåbær (Vaccinium corymbosum) Kredit:Public Domain At parre blåbærtærte med en kugle is er en dejlig sommeroplevelse. Udover at være velsmagende, denne kombination kan også hjæ
- Hvor i verden bruger de solenergi?
- Hvorfor fossil og solenergi det samme?
- Mest førskole matematik, alfabetiseringsapps, der ikke er designet til at hjælpe børn med at lær…
- Forskere bruger nanopartikler til at gøre fotodetektorer bedre i stand til at håndtere den ultravi…
- Sådan beregnes Km
- Hvor tyk er asthenosfæren i miles?


