Danner diskrete molekyler bindinger? Udforskning af binding i diskrete stoffer
Creatas/Creatas/Getty Images
Bring to magneter tæt sammen, og inden for en vis afstand vil de to magneter trække mod hinanden og derefter sætte sig fast. Når de trækkes fra hinanden, er magneterne stadig intakte, kun adskilt fra hinanden. Hvis molekyler opfører sig på denne måde - uanset om de er sammen eller trukket fra hinanden, bevarer de molekylær identitet - betragtes de som diskrete molekyler.
Diskret vs. kontinuerligt synspunkt
Diskret vs. kontinuerligt synspunkt
Diskret molekyler bevarer molekylær identitet, og sådanne molekyler ville fungere som adskilte enheder af stof, som sandkorn. Dette ville forklare, hvorfor molekyler eller grundstoffer kunne "klistre" sammen i en kemisk binding.
At blive betragtet som kontinuerlig , ville der ikke være skarpe opdelinger, og ét grundstof eller molekyle ville blande sig i et andet i en kemisk binding. Dette ville forklare stabilitet eller magnetismens kraft. Bemærk, at molekyler ikke er betragtes som indiskret.
Diskret versus kontinuerlig er analog med at spørge, om universets bestanddele fungerer som partikler eller bølger.
Diskrete molekyler og elementære former
Diskret
Molekyler og grundstoffer
I det diskrete synspunkt kan molekyler betragtes som diskrete i, hvordan de virker på molekylært niveau. Diskret partikelkemi betragter molekyler eller grundstoffer som diskrete afhængigt af manglen på interaktion.
Elementer i deres elementære form kan betragtes som diskrete. Et element i sin elementære form er kun sammensat af det element og ikke kombineret med andre elementer. Elementet ville eksistere frit (ukombineret) i naturen. Sådanne stoffer, selvom de tilsyneladende er enkle, produceres sjældent i ren form i naturen.
Alle ædelgasser eksisterer i elementær form. Et eksempel på et metal i elementær form ville være guld, da det kan findes i naturen i sin elementære tilstand. Andre grundstoffer fundet ukombineret er kobber, sølv, svovl og kulstof.
Diskrete molekyler:diatomiske og andre molekyler
Diskrete molekyler:
Diatomiske og andre molekyler
Flere af ikke-metallerne eksisterer som gasser ved stuetemperatur og som diatomiske molekyler:H2, N2, O2, F2, Cl2, I2 og Br2. Disse fungerer som diskrete molekyler.
Overvej også molekyler såsom vand, der eksisterer i diskret form gennem forskellige stoftilstande, såsom væske eller fast stof. Når isen smelter, ændrer den tilstand, men bevarer sin diskrete identitet.
Andre faste tilstande ville ikke opretholde denne diskrete identitet. For eksempel bryder almindeligt salt, NaCl, til ioner i en vandig tilstand og vil ikke blive betragtet som diskret.
Diskrete molekyler og bindingskræfter
Diskret
Molekyler og bindingskræfter
Diskrete molekyler ville generelt ikke interagere med andre molekyler.
Dipol-dipol-interaktioner og London-dispersionskræfter er to intermolekylære krafter s, der tillader diskrete molekyler at binde sig til hinanden, som mange små magneter ville.
Dipol-dipol-interaktioner
Dipol-dipol-interaktioner
I dipol-dipol-interaktioner dannes en delvis ladning i molekylet på grund af den ujævne fordeling af elektroner. En dipol er et par modsatte ladninger adskilt af en afstand. Et særligt tilfælde af en dipol-dipol-interaktion er hydrogenbinding.
Hydrogenbinding sker mellem to separate molekyler. Ved hydrogenbinding skal hvert molekyle have et hydrogenatom, der er kovalent bundet til et andet atom, der er mere elektronegativt. Det mere elektronegative atom vil trække de delte elektroner i den kovalente binding mod sig selv og danne delvise positive ladninger.
Overvej for eksempel vandmolekylet, H2O. Mellem hydrogenbindingen af et vandmolekyle og oxygenbindingen af et andet er der en vekselvirkning baseret på de partielle positive (hydrogenatom) og partielle negative (iltatom) ladninger.
Disse to små ladninger gør hvert enkelt vandmolekyle til en svag magnet, der vil tiltrække andre adskilte vandmolekyler.
LondonDispersion Forces
London
Spredningskræfter
London spredningskræfter er den svageste intermolekylære kraft. Det er en midlertidig tiltrækning, der sker, når elektroner på to tilstødende atomer interagerer for at danne midlertidige dipoler.
Normalt danner kun polære molekyler dipoler. Det vil sige elementer, der binder og har en ret høj elektronegativitetsforskel. Men selv upolære molekyler, dem der ikke har delvise elektriske ladninger i sig, kan have midlertidige let negative ladninger.
Da elektroner ikke er stationære, er det muligt, at mange af de negativt ladede elektroner kan være nær den ene ende af molekylet. I dette øjeblik har molekylet en let (omend momentan) negativ ende. Samtidig vil den anden ende momentvis være svagt positiv.
Denne øjeblikkelige dipol skaber en momentan polær karakter og kan tillade diskrete molekyler at interagere med nabomolekyler.
 Varme artikler
Varme artikler
-
 Neutroner undersøger iltgenererende enzym for en grønnere tilgang til rent vandKloritdismutase er et unikt oxygendannende enzym, der nedbryder chlorit, et industrielt forurenende stof, der findes globalt i grundvandet, drikkevand og jord. Forskning udført på ORNL bidrager til en
Neutroner undersøger iltgenererende enzym for en grønnere tilgang til rent vandKloritdismutase er et unikt oxygendannende enzym, der nedbryder chlorit, et industrielt forurenende stof, der findes globalt i grundvandet, drikkevand og jord. Forskning udført på ORNL bidrager til en -
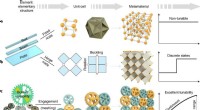 Gear-baserede mekaniske metamaterialer giver mulighed for oprettelse af konfigurerbare arkDesignkoncepter af mekaniske metamaterialer. a,b, klassisk paradigme:ikke-afstembart metamateriale (a) og typisk rekonfigurerbart metamateriale (b). c, Gear-baserede metamaterialer. Kredit:Nature Mate
Gear-baserede mekaniske metamaterialer giver mulighed for oprettelse af konfigurerbare arkDesignkoncepter af mekaniske metamaterialer. a,b, klassisk paradigme:ikke-afstembart metamateriale (a) og typisk rekonfigurerbart metamateriale (b). c, Gear-baserede metamaterialer. Kredit:Nature Mate -
 Forståelse af Calvins cyklus:Lysuafhængig fotosyntese forklaretFotosyntese er en to-trins proces. For det første udnytter lysafhængige reaktioner solenergi til at generere ATP og NADPH. For det andet bruger de lysuafhængige reaktioner – også kaldet Calvin cyklus
Forståelse af Calvins cyklus:Lysuafhængig fotosyntese forklaretFotosyntese er en to-trins proces. For det første udnytter lysafhængige reaktioner solenergi til at generere ATP og NADPH. For det andet bruger de lysuafhængige reaktioner – også kaldet Calvin cyklus -
 Bekæmpelse af svampeinfektioner med metallerEn petriskål med rød agar, hvorpå der vokser en svampetråd i form af elementsymbolet for platin (Pt). Kredit:CO-ADD Hvert år får mere end 1 milliard mennesker en svampeinfektion. Selvom de er uskad
Bekæmpelse af svampeinfektioner med metallerEn petriskål med rød agar, hvorpå der vokser en svampetråd i form af elementsymbolet for platin (Pt). Kredit:CO-ADD Hvert år får mere end 1 milliard mennesker en svampeinfektion. Selvom de er uskad
- Hvilken type virus inkorporerer dets genetiske materiales værtskromosomer?
- Hvor lever skildpadder og laver deres æg?
- Arver hvert dyr den samme blanding af gener fra dets forældre?
- Afblegning af koralrev viser alvorlige havcirkulationsændringer
- Afsløring af fremtiden for fotonik:Hydrogel-innovationer baner vejen
- Komet eller asteroide? Forskere ID interstellar gæst


