Afbalancering af magnesiumoxidligningen:En trin-for-trin-vejledning
Af Caroline Depalma, Opdateret 24. marts 2022
Hemera Technologies/PhotoObjects.net/Getty Images
Afbalancering af kemiske ligninger er en grundlæggende færdighed i kemi, der sikrer, at loven om bevarelse af masse holder stik. I denne kortfattede vejledning gennemgår vi det enkleste eksempel – dannelse af magnesiumoxid (MgO) fra magnesium (Mg) og oxygengas (O2 ). Trinene er designet til at være klare for studerende, undervisere og alle, der er interesseret i at styrke deres forståelse af støkiometri og ionbinding.
Trin 1:Identificer reaktanter og produkter
Skriv den ubalancerede ligning:
Mg + O2 → MgO
Trin 2:Tæl atomer på hver side
Til venstre har du 1 Mg-atom og 2 O-atomer (da O2 er diatomisk). Til højre har du 1 Mg og 1 O-atom.
Trin 3:Anvend ioniske bindingsprincipper
Magnesium (et gruppe 2 metal) danner typisk en 2+ ion, mens oxygen (et gruppe 16 ikke-metal) accepterer to elektroner for at danne en 2− ion. Den resulterende formel, MgO, afspejler dette 1:1-forhold mellem Mg²⁺ og O²⁻.
Trin 4:Balancer ligningen
For at matche ilttallet skal du placere en koefficient på 2 før magnesium på reaktantsiden og en koefficient på 2 før MgO på produktsiden:
2 Mg + O2 → 2 MgO
Ting, du skal bruge
- Periodisk tabel (for at bekræfte oxidationstilstande)
- Grundlæggende viden om ionbinding
- Blyant og papir (eller en digital note-app)
TL;DR
For ioniske forbindelser afspejler forholdet mellem grundstoffer ofte deres typiske ladninger. Her parres Mg (2+) med O (2−) for at danne MgO, så man fordobler simpelthen magnesiumkoefficienten for at balancere ilt.
Vigtig bemærkning
Selvom dette eksempel er ligetil, kan reaktioner i den virkelige verden involvere flere reaktanter, produkter eller reversible processer. Tjek altid din specifikke kontekst, og hvis du er i tvivl, kontakt din instruktør eller en pålidelig kemi-ressource.
Reference
- Tro, Nivaldo. Kemi:En molekylær tilgang , 2007.
 Varme artikler
Varme artikler
-
 Kemisk grundlag for papirproduktion:Fra kraftmasse til avanceret blegning og fiberbehandlingerNA/Photos.com/Getty Images Papir fremstår simpelt, men dets fremstilling er afhængig af sofistikeret kemi. Ved at omdanne brune træflis til lyse, alsidige ark fremviser papirindustrien en række præci
Kemisk grundlag for papirproduktion:Fra kraftmasse til avanceret blegning og fiberbehandlingerNA/Photos.com/Getty Images Papir fremstår simpelt, men dets fremstilling er afhængig af sofistikeret kemi. Ved at omdanne brune træflis til lyse, alsidige ark fremviser papirindustrien en række præci -
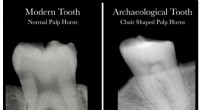 Videnskab møder arkæologi med opdagelsen af, at tandrøntgenstråler afslører D-vitaminmangelSammenligning af tandrøntgenbilleder fra patienter med og uden D-vitaminmangel. Kredit:McMaster University Menneskelige tænder rummer vital information om D-vitaminmangel, en alvorlig, men ofte sk
Videnskab møder arkæologi med opdagelsen af, at tandrøntgenstråler afslører D-vitaminmangelSammenligning af tandrøntgenbilleder fra patienter med og uden D-vitaminmangel. Kredit:McMaster University Menneskelige tænder rummer vital information om D-vitaminmangel, en alvorlig, men ofte sk -
 Hvorfor Tjernobyl var en forudsigelig katastrofeHvorfor Tjernobyl var en forudsigelig katastrofe Når folk tænker på Tjernobyl, forestiller de sig ofte en katastrofe fra den ene dag til den anden, som syntes uundgåelig. I virkeligheden var begivenh
Hvorfor Tjernobyl var en forudsigelig katastrofeHvorfor Tjernobyl var en forudsigelig katastrofe Når folk tænker på Tjernobyl, forestiller de sig ofte en katastrofe fra den ene dag til den anden, som syntes uundgåelig. I virkeligheden var begivenh -
 Kirigami kan dreje terahertz -stråler i realtid for at kigge ind i biologisk vævAtelier Kirigami/Origami. Cristian Bortes, CC BY 2.0. Med en letspinningsanordning inspireret af den japanske kunst at skære papir, University of Michigan forskere har fundet mikroskopiske vending
Kirigami kan dreje terahertz -stråler i realtid for at kigge ind i biologisk vævAtelier Kirigami/Origami. Cristian Bortes, CC BY 2.0. Med en letspinningsanordning inspireret af den japanske kunst at skære papir, University of Michigan forskere har fundet mikroskopiske vending
- Lavt iltniveau i søer og reservoirer kan fremskynde globale ændringer
- Alabama museum for at genoprette mockup af rumfærge i fuld størrelse
- Hvis du har 25 g zink og 300 g svovl, hvad er masseoverskydende reaktant?
- Hvad er kvantitetsaktivitet?
- Hvilket instrument målte varme?
- Hvad er den elektroniske konfiguration af kobber?


