Fordampning vs. kogning:De to nøgleformer for fordampning
Af John McDaniel , Opdateret 24. marts 2022
Fordampning er overgangen af en væske til en gas. I dagligdagens videnskab driver to primære mekanismer denne proces:fordampning og kogning. At forstå nuancerne mellem dem er afgørende for områder lige fra meteorologi til kulinarisk kunst.
Fordampning
Fordampning sker ved væskens overflade, når individuelle molekyler absorberer nok kinetisk energi - typisk fra varme - til at overvinde intermolekylære kræfter. Disse energigivende molekyler bryder fri og stiger op i luften som damp. Et almindeligt eksempel er en vandpyt, der tørrer på en solskinsdag, eller vand, der fordamper fra en søs overflade.
Kogning
Kogning er en masseproces, der kræver, at hele væsken når sit kogepunkt - den temperatur, hvor damptrykket er lig med atmosfæretrykket. Ved denne tærskel dannes dampbobler i væsken og stiger til overfladen og frigiver gas. Kogning er det, der sker, når du opvarmer vand på et komfur, indtil dampen synligt bryder ud.
Primære forskelle
Mens begge processer omdanner væske til gas, adskiller de sig fundamentalt i skala og observerbare tegn:
- Omfang: Fordampning er overfladebegrænset; kogning involverer hele volumen.
- Tryk: Kogning kræver damptryk for at matche eksternt tryk; fordampning sker ved lavere damptryk.
- Indikatorer: Kogning er præget af kraftig bobledannelse; fordampning er subtil og ofte usynlig.
Perspektiv på atomniveau
På molekylært niveau accelererer temperaturstigning molekylær bevægelse. Når den kinetiske energi overstiger bindingskræfterne, dissocieres molekyler og spredes som gas. Afkøling vender denne proces om, hvilket tillader molekyler at re-associere til en flydende tilstand.
For et dybere dyk ned i fysikken om kogning og fordampning, se Wikipedia-indlægget om kogning eller American Society of Heating, Refrigerating and Air-Conditioning Engineers (ASHRAE) retningslinjer for fordampningsprocesser.
 Varme artikler
Varme artikler
-
 Tellurium gør forskellenProfessor Wolfgang Weigand fra det tyske universitet i Jena viser usædvanlige strukturer af tellurforbindelser. Kredit:Anne Günther/Uni Jena Det periodiske system indeholder 118 kemiske grundstoff
Tellurium gør forskellenProfessor Wolfgang Weigand fra det tyske universitet i Jena viser usædvanlige strukturer af tellurforbindelser. Kredit:Anne Günther/Uni Jena Det periodiske system indeholder 118 kemiske grundstoff -
 Teknologi forlænger holdbarheden af mejerieksportEn sprøjtetørrer i pilotskala i laboratoriet til fødevarekvalitet i Monash University. Kredit:Monash University En række tørreteknologiplatforme udviklet af forskere ved Monash University kan hjæl
Teknologi forlænger holdbarheden af mejerieksportEn sprøjtetørrer i pilotskala i laboratoriet til fødevarekvalitet i Monash University. Kredit:Monash University En række tørreteknologiplatforme udviklet af forskere ved Monash University kan hjæl -
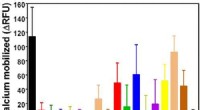 Oksekødspeptider blokerer for bitter smagKredit:American Chemical Society Fra burgere til bøffer, oksekød har en lang historie for at være en lækker del af aftensmaden. Men hvad nu hvis den behagelige oplevelse med at spise oksekød kunne
Oksekødspeptider blokerer for bitter smagKredit:American Chemical Society Fra burgere til bøffer, oksekød har en lang historie for at være en lækker del af aftensmaden. Men hvad nu hvis den behagelige oplevelse med at spise oksekød kunne -
 Magnetiske bakterier som mikropumperKredit:Unsplash/CC0 Public Domain ETH-forskere bruger magnetiske bakterier til at kontrollere væsker på mikroniveau. De overvejer allerede at bruge dem i den menneskelige blodbane til præcis lever
Magnetiske bakterier som mikropumperKredit:Unsplash/CC0 Public Domain ETH-forskere bruger magnetiske bakterier til at kontrollere væsker på mikroniveau. De overvejer allerede at bruge dem i den menneskelige blodbane til præcis lever


