Hvorfor det periodiske system er opbygget efter atomnummer:Rækker og kolonner forklaret
Af David Chandler, Opdateret 24. marts 2022
Jupiterimages/Photos.com/Getty Images
Det periodiske system arrangerer grundstoffer i rækkefølge efter stigende atomnummer - antallet af protoner i kernen. Denne rækkefølge afslører systematiske mønstre i kemisk adfærd, som vises i rækker (perioder) og kolonner (grupper).
Atomnummer
Atomnummeret identificerer entydigt hvert element. For eksempel er carbons atomnummer seks, svarende til dets seks protoner.
Neutrale atomer
Et neutralt atom har lige mange elektroner og protoner. Et neutralt kulstofatom indeholder således seks elektroner og seks protoner.
Elektronkonfiguration
Elektroner fylder energiskaller fra lavest til højeste. Elektroner i den yderste skal – valenselektroner – styrer, hvordan et atom binder sig til andre.
Perioder
Rækker på bordet kaldes perioder. Alle elementer inden for en periode deler en valensskal; antallet af valenselektroner stiger fra venstre mod højre. Når en skal er fyldt, starter en ny periode.
Grupper
Kolonner eller grupper samler elementer, der deler det samme antal valens-elektroner, hvilket giver dem lignende kemiske egenskaber. For eksempel har jordalkalimetallerne (Gruppe 2) hver to valenselektroner og udviser sammenlignelig reaktivitet.
Ved at kortlægge atomnummer og elektronkonfiguration på et to-dimensionelt gitter giver det periodiske system en forudsigelig ramme for kendte og endnu ikke-opdagede grundstoffer.
 Varme artikler
Varme artikler
-
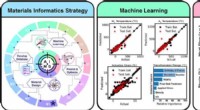 Ny formhukommelseslegering opdaget gennem kunstig intelligens-rammeGrafisk abstrakt. Kredit:Acta Materialia (2022). DOI:10.1016/j.actamat.2022.117751 Forskere fra Department of Materials Science and Engineering ved Texas A&M University har brugt en Artificial Inte
Ny formhukommelseslegering opdaget gennem kunstig intelligens-rammeGrafisk abstrakt. Kredit:Acta Materialia (2022). DOI:10.1016/j.actamat.2022.117751 Forskere fra Department of Materials Science and Engineering ved Texas A&M University har brugt en Artificial Inte -
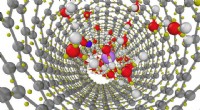 Indkredsning af virkningerne af nanoindeslutning på vandStruktur af en lithiumchloridopløsning indespærret i et 1,1 nanometer diameter carbon nanorør som opnået fra første principper molekylær dynamik simuleringer. Billede af Viktor Rozsa/University of Chi
Indkredsning af virkningerne af nanoindeslutning på vandStruktur af en lithiumchloridopløsning indespærret i et 1,1 nanometer diameter carbon nanorør som opnået fra første principper molekylær dynamik simuleringer. Billede af Viktor Rozsa/University of Chi -
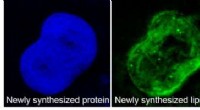 Kortlægning af den indre funktion i en levende celleDa levende celler absorberer tungt vand, deuterium er inkorporeret i nylavede proteiner, lipider og DNA. Da forskerne rettede lyset fra et stimuleret Raman -spredning (SRS) mikroskop mod en enkelt cel
Kortlægning af den indre funktion i en levende celleDa levende celler absorberer tungt vand, deuterium er inkorporeret i nylavede proteiner, lipider og DNA. Da forskerne rettede lyset fra et stimuleret Raman -spredning (SRS) mikroskop mod en enkelt cel -
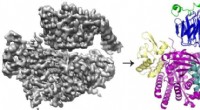 Undersøgelse afslører den indviklede måde, hvorpå to proteiner interagerer for at fremme cellebe…Cryo-EM 3D-rekonstruktionen (til venstre) af proteinet P-Rex1 bundet til Gβγ og proteinmodellen (til højre), der viser, at Gβγ (øverst; blå og grøn) binder til en kompakt, multi-domæne overflade på P-
Undersøgelse afslører den indviklede måde, hvorpå to proteiner interagerer for at fremme cellebe…Cryo-EM 3D-rekonstruktionen (til venstre) af proteinet P-Rex1 bundet til Gβγ og proteinmodellen (til højre), der viser, at Gβγ (øverst; blå og grøn) binder til en kompakt, multi-domæne overflade på P-
- Hvilke robotter bruges i dag?
- Mindre end 1% sandsynlighed for, at jordens energiubalance øges naturligt, siger forskere
- Opdagelsen af Comet SWAN af sol-watcher SOHO
- Træfald i den tørre sæson i São Paulo City skyldes dårlig forvaltning, undersøgelse tyder på
- 10 ounces er hvilken brøkdel af et pund?
- Hvad er de eneste to typer celler, der har spændende membraner?


