Konvertering af muldvarpe til millimoler:en praktisk guide
Af Sophie Johnson, Opdateret 24. marts 2022
Et mol er en fast mængde partikler – atomer, molekyler, ioner eller elektroner – svarende til antallet af atomer i 12 gram af kulstof-12-isotopen. Denne standard, etableret af International Union of Pure and Applied Chemistry (IUPAC), tillader kemikere at tælle mikroskopiske enheder i bulk-termer.
Trin 1 – Forstå forholdet
Der er 1.000 millimol i én mol:1 mol=1.000 mmol . Tilsvarende 1 mmol=0,001 mol . I fraktioneret form er dette udtrykt som 1 mol/1.000 mmol eller dets gensidige.
Trin 2 – Skriv konverteringsformlen
Vælg det format, der matcher dine beregningsbehov. For hurtige konverteringer skal du bruge den simple ligning 1 mol=1.000 mmol . For detaljeret arbejde, skriv brøknotationen:1.000 mmol/1 mol .
Trin 3 – Anvend formlen
Gang antallet af mol du har med konverteringsfaktoren. For eksempel for at konvertere 2 mol til millimol:
2 mol × 1,000 mmol/1 mol = 2,000 mmolHvis du starter med millimol, skal du vende fraktionen i overensstemmelse hermed.
Ting, du skal bruge
- Blyant
- Papir
- Lommeregner (valgfrit, for store tal)
TL;DR
Ved konvertering placeres målenheden oven på fraktionen. For mol→millimol skal du bruge 1.000 mmol/1 mol; for millimol→mol skal du bruge 1 mol/1.000 mmol .
Avogadros nummer – i øjeblikket 6,0221376×10 23 — er antallet af atomer i 12 g kulstof-12. Det er en målt konstant, der har udviklet sig med præcision; tidligere værdier i 1980'erne var 6,022045×10 23 .
Bemærkning om definitioner
Selvom Avogadros tal er bredt citeret, er molen defineret af den nøjagtige mængde atomer i 12 g kulstof-12, ikke af selve konstanten. Denne sondring understøtter alle støkiometriske beregninger i kemi.
 Varme artikler
Varme artikler
-
 Video:Forårsager sukker diabetes?Kredit:The American Chemical Society I USA, diabetes er meget almindelig - 1 ud af 10 personer har det, og titusindvis af mennesker dør af det hvert år. Hvis du har diabetes, du har alt for meget
Video:Forårsager sukker diabetes?Kredit:The American Chemical Society I USA, diabetes er meget almindelig - 1 ud af 10 personer har det, og titusindvis af mennesker dør af det hvert år. Hvis du har diabetes, du har alt for meget -
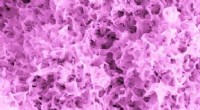 Proteiner koreograferer den uendelig lille dans af levende celler og funktionelle biomaterialerBlomsterlignende mikrostrukturer dannes på en nanoporøs glasmonolit med 31nm-diameter porer. Kredit:Lehigh University, Thamma, Kowal, Falk, Jain Et tværfagligt forskerhold ved Lehigh University ha
Proteiner koreograferer den uendelig lille dans af levende celler og funktionelle biomaterialerBlomsterlignende mikrostrukturer dannes på en nanoporøs glasmonolit med 31nm-diameter porer. Kredit:Lehigh University, Thamma, Kowal, Falk, Jain Et tværfagligt forskerhold ved Lehigh University ha -
 En ny katalysator til at bremse den globale opvarmningKredit:Shutterstock Russiske videnskabsmænd har udviklet en ny, højeffektiv katalysator til industriel forarbejdning af kuldioxid, der gør processen enkel og billig. Forskere fra MISIS University,
En ny katalysator til at bremse den globale opvarmningKredit:Shutterstock Russiske videnskabsmænd har udviklet en ny, højeffektiv katalysator til industriel forarbejdning af kuldioxid, der gør processen enkel og billig. Forskere fra MISIS University, -
 Hvordan man gør metangas flydende:Praktiske trin til sikker konverteringAf Andrew Mayfair J.D. Opdateret 24. marts 2022 Metan (CH4) er det enkleste carbonhydrid, der består af et carbonatom bundet til fire hydrogenatomer. Selvom det eksisterer naturligt som en gas under
Hvordan man gør metangas flydende:Praktiske trin til sikker konverteringAf Andrew Mayfair J.D. Opdateret 24. marts 2022 Metan (CH4) er det enkleste carbonhydrid, der består af et carbonatom bundet til fire hydrogenatomer. Selvom det eksisterer naturligt som en gas under
- Er kulnanorør den næste in-line til fremstilling af bærbar elektronik?
- Hvad er formlen for nitrogen og bromid?
- Regeringsvideoudstilling for at vise banebrydende
- Kan en natriumion kun danne en ionisk binding?
- Hvilken får flere elektroner, når to objekter gnides sammen?
- Ny teknik kan vise sammenhæng mellem byttedyr og mikroplast


