Egenskaber for faste stoffer, væsker og gasser forklaret
Af Kevin Lee | Opdateret 24. marts 2022
VvoeVale/iStock/Getty Images
Intermolekylære kræfter på arbejde
Atomer kombineres til molekyler såsom vand. Styrken af intermolekylære kræfter (IMF'er) bestemmer et stofs fase. Når IMF'er er svage, er stoffet typisk en gas ved 1atm og 25°C (77°F). Stærke IMF'er giver generelt et fast stof under de samme betingelser.
Faststoffer, væsker, gasser og partikeladfærd
I et fast stof overstiger partikeltiltrækningen kinetisk energi, og partiklerne er tæt pakket. Væsker har sammenlignelig kinetisk energi og tiltrækning, hvilket tillader partikler at glide forbi hinanden. Gasser indeholder vidt spredte partikler, hvis kinetiske energi dominerer over tiltrækning.
Faseovergange og deres drivere
Temperatur, tryk og sammensætning styrer faseændringer. Et fasediagram viser disse overgange. Almindelige processer omfatter fordampning (væske → gas), kondensation (gas → væske), sublimering (fast → gas), aflejring (gas → fast), frysning (væske → fast) og smeltning (fast → væske).
Sammenligning af faseforskelle
Is, flydende vand og vanddamp deler de samme molekyler, men adskiller sig i komprimerbarhed, form og volumenadfærd. Faste stoffer og væsker modstår kompression; gasser komprimeres let. Væsker og gasser tilpasser sig beholderformer, mens faste stoffer bevarer deres egen form. Gasser udvider sig også for at fylde hele deres beholder.
Sidste artikelByg din egen akvarie sump:En trin-for-trin guide
Næste artikelKonvertering af muldvarpe til millimoler:en praktisk guide
 Varme artikler
Varme artikler
-
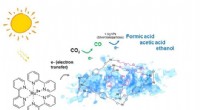 Ny lysaktiveret katalysator fanger CO2 for at lave ingredienser til brændstofSkematisk af en svampet nikkel-organisk fotokatalysator, der udelukkende omdanner carbondioxid til carbonmonoxid, som yderligere kan omdannes til flydende brændstof af høj værdi gennem synlig lys-indu
Ny lysaktiveret katalysator fanger CO2 for at lave ingredienser til brændstofSkematisk af en svampet nikkel-organisk fotokatalysator, der udelukkende omdanner carbondioxid til carbonmonoxid, som yderligere kan omdannes til flydende brændstof af høj værdi gennem synlig lys-indu -
 Ny biokemisk forbindelse kan nedbryde miljøforurenende stofferKredit:CC0 Public Domain Enzymer med flavinkofaktor spiller en vigtig rolle i planter, svampe, bakterier og dyr:som oxygenaser inkorporerer de ilt i organiske forbindelser. For eksempel giver dett
Ny biokemisk forbindelse kan nedbryde miljøforurenende stofferKredit:CC0 Public Domain Enzymer med flavinkofaktor spiller en vigtig rolle i planter, svampe, bakterier og dyr:som oxygenaser inkorporerer de ilt i organiske forbindelser. For eksempel giver dett -
 Et usandsynligt ægteskab blandt oxiderClaudia Cancellieri og Sebastian Siol undersøger heterostrukturelle legeringer på Empas Laboratory for Joining Technologies and Corrosion. Kredit:Swiss Federal Laboratories for Materials Science and T
Et usandsynligt ægteskab blandt oxiderClaudia Cancellieri og Sebastian Siol undersøger heterostrukturelle legeringer på Empas Laboratory for Joining Technologies and Corrosion. Kredit:Swiss Federal Laboratories for Materials Science and T -
 Skab en præcis 1 % saccharoseopløsning – trin-for-trin guideAf bidragende skribent – Opdateret 24. marts 2022 Astryda/iStock/GettyImages Bordsukker, eller saccharose, er et disaccharid, der består af glucose og fructose. Det er meget brugt i kulinariske appl
Skab en præcis 1 % saccharoseopløsning – trin-for-trin guideAf bidragende skribent – Opdateret 24. marts 2022 Astryda/iStock/GettyImages Bordsukker, eller saccharose, er et disaccharid, der består af glucose og fructose. Det er meget brugt i kulinariske appl
- Hvilke materialer opvarmes hurtigere?
- Hvordan frigøres energi fra olie?
- Beregn elektronhastighed ud fra spænding:En trin-for-trin guide
- Hvilke to processer skal finde sted, før en uoverensstemmelse kan dannes i geologi?
- Typer af chlorophyll til stede i Alger
- Mængden af energi, der frigives af et ørekage, måles på?


