Fysiske egenskaber for nitrogengas:massefylde, tilstande og industrielle anvendelser
TomekD76/iStock/GettyImages
Nitrogen tegner sig for 78,1% af Jordens atmosfære. På trods af dens træghed - så meget, at Lavoisier kaldte den "azote", hvilket betyder "uden liv" - er den uundværlig for liv og industri og danner rygraden i DNA, landbrugsgødning og adskillige industrielle processer.
Kenskaber
Nitrogengas (N2) er et ikke-metallisk, farveløst, lugtløst og smagløst diatomisk molekyle. Med et atomnummer på 7 og en atomvægt på 14,0067 har den en massefylde på 1,251gL⁻¹ ved 0°C og en specifik vægtfylde på 0,96737, lidt lettere end luft. Dets tredobbelte punkt – hvor gas, væske og fast stof eksisterer side om side – forekommer ved –210°C (63K) og 12,6 kPa.
Andre stater
Under dets kogepunkt på –195,79°C (77K) kondenserer nitrogen til flydende nitrogen, en klar, lugtfri væske, der ligner vand. Afkøling yderligere til dets smeltepunkt på –210°C (63K) giver et luftigt, snelignende fast stof.
Molekylær binding
I de fleste forbindelser danner nitrogen trivalente kovalente bindinger. N₂-molekylet indeholder en bemærkelsesværdig stærk tredobbeltbinding, understøttet af fem valenselektroner og en elektronegativitet på 3,04 (Pauling-skala), som understøtter dets kemiske stabilitet.
Anvendelser
Overfloden og den kemiske inertitet af nitrogen gør det uvurderligt i industrien. Det bruges i fødevarekonservering og brandslukningssystemer, beskytter iltfølsomme materialer såsom jern, stål og elektronik under fremstillingen og fungerer som et nøgleråmateriale til ammoniaksyntese via Haber-Bosch-processen.
Potentiale
I 2001 blev en undersøgelse offentliggjort i Nature rapporterede, at forskere ved Carnegie Institution of Washington omdannede gasformigt nitrogen til en fast tilstand ved at komprimere det mellem to diamantambolte under et tryk svarende til 1,7 millioner atmosfærer. Det resulterende faste stof lignede is, men havde alligevel et diamantlignende krystalgitter. Når trykket blev udløst ved temperaturer under -173,15°C (100K), forblev det faste stof stabilt. Faseovergangen frigiver betydelig energi, hvilket får fysiker Dr. Richard M. Martin til at spekulere over nitrogens potentiale som et højenergi-raketdrivstof.
 Varme artikler
Varme artikler
-
 Forskning giver håb om enklere kræftdiagnose og behandlingRyan Kelly i sit laboratorium. Kredit:Jaren Wilkey/BYU Overvågning af kræft kan ofte være en påtrængende og udmattende proces for patienter. Men med Brigham Young University kemiprofessor Ryan Kel
Forskning giver håb om enklere kræftdiagnose og behandlingRyan Kelly i sit laboratorium. Kredit:Jaren Wilkey/BYU Overvågning af kræft kan ofte være en påtrængende og udmattende proces for patienter. Men med Brigham Young University kemiprofessor Ryan Kel -
 UTA tildelte patent for smøremiddelsammensætning til universalfedt til flyPranesh Aswath, førende opfinder for denne forskning og professor i materialevidenskab og teknik og mekanisk og rumfartsteknik. Kredit:University of Texas i Arlington University of Texas i Arlingt
UTA tildelte patent for smøremiddelsammensætning til universalfedt til flyPranesh Aswath, førende opfinder for denne forskning og professor i materialevidenskab og teknik og mekanisk og rumfartsteknik. Kredit:University of Texas i Arlington University of Texas i Arlingt -
 Beregning af molaritet ud fra molekylvægt:En trin-for-trin guideAf Michael Judge Opdateret 30. august 2022 Forskere stoler på molaritet (M) til at udtrykke koncentrationen af en kemisk opløsning. Molaritet er defineret som antallet af mol af et opløst stof pr. l
Beregning af molaritet ud fra molekylvægt:En trin-for-trin guideAf Michael Judge Opdateret 30. august 2022 Forskere stoler på molaritet (M) til at udtrykke koncentrationen af en kemisk opløsning. Molaritet er defineret som antallet af mol af et opløst stof pr. l -
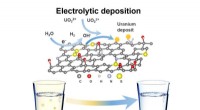 Brug af grafenskum til at filtrere toksiner fra drikkevandEt genanvendeligt 3D-funktionaliseret reduceret grafenoxidskum (3D-FrGOF) bruges som en in situ elektrolytisk aflejringselektrode til at udvinde uran fra forurenet vand. Kredit:MIT Nogle former fo
Brug af grafenskum til at filtrere toksiner fra drikkevandEt genanvendeligt 3D-funktionaliseret reduceret grafenoxidskum (3D-FrGOF) bruges som en in situ elektrolytisk aflejringselektrode til at udvinde uran fra forurenet vand. Kredit:MIT Nogle former fo
- Hvis solen var berømt, hvor ville den gå hen?
- Hvilket element viser spontan forbrænding?
- Kinesiske frivillige bruger 200 dage på virtuel månebase
- Forskere forklarer, hvordan grønne alger og bakterier sammen bidrager til klimabeskyttelse
- Soldrevet dyresporing transformerer, hvordan forskere indsamler data om dyr i naturen
- Hvorfor er ingen to emissionsspektre for forskellige elementer nogensinde de samme?


