Sikker opløsning af jern med saltsyre:En detaljeret trin-for-trin guide
Af John Brennan, Opdateret 24. marts 2022
Jern er notorisk modstandsdygtigt over for vand, men det reagerer kraftigt med saltsyre (HCl). Reaktionen frigiver brændbar brintgas og giver opløseligt jern(II)chlorid, hvilket gør det til en klassisk demonstration af reaktionskinetik. På grund af de involverede farer – ætsende syre, brintgas og potentielle stænk – bør dette eksperiment udføres i et stinkskab med fuldt personligt beskyttelsesudstyr.
Trin 1 – Forbered dit sikkerhedsudstyr
Inden du begynder, skal du tage sikkerhedsbriller, nitrilhandsker, en laboratoriefrakke og lukkede sko på. Sikring af en tætsiddende pasform på dine øjne og hænder beskytter mod utilsigtede stænk.
Trin 2 – Konfigurer reaktionsbeholderen
Placer et enkelt jernsøm (kort nok til at sidde i bunden af et 250 ml bægerglas) i bægeret. Denne orientering gør det muligt for neglen at være helt nedsænket, hvilket sikrer ensartet kontakt med syren.
Trin 3 – Anbring apparatet i et stinkskab
Flyt bægeret, en kalibreret målecylinder og en flaske 1M HCl ind i stinkskabet. Kontroller, at emhættens udsugningsventilator kører korrekt; konsulter producentens instruktioner, hvis det er nødvendigt.
Trin 4 – Mål og tilsæt syren
Brug målecylinderen til at måle 100 ml 1M HCl. Hæld syren forsigtigt over jernsømmet. Observer den kraftige opbrusning, når der frigives brintgas.
Ting påkrævet
- Sikkerhedsbriller
- Nitrilhandsker
- Laboratoriefrakke
- Jernsøm
- Bægerglas (250 ml)
- 1M saltsyre
- Stinkskab
- Klassificeret cylinder (250 ml)
TL;DR
Saltsyre opløser jern og producerer brintgas og jern(II)chlorid. Mere koncentrerede opløsninger fremskynder reaktionen, men øger risikoen. Brug altid et stinkskab og PPE.
Advarsel
Fordi reaktionen udsender brændbart brint, og syren er stærkt ætsende, skal du kun udføre forsøget i et stinkskab. Undgå kontakt med hud eller øjne, og brug beskyttelsestøj hele vejen igennem.
 Varme artikler
Varme artikler
-
 Hvordan ioniske og kovalente forbindelser opfører sig i vand:dissociation vs. opløselighedAf Claire Gillespie | Opdateret 30. august 2022 TL;DR Når et ionisk salt opløses, spaltes det til frie ioner og bliver til en elektrolyt, der leder elektricitet. De fleste kovalente molekyler forbliv
Hvordan ioniske og kovalente forbindelser opfører sig i vand:dissociation vs. opløselighedAf Claire Gillespie | Opdateret 30. august 2022 TL;DR Når et ionisk salt opløses, spaltes det til frie ioner og bliver til en elektrolyt, der leder elektricitet. De fleste kovalente molekyler forbliv -
 At gøre alkohol til nøgleingredienser til ny medicinForskere har fundet en måde at omdanne alkohol til aminosyrer, afgørende komponenter i mange lægemidler. Kredit:Unsplash Kemikere har fundet en måde at omdanne alkohol til aminosyrer, livets bygge
At gøre alkohol til nøgleingredienser til ny medicinForskere har fundet en måde at omdanne alkohol til aminosyrer, afgørende komponenter i mange lægemidler. Kredit:Unsplash Kemikere har fundet en måde at omdanne alkohol til aminosyrer, livets bygge -
 Vibration kun i én retningDet nydesignede materiale. Den transmitterer vibrationer fra venstre mod højre, men ikke fra højre mod venstre. Kredit:UvA/Brandenbourger et al. Elektroniske komponenter såsom transistorer transmi
Vibration kun i én retningDet nydesignede materiale. Den transmitterer vibrationer fra venstre mod højre, men ikke fra højre mod venstre. Kredit:UvA/Brandenbourger et al. Elektroniske komponenter såsom transistorer transmi -
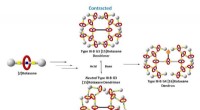 Gennembrud i makromolekylære maskiner til aktivt kontrolleret levering af kræftmedicinMolekylære maskiners kemiske struktur. Kredit:HKBU Forskere fra Hong Kong Baptist University (HKBU) demonstrerede design og syntese af et smart globulært makromolekylært maskinkøretøj til aktivt k
Gennembrud i makromolekylære maskiner til aktivt kontrolleret levering af kræftmedicinMolekylære maskiners kemiske struktur. Kredit:HKBU Forskere fra Hong Kong Baptist University (HKBU) demonstrerede design og syntese af et smart globulært makromolekylært maskinkøretøj til aktivt k
- Endnu en dag på kontoret:Sherpa fuldfører rekord 23. Everest-bestigning
- Hvordan er smeltepunktet af siliciumdioxid lavere end diamant?
- Forbliver eller fjernes volumenet af et stof, når varmen tilsættes varme?
- Nogle stoffer fordamper lettere end andre, fordi de kondenserer på kolde overflader kan opvarmes at…
- Sådan konverteres Kilopascals til Joules
- Graduation Typer på Steel Linjaler


