Natriumkarbonat vs. Calciumkarbonat:Nøgleforskelle, produktion og daglig brug
Af Chris Deziel – Opdateret 24. marts 2022
Carbonationen (CO₃²⁻) kombineres med alkalimetaller og danner en række essentielle industrielle og husholdningsforbindelser. To af de mest brugte er natriumcarbonat (Na₂CO₃) - almindeligvis kendt som soda eller vaskesoda - og calciumcarbonat (CaCO₃), den mineralske form af calcit, der udgør kridt, kalksten og marmor.
Fra naturen til fabrikken:Sådan produceres natriumkarbonat
Mens calciumcarbonat findes naturligt i marmor, kridt, kalksten og endda skallerne af marine organismer, ekstraheres natriumcarbonat traditionelt fra tronamalm eller mineralet nahcolit (en naturligt forekommende form for natriumbicarbonat). Opvarmning af disse råmaterialer frigiver det ønskede salt.
Derudover kan industrien fremstille "syntetisk soda" ved at reagere calciumcarbonat med natriumchlorid:
CaCO3 + 2NaCl → CaCl2 + Na₂CO3
Denne syv-trins proces giver et produkt med høj renhed, der bruges i en række applikationer.
pH og opløselighed:To grundlæggende forbindelser, forskellig adfærd
Begge salte er basiske. I en 10 mM vandig opløsning udviser natriumcarbonat en pH på 10,97, mens calciumcarbonatets pH er 9,91. Natriumcarbonat er moderat opløseligt i vand og er en almindelig pH-justerer i svømmebassiner og industrielle processer.
Calciumcarbonats opløselighed er lav i rent vand, men stiger ved tilstedeværelse af opløst CO₂, som danner kulsyre. Denne egenskab ligger til grund for den naturlige erosion af kalkstensformationer af regnvand.
Industrielle og husholdningsapplikationer
Glasproducenter er afhængige af natriumcarbonat som flusmiddel; det sænker smeltepunktet for silica, hvilket gør glasproduktionen mere energieffektiv. I boliger bruges soda til blødgøring af vand, sanitet i poolen og farvefiksering.
Calciumcarbonats primære anvendelser er i byggeriet:det tjener som et mørteladditiv, en nøglekomponent i gipsvæg og fugemasse og et pigment i maling. Gartnere anvender det som en jord pH-balancer, og det findes også i mange antacida og calciumtilskud.
Vigtige takeaways
- Na₂CO₃ (soda) er mere opløseligt og har en højere pH end CaCO₃ (calcit).
- CaCO₃ er rigeligt og udgør omkring 4 % af jordskorpen.
- Begge er hvide pulvere med udbredt industriel og husholdningsbrug.
- Syntetisk soda kan fremstilles ved at reagere CaCO₃ med NaCl.
Sidste artikelSådan bestemmes en sfæres vægt ved hjælp af volumen og tæthed
Næste artikelFem grundlæggende egenskaber ved gasser
 Varme artikler
Varme artikler
-
 Praktiske videnskabsaktiviteter for at udforske frosne væskerAf Lily Mae, opdateret 30. august 2022 Når en væske bliver til et fast stof, ændres dens egenskaber på måder, der fascinerer både videnskabsmænd og studerende. Disse omhyggeligt designede eksperiment
Praktiske videnskabsaktiviteter for at udforske frosne væskerAf Lily Mae, opdateret 30. august 2022 Når en væske bliver til et fast stof, ændres dens egenskaber på måder, der fascinerer både videnskabsmænd og studerende. Disse omhyggeligt designede eksperiment -
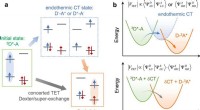 Endoterm ladningsoverførsel medierer overfladeafstandsafhængig trilling energimigrationen skematisk afbildning af de indledende og endelige tilstande og mellemliggende endoterme CT -tilstande. 3D* -A og D-3A* er de indledende og sidste tilstande, henholdsvis, der henviser til, at D −- A
Endoterm ladningsoverførsel medierer overfladeafstandsafhængig trilling energimigrationen skematisk afbildning af de indledende og endelige tilstande og mellemliggende endoterme CT -tilstande. 3D* -A og D-3A* er de indledende og sidste tilstande, henholdsvis, der henviser til, at D −- A -
 Nye biokompatible hybridhydrogeler med imponerende mekaniske egenskaberFigur 1:SAXS -opsætningen på I22. Kredit:Diamond lyskilde For første gang er der skabt en familie af hydrogeler, med unikke egenskaber, der gør det muligt at bruge dem i biologiske applikationer.
Nye biokompatible hybridhydrogeler med imponerende mekaniske egenskaberFigur 1:SAXS -opsætningen på I22. Kredit:Diamond lyskilde For første gang er der skabt en familie af hydrogeler, med unikke egenskaber, der gør det muligt at bruge dem i biologiske applikationer. -
 Forurenende stoffer, patogener kunne slå sig sammen for at gøre os sygeKredit:CC0 Public Domain Mange mennesker ser forurenende stoffer og patogener som separate årsager til sygdom. Imidlertid, nyere forskning viser, at de to kan interagere, ændre, hvordan mennesker
Forurenende stoffer, patogener kunne slå sig sammen for at gøre os sygeKredit:CC0 Public Domain Mange mennesker ser forurenende stoffer og patogener som separate årsager til sygdom. Imidlertid, nyere forskning viser, at de to kan interagere, ændre, hvordan mennesker
- Den scene, hvor stjerner producerer energi gennem fusionen af brint til helium?
- Lavfrekvente havlyde ringer klart i store højder
- Mekanisme dechifreret:Hvordan organiske syrer dannes i atmosfæren
- Hvilke stoffer er cellulær cytoplasma primært sammensat af?
- Brug af lignin til at erstatte fossile materialer
- Når forårsager varme eller overførsel af energi fra et objekt til et andet?


