Mestring af pH-beregninger for stærke syrer:En trin-for-trin guide
Af Kevin Beck Opdateret 24. marts 2022
Jupiterimages/Pixland/Getty Images
Hvis du vil have succes i kemi, skal du forstå syrer og baser. Du bør ikke kun forstå, hvad disse forbindelser er, og hvordan de opfører sig i opløsning, men også være i stand til at udføre simple beregninger af pH og forstå, hvorfor stærke syres adfærd forenkler beregninger, der involverer disse stoffer.
Til at begynde med bør du vide, at i kemi, koncentration udtrykkes ofte i mol pr. volumenenhed, normalt liter (mol/L) snarere end i masseenheder pr. liter. Antallet af gram i 1 mol af et stof kan bestemmes ud fra molmasserne eller molekylvægtene af dets bestanddele, som er tilgængeligt i det periodiske system af grundstoffer.
- Mængden mol/L skrives normalt som det enkelte symbol M.
Hvad er syrer og baser?
Hvad er syrer og baser?
En syre er en forbindelse, der donerer en proton i vandig opløsning. Denne proton er nogle gange repræsenteret i ligninger som en selvstændig proton (H+) eller som en hydroniumion (en proton plus vand:H3O+). Den anden komponent i den opløste syre kaldes konjugatbasen. Den generelle formel for dissociation af en syre er HA → H+ + A–, hvor A– er den konjugerede base.
Baser tjener på den anden side som syrernes dobbeltgangere:De accepterer let protoner, hvilket svarer til at donere hydroxidioner (OH-) i vandig opløsning. Resten af en dissocieret base kaldes konjugatsyren , og er ofte en metalkation såsom Na+.
Hvad er pH i kemi?
Hvad er pH i kemi?
pH-værdien eller "brintstyrken" er en værdi generelt (men ikke matematisk) begrænset til det numeriske område fra 0 til 14,0. Opløsninger, der er sure, har en lav pH, neutrale opløsninger (såsom rent vand) har en pH på 7, og basiske opløsninger har højere pH-værdier.
Matematisk er pH kun det negative af logaritmen til basen 10 af koncentrationen af H+ (eller H3O+) ioner:pH =–log10[H+]. Så længe du har en lommeregner og er forsigtig med dine potenser på 10, er disse beregninger ligetil.
Styrken af syrer og baser
Styrken af syrer og baser
En stærk syre er en, der let giver afkald på sine protoner, og gør det selv når den omgivende pH er lav, hvilket betyder, at der allerede er mange protoner, der flyder rundt. Svage syrer afgiver ikke deres protoner så let, og bliver kun dissocieret i et meningsfuldt omfang, når pH er tættere på neutral. Stærke baser afgiver ligeledes let hydroxidioner selv i opløsninger med høj pH.
Styrken af syre og baser kan tildeles en værdi:pK a, eller syredissociationskonstanten , den pH-værdi, ved hvilken halvdelen af en syre har doneret sine protoner, mens den anden halvdel forbliver i den konjugerede tilstand. (Baser har, du gættede det, pKb-værdier.) Stærkere syrer har således lavere pKa-værdier.
Beregning af pH af saltsyre
Beregning af pH af saltsyre
Saltsyre, eller HCl, er en velkendt og almindelig stærk syre. Saltsyreanvendelser omfatter kemilaboratorier på højskoler og gymnasier rundt omkring i verden samt en lang række industrielle og fremstillingsapplikationer.
Eksempel:Beregn pH-værdien af en 0,100 M opløsning af HCl.
Da HCl er en stærk syre, ioniserer den fuldstændigt, og pH-værdien af HCl i opløsning kan findes ud fra koncentrationen (molariteten) af H+-ionerne, per definition lig med 0,100 M. (Syrens konjugatbase, som er chloridionen Cl–, ville også have en koncentration på 0,100 M.)
pH er således –log(0,100) =1,000 .
Det er klart, at højere molaritetsværdier vil give lavere pH-værdier og omvendt for HCl (eller enhver syre).
Online pH-beregner for stærke syrer
Online pH-beregner for stærke syrer
Hvis du ikke har lyst til at slæbe en lommeregner frem og ønsker at lære om den kemiske opførsel af nogle flere stærke syrer, så se siden i Ressourcerne.
 Varme artikler
Varme artikler
-
 Biologer opdager carotenoidoverførsel mellem to proteinerCover art til denne artikel minder om coveret til albummet The Dark Side of the Moon af Pink Floyd. Det viser, hvor rødt, lilla, orange og violette proteiner kan fås fra et farveløst protein og en typ
Biologer opdager carotenoidoverførsel mellem to proteinerCover art til denne artikel minder om coveret til albummet The Dark Side of the Moon af Pink Floyd. Det viser, hvor rødt, lilla, orange og violette proteiner kan fås fra et farveløst protein og en typ -
 Hele forestillingen, intet af balladen:nitrilhydrogenering udført rigtigtFigur 1:Katalytisk hydrogenering af nitriler til primære aminer. Kredit:Osaka University Behovet for at være opmærksomme forbrugere er ved at blive en prioritet for en stadigt voksende del af samf
Hele forestillingen, intet af balladen:nitrilhydrogenering udført rigtigtFigur 1:Katalytisk hydrogenering af nitriler til primære aminer. Kredit:Osaka University Behovet for at være opmærksomme forbrugere er ved at blive en prioritet for en stadigt voksende del af samf -
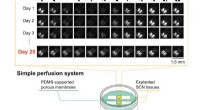 Hjernevæv holdt i live i ugevis på en kunstig membranNederst:mikroenhedsopsætningen med eksplanteret suprachiasmatic nucleus (SCN) væv. Øverst:rytmisk døgnaktivitet var stadig tydelig efter 25 dage, som angivet ved bioluminescensbilleddannelse. Kredit:R
Hjernevæv holdt i live i ugevis på en kunstig membranNederst:mikroenhedsopsætningen med eksplanteret suprachiasmatic nucleus (SCN) væv. Øverst:rytmisk døgnaktivitet var stadig tydelig efter 25 dage, som angivet ved bioluminescensbilleddannelse. Kredit:R -
 Er emballage af gurkemeje film fremtiden for supermarkedernes hylder?Kredit:pinkomelet/123rf Forskere i Malaysia har udviklet en biopolymerfilm, der indeholder gurkemejeolie, der stopper væksten af en almindelig madsvamp og nedbrydes godt i jorden. Filmen kan giv
Er emballage af gurkemeje film fremtiden for supermarkedernes hylder?Kredit:pinkomelet/123rf Forskere i Malaysia har udviklet en biopolymerfilm, der indeholder gurkemejeolie, der stopper væksten af en almindelig madsvamp og nedbrydes godt i jorden. Filmen kan giv
- I Californien, tørken og yuck -faktoren
- Hvilken krop af vand har de mest olieaflejringer omkring det?
- Hvordan en enorm skov af uddøde træer udløste transformation af livet på Jorden
- Undersøgelse tyder på, at palmeoliedyrkning i Afrika yderligere kan bringe primater i fare
- Hvad er levende anatomi?
- Forskere introducerer programmerbare materialer til at hjælpe med at helbrede brækkede knogler


