Hvordan sukker sænker vands frysepunkt - en videnskabelig forklaring
Af Claire Gillespie, Opdateret 24. marts 2022
Allexxandar/iStock/GettyImages
Frysepunkt
Den temperatur, hvor en væske bliver til et fast stof, kaldes dets frysepunkt. For rent vand er dette 32°F (0°C). Ved denne temperatur er vandmolekyler og ismolekyler i dynamisk ligevægt - vand fryser, mens is smelter med samme hastighed.
Vandmolekyler
Et vandmolekyle er sammensat af et oxygenatom og to hydrogenatomer. Når temperaturen falder, falder den kinetiske energi af disse molekyler, hvilket giver dem mulighed for at danne hydrogenbindinger, der skaber et krystallinsk gitter kendt som is.
Tilføjelse af sukker til vand
Når sukker (saccharose) opløses i vand, bliver sukkermolekylerne spredt i opløsningsmidlet. De forstyrrer vandmolekylernes evne til at tilpasse sig den regulære hydrogenbundne struktur, der kræves til isdannelse. Sukkermolekylerne optager plads, der ellers ville være tilgængelig for vandet, og "overfylder" effektivt opløsningen.
Frysepunktsdepression
Fordi sukkerpartikler forbliver i væskefasen, sænker de opløsningens kemiske potentiale. Dette fænomen, kendt som frysepunktsdepression, betyder, at blandingen skal afkøles til under 32°F (0°C), før der kan dannes is. Omfanget af depressionen afhænger af koncentrationen af sukker:en højere mængde opløst sukker fører til et større fald i frysetemperaturen.
I praksis er det derfor, sukkerholdige drikkevarer og desserter forbliver flydende ved temperaturer, der ville fryse almindeligt vand. Princippet anvendes i vid udstrækning til konservering af fødevarer og til at skabe isbaser, der bevarer en ønskværdig tekstur.
 Varme artikler
Varme artikler
-
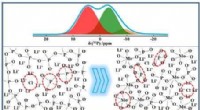 Forskere undersøger strukturen af fosfat-ionisk ledende glas ved hjælp af solid-state NMRStrukturudviklingen af hurtige ionledende glas karakteriseret ved brug af solid-state NMR-teknologier. Kredit:SIOM Glasagtige hurtige ioniske ledere kan bruges som faste elektrolytter, katode ma
Forskere undersøger strukturen af fosfat-ionisk ledende glas ved hjælp af solid-state NMRStrukturudviklingen af hurtige ionledende glas karakteriseret ved brug af solid-state NMR-teknologier. Kredit:SIOM Glasagtige hurtige ioniske ledere kan bruges som faste elektrolytter, katode ma -
 En ny måde at levere lysfølsomme lægemidler til at bekæmpe problemet med antibiotikaresistensKredit:CC0 Public Domain Queens University-forsker P. Andrew Evans har afsløret en ny proces til at levere antibiotika ved hjælp af pollen til at beskytte dem. Antibiotika er kraftfuld medicin, d
En ny måde at levere lysfølsomme lægemidler til at bekæmpe problemet med antibiotikaresistensKredit:CC0 Public Domain Queens University-forsker P. Andrew Evans har afsløret en ny proces til at levere antibiotika ved hjælp af pollen til at beskytte dem. Antibiotika er kraftfuld medicin, d -
 Forskerhold skruer op for varmen på 3D-printblækEn 3D-printet blomst demonstrerer kvaliteterne af en multifunktionel printgel, der reagerer på fugt. Kredit:Ke Functional Research Group i Dartmouth. En proces, der bruger varme til at ændre arran
Forskerhold skruer op for varmen på 3D-printblækEn 3D-printet blomst demonstrerer kvaliteterne af en multifunktionel printgel, der reagerer på fugt. Kredit:Ke Functional Research Group i Dartmouth. En proces, der bruger varme til at ændre arran -
 Forskere laver syntetiske polymerer inde i levende cellerKredit:CC0 Public Domain Et team af forskere ved University of Edinburgh har vist, at det er muligt at skabe syntetiske polymerer inde i levende celler. I deres papir offentliggjort i tidsskriftet
Forskere laver syntetiske polymerer inde i levende cellerKredit:CC0 Public Domain Et team af forskere ved University of Edinburgh har vist, at det er muligt at skabe syntetiske polymerer inde i levende celler. I deres papir offentliggjort i tidsskriftet
- Hvor i alverden kunne du se alle konstellationer stige og sætte?
- Hvilken effekt har en katalysator?
- Forældre får lynkursus i fjernundervisningsdilemmaer
- Hvordan er springet år relateret til den tid, det tager Jorden, drejer sig om solen?
- En af de værste stadiontragedier i historien:En ekspert forklarer, hvad der førte til fodboldstamp…
- Navn på kongeriget Mange cellede organismer, der bevæger sig rundt og spiser?


