Beregning af ioniske tiltrækningskræfter ved hjælp af Coulombs lov
Af Jack Brubaker
Opdateret 24. marts 2022
Når metaller og ikke-metaller danner forbindelser, donerer metalatomer elektroner til ikke-metalatomer. Metalatomerne bliver positivt ladede ioner, mens ikke-metalatomerne bliver negativt ladede ioner. Modsatte ladninger tiltrækker, et forhold kvantificeret af Coulombs lov:
F =k \frac{q_1 q_2}{d^2}Her F er tiltrækningskraften i Newton, q_1 og q_2 er de ioniske ladninger i coulombs, d er afstanden mellem ionernes kerner i meter, og k er Coulomb-konstanten (8,99 × 10 9 N·m²/C²).
Trin 1 – Identificer ioniske ladninger
Se en tabel med almindelige ioner for at bestemme ladningerne af de positive og negative arter i forbindelsen. Kemiske formler viser først kationen. For eksempel i calciumbromid (CaBr2 ), calcium er kationen med en ladning på +2, mens brom er anionen med en ladning på -1. Således q1 =2 og q2 =1 (i elementære ladningsenheder).
Trin 2 – Konverter gebyrer til Coulombs
Multiplicer hver ladning med den elementære ladning (1.602 × 10 –19 C). Calciumionen bærer 2 × 1.602 × 10 –19 =3.204 × 10 –19 C, mens bromidionen bærer 1 × 1.602 × 10 –19 =1.602 × 10 –19 C.
Trin 3 – Bestem interionisk afstand
Brug en tabel med ioniske radier til at finde størrelsen af ionerne. I faste stoffer indtager ioner positioner, der minimerer deres adskillelse, så afstanden er lig med summen af radierne. For Ca 2+ (≈1,00 Å) og Br – (≈1,96 Å), kerneseparationen er 1,00 + 1,96 =3,96 Å.
Trin 4 – Konverter afstand til meter
Konverter ångstrøm til meter ved at gange med 1 × 10 –10 . Således er 3,96 Å =3,96 × 10 –10 m.
Trin 5 – Beregn kraften
Indsæt værdierne i Coulombs ligning:
F =(8,99 × 10 9 ) × (3,204 × 10 –19 ) × (1.602 × 10 –19 ) ÷ (3,96 × 10 –10 ) 2Kvadre først afstanden:(3,96 × 10 –10 ) 2 =1,57 × 10 –19 m². Udførelse af multiplikation og division giver F ≈ 4,1 × 10 –9 N. Dette er størrelsen af tiltrækningskraften mellem calcium- og bromidionerne i krystalgitteret.
Nødvendige værktøjer
- Referencetabel over almindelige ioner
- Referencetabel over ioniske radier
- Videnskabelig lommeregner i stand til videnskabelig notation
TL;DR (for lang; læste ikke)
Videnskabelig notation som 1,9 × 10 –19 betyder "et punkt ni gange ti til den negative nittende potens." Indtast disse værdier direkte i en videnskabelig lommeregner ved hjælp af EE-knappen.
 Varme artikler
Varme artikler
-
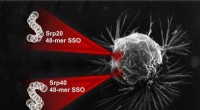 Biokemikere rapporterer en måde at stoppe kræftcellernes udødelighed med oligonukleotiderKredit:Natalia Deryugina RUDN biokemikere fandt en måde at reducere aktiviteten af telomerase (enzymet udødelighed af celler) 10 gange. Opdagelsen kan føre til nye antitumorlægemidler og give en
Biokemikere rapporterer en måde at stoppe kræftcellernes udødelighed med oligonukleotiderKredit:Natalia Deryugina RUDN biokemikere fandt en måde at reducere aktiviteten af telomerase (enzymet udødelighed af celler) 10 gange. Opdagelsen kan føre til nye antitumorlægemidler og give en -
 Forskere afslører hovedårsagen til resistens i faste elektrolytterAt se det usynlige:Et elektronhologram af en korngrænse i en let doteret fast elektrolytprøve, hvorfra elektrisk potentiale ved korngrænsen kan genvindes. Kredit:Argonne National Laboratory Redukt
Forskere afslører hovedårsagen til resistens i faste elektrolytterAt se det usynlige:Et elektronhologram af en korngrænse i en let doteret fast elektrolytprøve, hvorfra elektrisk potentiale ved korngrænsen kan genvindes. Kredit:Argonne National Laboratory Redukt -
 Forskere formår at forbedre metalliske brillerMetallisk glasprøve. Kredit:NUST MISIS Forskere ved National University of Science and Technology MISIS (NUST MISIS) har formået at udvikle en unik metode til behandling af store glas i metal. Ifø
Forskere formår at forbedre metalliske brillerMetallisk glasprøve. Kredit:NUST MISIS Forskere ved National University of Science and Technology MISIS (NUST MISIS) har formået at udvikle en unik metode til behandling af store glas i metal. Ifø -
 Forskere identificerer den indre funktion af cellulære calciumpumperKredit:Aarhus Universitet Förster resonance energy transfer (FRET) kombinerer laserlys og ultrafølsomme kameraer, der sender signaler ind i et individuelt molekyle. Dette signal spredes til det andet
Forskere identificerer den indre funktion af cellulære calciumpumperKredit:Aarhus Universitet Förster resonance energy transfer (FRET) kombinerer laserlys og ultrafølsomme kameraer, der sender signaler ind i et individuelt molekyle. Dette signal spredes til det andet
- Hvordan ligner lysene på stadion stjerner i himlen?
- Nanodiamond bliver til kontrollerbar lyskilde
- Forskere skitserer spilteoretisk tilgang til bedre at forstå genetik
- Undersøgelse inspicerer ung åben klynge NGC 3293
- Hvad er en måde at kortlægge jord på flad overflade på?
- Beregning af toppunktet for en parabel:En trin-for-trin guide


