4 nøglefaktorer, der påvirker diffusionshastigheden
Af Riti Gupta Opdateret 24. marts 2022
Achisatha Khamsuwan/iStock/GettyImages
Diffusion opstår på grund af den tilfældige bevægelse af partikler. Det sker normalt på grund af en koncentrationsgradient, hvilket betyder, at molekyler bevæger sig fra et område med høj koncentration til et område med lavere koncentration.
Et eksempel er vist på billedet ovenfor. Når farvestof tilsættes opløsningen, diffunderer det over tid. Først ser du streger af blåt bevæge sig gennem opløsningen, indtil hele opløsningen til sidst bliver blå, fordi koncentrationen af farvestof er den samme overalt. På dette tidspunkt, selvom farvestofmolekylerne stadig bevæger sig rundt, vil du ikke være i stand til at opfatte det, da det blå farvestof har spredt sig og farvet hele væskevolumenet.
Diffusion er således en passiv proces (hvilket betyder, at det ikke kræver tilførsel af energi). Et stof bevæger sig fra et område med høj koncentration til et område med lavere koncentration. Denne bevægelse fortsætter, indtil koncentrationen af stoffet udjævnes. Når koncentrationen er udjævnet, bevæger stoffet sig stadig, men vil ikke længere have en koncentrationsgradient. Denne tilstand kaldes dynamisk ligevægt .
Hvilke faktorer påvirker diffusionshastigheden?
Hvilke faktorer påvirker diffusionshastigheden?
Molekyler bevæger sig konstant rundt på grund af mængden af termisk energi, de har. Denne bevægelse er påvirket af størrelsen af partiklen og det miljø, partiklen befinder sig i. Partikler vil altid bevæge sig rundt i et medium, men den samlede diffusionshastighed kan påvirkes af mange faktorer.
Koncentration :Diffusion af molekyler er helt afhængig af at bevæge sig fra et område med højere koncentration til et område med lavere koncentration. Diffusion sker med andre ord ned ad koncentrationsgradienten af det pågældende molekyle. Hvis forskellen i koncentration er højere, så vil molekylerne gå hurtigere ned i koncentrationsgradienten. Hvis der ikke er så stor forskel i koncentrationen, vil molekylerne ikke bevæge sig så hurtigt, og diffusionshastigheden vil falde.
**Temperatur:** Partikler bevæger sig på grund af den kinetiske energi, der er forbundet med dem. Når temperaturen stiger, øges den kinetiske energi, der er forbundet med hver partikel. Som et resultat vil partikler bevæge sig hurtigere. Hvis de kan bevæge sig hurtigere, så kan de også diffundere hurtigere. Omvendt, når den kinetiske energi forbundet med molekylerne falder, falder deres bevægelse også. Som et resultat vil diffusionshastigheden være langsommere.
**Partikelmasse:** Tyngre partikler vil bevæge sig langsommere og vil derfor have en langsommere diffusionshastighed. Mindre partikler vil på den anden side diffundere hurtigere, fordi de kan bevæge sig hurtigere. Som det er nøglen med alle faktorer, der påvirker diffusionen, er bevægelse af partiklen altafgørende for at afgøre, om diffusionen bremses eller fremskyndes.
**Opløsningsmiddelegenskaber:** Viskositet og densitet påvirker diffusionen i høj grad. Hvis mediet, som en given partikel skal diffundere igennem, er meget tæt eller tyktflydende, så vil partiklen have sværere ved at diffundere igennem det. Så diffusionshastigheden vil være lavere. Hvis mediet er mindre tæt eller mindre viskøst, vil partiklerne være i stand til at bevæge sig hurtigere og vil diffundere hurtigere.
Alle de faktorer, der påvirker diffusionen, kan have en kombineret effekt. For eksempel kan en lille ion diffundere hurtigere gennem en viskøs opløsning end et stort sukkermolekyle. Ionen har en mindre størrelse og er dermed i stand til at bevæge sig hurtigere. Det store sukkermolekyle bevæger sig langsommere på grund af dets størrelse. Viskositeten af opløsningen påvirker begge dele, men vil forstærke den langsomme diffusion, som det større molekyle gennemgår.
TL;DR (for lang; læste ikke)
Enhver faktor, der fremskynder bevægelse af partikler gennem et medium, vil resultere i en hurtigere diffusionshastighed.
 Varme artikler
Varme artikler
-
 Mindre salt, mere protein:Adressering af mejeriprocesser miljømæssigt, bæredygtighedsspørgsmålEn grafisk fremstilling af den nye valleforarbejdningsmetode. Kredit:Xiao Su Forskere siger, at det høje saltindhold i valle - den vandige del af mælk, der efterlades efter ostfremstilling - er me
Mindre salt, mere protein:Adressering af mejeriprocesser miljømæssigt, bæredygtighedsspørgsmålEn grafisk fremstilling af den nye valleforarbejdningsmetode. Kredit:Xiao Su Forskere siger, at det høje saltindhold i valle - den vandige del af mælk, der efterlades efter ostfremstilling - er me -
 Team udvikler nye måder at skabe og levere medicin til en bred vifte af immunmedicinske neuropatierKredit:Liverpool School of Tropical Medicine Forskere ved LSTM ser på nye måder at skabe og levere medicin til en bred vifte af immunmedicinerede neuropatier, ved at udvikle nye syntetiske version
Team udvikler nye måder at skabe og levere medicin til en bred vifte af immunmedicinske neuropatierKredit:Liverpool School of Tropical Medicine Forskere ved LSTM ser på nye måder at skabe og levere medicin til en bred vifte af immunmedicinerede neuropatier, ved at udvikle nye syntetiske version -
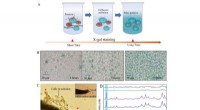 Ny SERS-strategi udviklet til beta-galactosidase aktivitetsanalyseIn-situ SERS udlæsningsstrategi for individuelle celler. (A) Skematisk strategi for at forbedre pålideligheden ved at forkorte farvningstider. (B) X-gal farvning assay for celler. (C og D) In-situ SER
Ny SERS-strategi udviklet til beta-galactosidase aktivitetsanalyseIn-situ SERS udlæsningsstrategi for individuelle celler. (A) Skematisk strategi for at forbedre pålideligheden ved at forkorte farvningstider. (B) X-gal farvning assay for celler. (C og D) In-situ SER -
 Halvledergennembrud kan være en game-changer for organiske solcellerEn organisk solcelletest inde i Randall Lab på Central Campus Ann Arbor, MI. Forskere fra University of Michigan har fundet en måde at lokke elektroner til at rejse meget længere, end man tidligere tr
Halvledergennembrud kan være en game-changer for organiske solcellerEn organisk solcelletest inde i Randall Lab på Central Campus Ann Arbor, MI. Forskere fra University of Michigan har fundet en måde at lokke elektroner til at rejse meget længere, end man tidligere tr
- Er Titans klitter lavet af kometstøv?
- Et objekt rejser i et lige linjeplads, ingen kræfter handler på det baserede dette bevis Hvad vil …
- Yangtze-flodens observationssystem for at forbedre prognosen for østasiatisk regnsæson
- På det kemiske laboratorium, hvorfor bruger forskere en mørtel og en pestle?
- Udløste en udenjordisk påvirkning udryddelsen af istidsdyr?
- Afbalanceret kemisk ligning:Reaktion af aluminium og saltsyre


