Sådan beregnes sublimationsvarmen - en trin-for-trin guide
Af Jack Brubaker, opdateret 24. marts 2022
Sublimering er den direkte overgang af et fast stof til en gas, der går uden om væskefasen. Fordi processen absorberer energi, er den klassificeret som endoterm. Forskere kvantificerer den nødvendige energi og udtrykker den som sublimationsvarmen, typisk i joule pr. gram (J/g) eller joule pr. mol (J/mol).
Trin 1 – Indstil kalorimeteret
Følg producentens instruktioner for at samle kalorimeteret. Sørg for, at beholderen er forseglet, termometeret er korrekt placeret, og prøven er klar til introduktion.
Trin 2 – Mål temperaturfaldet
Registrer den indledende temperatur af vandet og den endelige temperatur efter sublimeringshændelsen. Beregn temperaturændringen (ΔT) ved at trække den endelige værdi fra den oprindelige. For eksempel, hvis vandet afkøles fra 55,0°C til 22,6°C, ΔT =22,6°C – 55,0°C =–32,4°C.
Trin 3 – Beregn den varme, der går tabt af vandet
Brug formlen Q =m × c × ΔT, hvor m er massen af vandet (1mL ≈ 1g) og c er vandets specifikke varmekapacitet (4.184Jg⁻¹°C⁻¹). Med 200mL vand, m =200g, ΔT =–32,4°C, er varmetabet Q =200g × 4,184Jg⁻¹°C⁻¹ × (–32,4°C) =–27.100 J. Det negative fortegn angiver varmetab; det sublimerende stof får lige meget varme.
Trin 4 – Bestem sublimationsvarmen
Divider størrelsen af den varme absorberet af det sublimerende materiale med dets masse. Hvis der blev brugt 47,5 g af stoffet, er sublimationsvarmen 27.100 J ÷ 47,5 g =571 Jg⁻¹.
Væsentligt udstyr
- Lommeregner
- Kalorimeter
- Prøve af stoffet, der skal sublimeres
 Varme artikler
Varme artikler
-
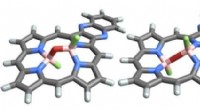 Opdagelse til at gruppere atomer påkalder PasteurForskernes molekyler ændrer form ved, at det centrale oxygenatom (vist med rødt) bøjer sig som et hængsel. De venstre og højre billeder viser, hvad formerne på disse molekyler er, når de er stabile. H
Opdagelse til at gruppere atomer påkalder PasteurForskernes molekyler ændrer form ved, at det centrale oxygenatom (vist med rødt) bøjer sig som et hængsel. De venstre og højre billeder viser, hvad formerne på disse molekyler er, når de er stabile. H -
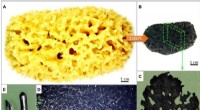 Ekstrem biomimetik - søgen efter naturlige kilder til materialeteknisk inspirationOversigt over transformationen af svampestilladser til en karboniseret 3D -struktur ved 1200 ° C. (A) Typisk cellulær og hierarkisk morfologi af Hippospongia communis demosponge organisk skelet efte
Ekstrem biomimetik - søgen efter naturlige kilder til materialeteknisk inspirationOversigt over transformationen af svampestilladser til en karboniseret 3D -struktur ved 1200 ° C. (A) Typisk cellulær og hierarkisk morfologi af Hippospongia communis demosponge organisk skelet efte -
 Retsmedicinsk kemiker opdager brug af marihuana baseret på svedtestUAlbany retsmedicinsk kemiker Jan Halámek med kandidatstuderende forsker Mindy Hair. Kredit:Scott Freedman Retsmedicinsk kemiker Jan Halámek beviser, at vores egen sved ikke kun fortæller, hvor fu
Retsmedicinsk kemiker opdager brug af marihuana baseret på svedtestUAlbany retsmedicinsk kemiker Jan Halámek med kandidatstuderende forsker Mindy Hair. Kredit:Scott Freedman Retsmedicinsk kemiker Jan Halámek beviser, at vores egen sved ikke kun fortæller, hvor fu -
 Hvordan pH-buffere stabiliserer surhed og alkalinitetAf Carrie Perles Opdateret 24. marts 2022 Introduktion En pH-buffer er en omhyggeligt afbalanceret opløsning, der modstår ændringer i surhedsgrad eller basicitet, når små mængder af en syre eller ba
Hvordan pH-buffere stabiliserer surhed og alkalinitetAf Carrie Perles Opdateret 24. marts 2022 Introduktion En pH-buffer er en omhyggeligt afbalanceret opløsning, der modstår ændringer i surhedsgrad eller basicitet, når små mængder af en syre eller ba
- Beregning af genotypeforhold med Punnett-kvadrater
- Fremtiden for plastik – genbruge det dårlige og opmuntre det gode
- Iron Pillar er bygget ved hjælp af hvilken klippe?
- Hvorfor kulstof er det eneste element med et relativt atomnummer, hvilket hele nummer?
- USA anklager Facebook for højteknologisk boligdiskrimination
- Platin-grafen brændselscellekatalysatorer viser overlegen stabilitet i forhold til bulk platin


