Konvertering af atmosfærer til mol gas:en praktisk guide
Chain45154/Getty Images
En hæveautomat (atmosfære) er en enhed for gastryk. Én atm svarer til standardatmosfærisk tryk ved havoverfladen:14,7psi, 101325Pa, 1,01325bar eller 1013,25mbar. Den ideelle gaslov giver dig mulighed for at forbinde en gass tryk inde i en beholder til antallet af mol, den indeholder, så længe temperatur og volumen forbliver konstant.
Ved standardtemperaturen og -trykket (STP) på 273K (0°C / 32°F) og 1atm optager et mol af en ideel gas 22,4 l. Dette forhold er grundlaget for at konvertere tryk målt i atmosfærer til mol gas.
Den ideelle gaslov
Den ideelle gaslov er udtrykt som:
PV=nRT
hvor P er tryk, V er volumen, n er antallet af mol, T er absolut temperatur i Kelvin, og R er den ideelle gaskonstant. Når trykket måles i atmosfærer, R =0,082057 Latmmol⁻1K⁻1. Hvis du foretrækker SI-enheder, R =8,3145 Jmol⁻¹K⁻¹ (≈8,3145m³Pamol⁻¹K⁻¹).
Denne ligning gælder for en ideel gas - en hvis molekyler er perfekt elastiske og ikke optager noget volumen. Selvom ingen rigtig gas opfylder disse kriterier nøjagtigt, er loven en god tilnærmelse for de fleste gasser under STP-forhold.
Relateret tryk til mol gas
Omarrangering af den ideelle gaslov giver to nyttige former:
P=(nRT)/V eller n=(PV)/(RT)
Hvis du holder temperatur og volumen konstant, er trykket og antallet af mol direkte proportionale:P=Cn og n=P/C , hvor C=RT/V .
For at beregne C , mål volumen i liter eller kubikmeter, og brug den tilsvarende værdi af R . Temperaturen skal altid udtrykkes i Kelvin; konverter fra Celsius ved at lægge 273,15 til eller fra Fahrenheit ved at trække 32 fra, gange med 5/9 og derefter lægge 273,15 sammen.
Eksempel
Overvej en 0,5-L pære fyldt med argon ved et tryk på 3,2 atm, når pæren er slukket og stuetemperaturen er 25°C. Hvor mange mol argon indeholder pæren?
Bestem først C ved hjælp af R=0,082Latmmol⁻¹K⁻¹ :
C=(RT)/V=(0,082×298,15)/0,5=48,9atmmol⁻¹
Beregn derefter molerne:
n=P/C=3,2/48,9≈0,065 mol
Referencer
- Kemi LibreTexts:Den ideelle gaslov
- ThoughtCo:Lær om STP i kemi
 Varme artikler
Varme artikler
-
 Nøjagtig længde- og breddemåling for omkredse og områderAf Kathryn Hatter Opdateret 30. august 2022 At måle dimensionerne af et rektangulært eller kvadratisk rum nøjagtigt er afgørende for at beregne omkreds og areal. Denne vejledning forklarer, hvordan d
Nøjagtig længde- og breddemåling for omkredse og områderAf Kathryn Hatter Opdateret 30. august 2022 At måle dimensionerne af et rektangulært eller kvadratisk rum nøjagtigt er afgørende for at beregne omkreds og areal. Denne vejledning forklarer, hvordan d -
 Mestring af forældrefunktioner:Kerneformerne i alle graferAf Usha Dadighat 31. juli 2023 kl. 15:24 EST Forældrefunktioner er de enkleste repræsentanter for hele familier af matematiske funktioner. De fanger den væsentlige geometri af en funktion uden tilfø
Mestring af forældrefunktioner:Kerneformerne i alle graferAf Usha Dadighat 31. juli 2023 kl. 15:24 EST Forældrefunktioner er de enkleste repræsentanter for hele familier af matematiske funktioner. De fanger den væsentlige geometri af en funktion uden tilfø -
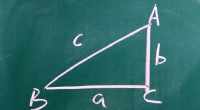 Sådan bestemmes den ukendte vinkel i enhver trekantZorabc/Shutterstock Trekantligninger er en fast bestanddel af geometri- og algebraforløb, og symbolet X bruges oftest til at betegne en ukendt vinkel. Ved at analysere markeringerne på trekanten og a
Sådan bestemmes den ukendte vinkel i enhver trekantZorabc/Shutterstock Trekantligninger er en fast bestanddel af geometri- og algebraforløb, og symbolet X bruges oftest til at betegne en ukendt vinkel. Ved at analysere markeringerne på trekanten og a -
 Beregning af procentvis afvigelse:En trin-for-trin guidemarekuliasz/Shutterstock Procentvis afvigelse kvantificerer, hvor langt individuelle datapunkter afviger fra gennemsnitsværdien af et datasæt. Det er en nøgleindikator for variabilitet og hjælper med
Beregning af procentvis afvigelse:En trin-for-trin guidemarekuliasz/Shutterstock Procentvis afvigelse kvantificerer, hvor langt individuelle datapunkter afviger fra gennemsnitsværdien af et datasæt. Det er en nøgleindikator for variabilitet og hjælper med
- Hvad er det nærmeste system til din sol?
- S. Koreas LG Group er på vej mod fjerde generation efterfølger
- Hvordan påvirker dets masse at ændre formen på et objekt?
- Hvad er reaktivitetsnummeret for jern?
- Hvilket molekyle har den største mængde potentiel energi i cellulær respiration?
- Hvad hedder rumfartøjet, som de første mænd på månen tog?


