Kræftforskere mener, at nanopartikler præcist kunne målrette mod tumorer, undgå bivirkninger
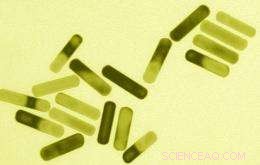
MIT forskere udviklede disse guld nanorods, der absorberer energi fra nær-infrarødt lys og udsender det som varme, ødelægge kræftceller. Billede:Sangeeta Bhatia Laboratory; MIT
I de sidste 40 år, forskere har lært meget om, hvordan celler bliver til kræft. Noget af den viden har oversat til nye behandlinger, men det meste af tiden er læger tvunget til at stole på standard kemoterapi og stråling, som kan gøre næsten lige så meget skade på patienterne, som de gør på tumorerne. Denne serie ser på målrettede behandlinger, der er i horisonten, og hvad der skal gøres for at gøre dem til virkelighed.
Doxorubicin, et lægemiddel, der almindeligvis anvendes til behandling af leukæmi og andre kræftformer, dræber tumorceller ved at beskadige deres DNA. Selvom stoffet er effektivt, det kan også være giftigt for hjerteceller. I 2005, FDA godkendte en ny type doxorubicin, kendt som Doxil. I denne nye formulering, stoffet er pakket ind i en fed belægning kaldet et liposom, som hæmmer dens evne til at trænge ind i hjerteceller (og andre raske celler).
Doxil, normalt ordineret til kræft i æggestokkene i det sene stadie, repræsenterer den første generation af kræftbehandlinger leveret af bittesmå partikler. Doxil-partikler er på størrelsesordenen milliontedele af en meter, men forskere arbejder nu på partikler i nanostørrelse, som måles i milliardtedele meter. Sådanne partikler kunne give læger mulighed for at give større doser kemoterapi og samtidig skåne sundt væv for farlige bivirkninger.
Flere nanopartikellægemidler er nu i kliniske forsøg, og mange flere bliver udviklet i forskningslaboratorier. Disse partikler rummer et stort potentiale til at forbedre ydeevnen af eksisterende kræftlægemidler, siger læge og ingeniør Sangeeta Bhatia, Wilson professor i sundhedsvidenskab og teknologi og elektroteknik og datalogi ved MIT. "Kemoterapi og stråling og kirurgi er, hvad vi har nu, men nanoteknologi dukker op som en tilgang, der komplementerer det eksisterende armamentarium af kliniske værktøjer for at have en betydelig indvirkning, ” siger hun.
Liposomer blev først opdaget for omkring 50 år siden, men for nylig, forskere har indset, at store syntetiske molekyler (polymerer) såsom polyethylenglycol (PEG) kan være ugiftige og ikke fremkalde et immunrespons. PEG, som består af en lang kæde af gentagne enheder kaldet ethere, kan fastgøres til nedbrydelige polymerer for at danne små, lægemiddelafgivende partikler. Disse partikler er bemærkelsesværdigt stabile og kan beskytte lægemidler mod kroppens eget immunsystem, som ellers kunne ødelægge dem, før de når deres destination. For omkring 15 år siden, videnskabsmænd ledet af MIT's institut professor Robert Langer opdagede, at PEG også egner sig til kemisk manipulation, giver videnskabsfolk mulighed for at skabe skræddersyede partikler til lægemiddellevering.
"Da nanovidenskaben begyndte at udvikle sig, og vi blev dygtige til at skabe vores egne nanopartikler, vi fandt måder til specifikt at designe nanopartikler, så de havde egenskaber, vi ønskede, siger Paula Hammond, Bayer-professoren i kemiteknik og medlem af David H. Koch Institute for Integrative Cancer Research ved MIT. For eksempel, forskere kan designe partikler til at udlede deres lægemiddellast, når de støder på sure lommer inde i en tumorcelle.
Forskere kan også målrette nanopartikler specifikt for at angribe tumorceller. Der er to måder at gøre det på - en passiv og en aktiv. I 1980'erne, videnskabsmænd indså, at blodkarrene omkring tumorer har små huller, op til 500 nanometer i diameter, som tillader små partikler at strømme fra blodbanen ind i væsken, der omgiver tumoren.
Mens den passive målretning får nanopartikler til det rigtige sted, partiklerne vaskes væk efter ca. 12 til 24 timer, siger Hammond. "Hvis du ønsker, at kemoterapien skal komme tættere på sit mål, så skal du gøre noget for at få kræftcellen til at optage den, ” siger hun.
Til det formål, hun og Bhatia arbejder på nye måder at aktivt målrette mod nanopartikler ved at dekorere dem med molekyler, der binder til proteiner, der findes i store mængder på tumorceller. For eksempel, de kan binde proteiner til folatreceptorer, som er placeret i høj tæthed på kræftceller, fordi cellerne har brug for store mængder folat for at producere nyt DNA, når de deler sig. Imidlertid, folatreceptorer findes også på raske celler, i mindre antal, så der er stadig en chance for uønskede bivirkninger.
For at hjælpe med at overvinde den forhindring, en samarbejdspartner for Bhatia, Erkki Ruoslahti ved University of California i Santa Barbara, har været banebrydende for en ny måde at screene biblioteker af proteiner på for at identificere dem, der udelukkende vil binde til tumorceller. Denne tilgang har vist hundredvis af nye kandidater, siger Bhatia, som også er medlem af Koch Institute og Howard Hughes Medical Institute.
Mange anvendelser for nanopartikler
Andre nanoteknologiske tilgange til kræft drager fordel af nogle nanopartiklers unikke fysiske egenskaber. For eksempel, guld nanopartikler absorberer forskellige frekvenser af lys afhængigt af deres form. Stangformede partikler absorberer nær-infrarødt lys, som kan passere gennem huden. Sidste år, Bhatia og en af hendes elever, Geoffrey von Maltzahn, demonstrerede, at de kunne injicere guld nanorods i mus, og at sådanne nanorods ville akkumulere på tumorsteder. Når nanoroderne var i tumorerne, forskerne opvarmede dem med nær-infrarødt lys, hæve temperaturen til 70 grader C, varmt nok til at dræbe tumorcellerne uden at beskadige nærliggende sundt væv. Teknikken kan også bruges til at afbilde tumorceller.
En anden lovende applikation til nanopartikler er at levere RNA-interferens - bittesmå RNA-strenge, der kan blokere celler i at producere de proteiner, der kodes af kræftgener. Med udgangspunkt i den idé, Hammond arbejder nu på nanopartikler, der ville levere et en-to-slag, skiftende lag af RNA og kemoterapi.
Indtil nu, Doxil er et af kun to liposomale kræftlægemidler, der nu er godkendt i USA, men andre lægemidler leveret af nanopartikler er nu i kliniske forsøg. Kliniske forsøg forventes at begynde snart for nanopartikler konstrueret af Langer, medlem af Koch Instituttet, Harvard Medical School lektor Omid Farokhzad og andre. Disse nanopartikler vil levere kemoterapilægemidlet docetaxel til prostatakræftpatienter. I dyreforsøg, partiklerne viste en 20-fold stigning i koncentrationen på tumorstedet med minimale bivirkninger.
Som med enhver ny type medicinsk behandling, forskere vurderer også sikkerhedsrisici. I de seneste år, et nyt felt inden for nanotoksikologi er opstået for at undersøge eventuelle risici, nanopartikler kan udgøre for mennesker. På nanoskala, materialer får ofte nye træk - f.eks. nanopartikler har et meget højere overflade-til-volumen-forhold end større partikler, hvilket er vigtigt, fordi det meste af deres aktivitet foregår på overfladen, siger Vladimir Torchilin, direktør for Center for Farmaceutisk Bioteknologi og Nanomedicin ved Northeastern University.
Imidlertid, han siger, kliniske forsøg bør afsløre, om en given nanopartikel er sikker eller farlig, ligesom de gør for traditionelle stoffer. "Hidtil har det er ret svært at sige, på forhånd, det kan være farligt på grund af det, det eller det, " siger Torchilin, der udvikler nanopartikler til kræftbehandling.
I 2007 en FDA-taskforce om nanoteknologi anbefalede, at agenturet danner nye retningslinjer for at bestemme, hvordan man regulerer nanoteknologiske produkter. I mellemtiden, kliniske forsøg, der involverer nanopartikler, forløber ligesom ethvert klinisk forsøg med lægemidler. PEG, som er hovedkomponenten i mange lægemiddelleverende nanopartikler, tilhører FDA-kategorien af stoffer "generelt anerkendt som sikre."
Hammond er optimistisk om, at nanoteknologi vil ende med at hjælpe kræftpatienter, muligvis inden for de næste tre til fem år. "Jeg tror, det giver alt for mange fordele til, at vi kan trække os væk fra det, ” siger hun.
Denne historie er genudgivet med tilladelse fra MIT News (web.mit.edu/newsoffice/), et populært websted, der dækker nyheder om MIT-forskning, innovation og undervisning.
 Varme artikler
Varme artikler
-
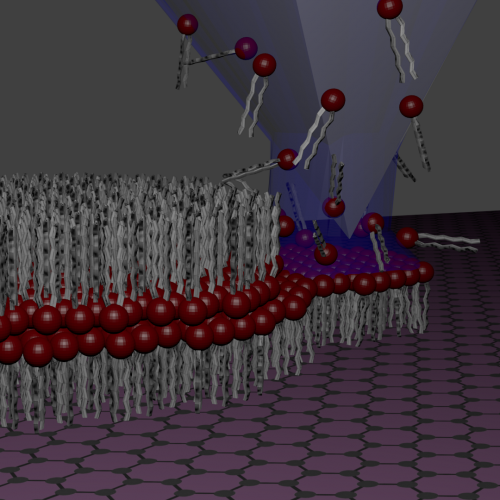 Direkte skrivning af kunstige cellemembraner på grafenLipidmembraner kan direkte skrives på grafen med en dip-pen i nanoskala. Kredit:University of Manchester Grafen dukker op som en alsidig ny overflade til at samle modelcellemembraner, der efterlig
Direkte skrivning af kunstige cellemembraner på grafenLipidmembraner kan direkte skrives på grafen med en dip-pen i nanoskala. Kredit:University of Manchester Grafen dukker op som en alsidig ny overflade til at samle modelcellemembraner, der efterlig -
 Caltech -forskere designer et nyt nanomesh -materialeØverst:Et scanningselektronmikroskopbillede viser gitteret af små huller i nanomesh -materialet. Nederst:På denne tegning, hver kugle repræsenterer et siliciumatom i nanomesh. De farverige bånd viser
Caltech -forskere designer et nyt nanomesh -materialeØverst:Et scanningselektronmikroskopbillede viser gitteret af små huller i nanomesh -materialet. Nederst:På denne tegning, hver kugle repræsenterer et siliciumatom i nanomesh. De farverige bånd viser -
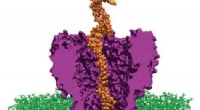 Whole-Genome-sekventering simuleret på supercomputereForskere simulerer DNA, der interagerer med et konstrueret protein. Systemet kan bremse DNA -tråde, der bevæger sig gennem porerne nok til at aflæse en patients individuelle genom. (Billede udlånt af
Whole-Genome-sekventering simuleret på supercomputereForskere simulerer DNA, der interagerer med et konstrueret protein. Systemet kan bremse DNA -tråde, der bevæger sig gennem porerne nok til at aflæse en patients individuelle genom. (Billede udlånt af -
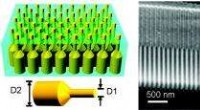 Et nyt twist for nanopillar lyssamlereTil venstre et skema af en germanium nanopillar array indlejret i en aluminiumoxidfoliemembran; til højre er tværsnits-SEM-billeder af en blank aluminiumoxidmembran med porer med dobbelt diameter; ind
Et nyt twist for nanopillar lyssamlereTil venstre et skema af en germanium nanopillar array indlejret i en aluminiumoxidfoliemembran; til højre er tværsnits-SEM-billeder af en blank aluminiumoxidmembran med porer med dobbelt diameter; ind
- Drivhusgasser krymper stratosfæren
- Forskere anvender en ny tilgang til at samle peptoider på en fast overflade
- Ny teknik, hvor lægemidler får bakterier til at lyse, kan hjælpe med at bekæmpe antibiotikaresis…
- Hånddesinfektionsmiddel er fantastisk til at bevare insekt -DNA
- Batteri og hukommelsesenhed i ét:Fremtidige nanoelektroniske informationslagringsenheder er også s…
- Mangroveskovundersøgelser har takeaways til kystsamfund


