Forskere konstruerer RNA-nanopartikler til sikkert at levere langvarig terapi til celler

Peixuan Guo, Ph.d., Dane og Mary Louise Miller begav stol i biomedicinsk teknik med studerende i sit laboratorium på Vontz Center for Molecular Studies. Kredit:University of Cincinnati
(PhysOrg.com) - Nanoteknologiforskere har i årevis vidst, at RNA, fætter til DNA, er et lovende værktøj til nanoterapi, hvor terapeutiske midler kan leveres inde i kroppen via nanopartikler. Men vanskelighederne ved at producere langvarig, terapeutisk RNA, der forbliver stabilt og ikke-toksisk, mens det kommer ind i målrettede celler, har udgjort udfordringer for deres fremskridt.
I to nye publikationer i tidsskriftet Molekylær terapi , University of Cincinnati (UC) professor i biomedicinsk teknik Peixuan Guo, Ph.d., beskriver vellykkede metoder til fremstilling af store RNA -nanopartikler og testning af deres sikkerhed ved levering af terapi til målrettede celler.
Artiklerne, på forhånd online udgivelse, repræsentere "to meget vigtige milepæle i RNA -nanoterapi, "siger Guo.
"Et problem i RNA -terapi er kravet til generering af relativt store mængder RNA, ”Siger han. "I denne forskning, vi fokuserede på at løse det mest udfordrende problem med industriel produktion af store RNA-molekyler ved en topartet tilgang, at finde ud af, at pRNA kan samles fra to stykker mindre RNA -moduler. ”
Guo, Dane og Mary Louise Miller begavet formand for biomedicinsk teknik, fungerer som direktør for National Cancer Institute (NCI) Alliance for Nanotechnology in Cancer Platform Partnership Program ved UC. Han har fokuseret sin forskning på RNA i årtier, banebrydende for dens anvendelse som en alsidig byggesten til nanoteknologi, eller til konstruktion af funktionelle systemer i molekylær skala. I 1987, han opdagede en emballage -RNA (pRNA) i bakteriofagen phi29 -virus, som kan geare en motor til at pakke DNA ind i viralproteinskallen. I 1998, hans laboratorium opdagede, at pRNA kan samle sig selv eller blive konstrueret til nanopartikler til gear af motoren.
I sin seneste forskning, Guo og kolleger beskriver flere tilgange til konstruktionen af et funktionelt 117-base pRNA-molekyle indeholdende lille interfererende RNA (siRNA). siRNA har allerede vist sig at være et effektivt værktøj til at dæmpe gener i celler, men tidligere forsøg har produceret kemisk modificeret siRNA, der kun varer 15-45 minutter i kroppen og ofte fremkalder uønskede immunresponser.
"De pRNA -partikler, vi konstruerede til at rumme siRNA, har en halveringstid på mellem fem og 10 timer i dyremodeller, er giftfri og producerer ingen immunrespons, ”Siger Guo. "Den tidoblet forøgelse af cirkulationstiden i kroppen er vigtig for lægemiddeludvikling og baner vejen mod kliniske forsøg med RNA -nanopartikler som terapeutiske lægemidler."
Guo siger, at størrelsen af det konstruerede pRNA -molekyle er afgørende for effektiv levering af terapeutiske midler til syge væv.
"RNA -nanopartikler skal være inden for området 15 til 50 nanometer, ”Siger han, "stor nok til at blive tilbageholdt af kroppen og ikke tilfældigt komme ind i celler, forårsager toksicitet, men lille nok til at komme ind i de målrettede celler ved hjælp af celleoverflademodtagelser.
I avisen, "Samling af terapeutiske pRNA-siRNA-nanopartikler ved hjælp af topartsmetode, ”Guo og hans kolleger brugte to syntetiske RNA-fragmenter til at skabe det 117-baserede pRNA, som var i stand til yderligere at samle sig med andre pRNA -molekyler og fungere i bakteriofag phi29 viral motor til at pakke DNA.
"Den todelt tilgang til pRNA-syntese overvandt udfordringer med størrelsesbegrænsninger i kemisk syntese af RNA-nanopartikler, ”Skrev Guo. "De resulterende nanopartikler var kompetente til at levere og frigive terapeutika til celler og dæmpe generne i dem. Evnen til kemisk at syntetisere disse nanopartikler muliggør yderligere kemisk modifikation af RNA for stabilitet og specifik målretning."
Den anden publikation, "Farmakologisk karakterisering af kemisk syntetiseret monomer phi29 pRNA -nanopartikler til systemisk levering, ”Bygger på den forskning, demonstrerer, at modificerede tredimensionelle pRNA-nanopartikler let blev fremstillet ved hjælp af todelt tilgang. De modificerede nanopartikler var resistente over for almindelige enzymer, der kan angribe og nedbryde RNA og forblev kemisk og metabolisk stabile.
Desuden, når den leveres til målceller i en dyremodel, nanopartiklerne var ugiftige og fremkaldte ikke et immunrespons, gør nanopartiklerne i stand til at binde til kræftceller in vivo.
Tidligere undersøgelser har indkapslet terapeutisk siRNA i en polymercoating eller liposom til levering til celler.
"Så vidt vi ved, dette er de første nøgne RNA -nanopartikler, der er blevet fuldstændigt undersøgt farmakologisk in vivo og vist sig at være sikre, samt levere sig selv til tumorvæv ved en specifik målretningsmekanisme, ”Siger han. "Det tyder på, at pRNA -nanopartiklerne uden belægning har alle de foretrukne farmakologiske egenskaber til at tjene som en effektiv nanodeliveringsplatform til brede medicinske anvendelser."
 Varme artikler
Varme artikler
-
 Fleksibel, semi-transparente ultratynde solcellerDette er et mikroskopfotografi af WSe2-prøver, tilsluttet elektroder. Kredit:TU Wien Der er for nylig blevet forsket meget på grafen - kulstofflager, bestående af kun et lag atomer. Det viser sig,
Fleksibel, semi-transparente ultratynde solcellerDette er et mikroskopfotografi af WSe2-prøver, tilsluttet elektroder. Kredit:TU Wien Der er for nylig blevet forsket meget på grafen - kulstofflager, bestående af kun et lag atomer. Det viser sig, -
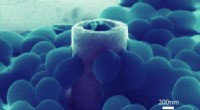 Se først på, hvordan individuelle Staphylococcus-celler klæber til nanostrukturer, kan føre til …Dette scanningselektronmikroskopibillede afslører, hvordan Staphylococcus Aureus-celler fysisk interagerer med en nanostruktur. En bakteriecelle (blå) er indlejret i den hule nanopillers hul, og flere
Se først på, hvordan individuelle Staphylococcus-celler klæber til nanostrukturer, kan føre til …Dette scanningselektronmikroskopibillede afslører, hvordan Staphylococcus Aureus-celler fysisk interagerer med en nanostruktur. En bakteriecelle (blå) er indlejret i den hule nanopillers hul, og flere -
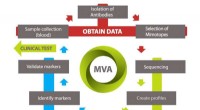 Risikovurdering på nanoskala -niveau:Et nærmere kig på mimotopvariationsanalysenKredit:Protobios, www.protobios.com Siden januar 2018 udvikler EU -projektet PANBioRA et modulopbygget system til en omfattende risikovurdering af biomaterialer. Instrumentet vil kunne sammenligne
Risikovurdering på nanoskala -niveau:Et nærmere kig på mimotopvariationsanalysenKredit:Protobios, www.protobios.com Siden januar 2018 udvikler EU -projektet PANBioRA et modulopbygget system til en omfattende risikovurdering af biomaterialer. Instrumentet vil kunne sammenligne -
 I solceller, justering af de mindste dele giver et stort spring i effektivitetElektrisk ingeniør Vladimir Mitin og hans kolleger har øget solcellernes elektriske effekt betydeligt ved at indlejre ladede kvanteprikker i dem. (PhysOrg.com) -- Ved at justere de mindste dele, e
I solceller, justering af de mindste dele giver et stort spring i effektivitetElektrisk ingeniør Vladimir Mitin og hans kolleger har øget solcellernes elektriske effekt betydeligt ved at indlejre ladede kvanteprikker i dem. (PhysOrg.com) -- Ved at justere de mindste dele, e
- Marriotts sikkerhedsbrud afslørede data på op til 500 millioner gæster (Opdatering)
- Polymer afledt af materiale i rejeskaller kunne levere anti-cancermedicin til tumorsteder
- Undersøiske havgræsbede slår forurenet havvand tilbage
- Sådan beregnes procentandel mellem to tal
- Kvindefodbold vokser muligvis i popularitet, men spillet kæmper stadig for overlevelse
- Fugleinformation til børn


