Nanovidenskaber:Alle systemer går på biofabrikken
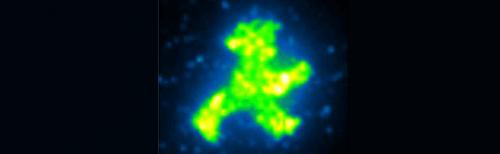
For at samle nye biomolekylære maskiner, individuelle proteinmolekyler skal installeres på deres arbejdssted med nanometerpræcision. Ludwig Maximilian University forskere har nu fundet en måde at gøre netop det på. Grønt lys på proteinsamling.
Den finpudrede spids af atomkraftmikroskopet (AFM) gør det muligt for en at opfange enkelte biomolekyler og deponere dem andre steder med nanometernøjagtighed. Teknikken kaldes Single-Molecule Cut &Paste (SMC &P), og blev udviklet af forskningsgruppen ledet af LMU -fysikeren professor Hermann Gaub. I sin oprindelige form, det var kun gældende for DNA -molekyler. Imidlertid, de molekylære maskiner, der er ansvarlige for mange af de biokemiske processer i celler, består af proteiner, og den kontrollerede samling af sådanne enheder er et af nanoteknologiens hovedmål. En praktisk metode til at gøre det ville ikke kun give ny indsigt i hvordan levende celler fungerer, men ville også give en måde at udvikle sig på, konstruere og bruge designer nanomaskiner.
I et stort skridt mod dette mål, LMU -teamet har ændret metoden, så de kan tage proteiner fra et opbevaringssted og placere dem på definerede steder inden for et konstruktionsområde med nanometerpræcision. "I flydende medium ved stuetemperatur, "vejrforholdene" i nanoskalaen kan sammenlignes med dem i en orkan, "siger Mathias Strackharn, første forfatter til den nye undersøgelse. Derfor, molekylerne, der manipuleres, skal fastgøres fast til spidsen af AFM og holdes sikkert på plads i byggeområdet.
Trafiksignaler beviser effektiviteten
De kræfter, der binder proteinerne under transport og samling, skal også være svage nok til ikke at forårsage skade, og skal kontrolleres tæt. For at nå disse to mål, forskerne brugte en kombination af antistoffer, DNA-bindende "zink-finger" proteiner, og DNA -ankre. "Vi demonstrerede metodens gennemførlighed ved at bringe hundredvis af fluorescerende GFP -molekyler sammen for at danne en lille grøn mand, ligesom lyskrydsfiguren, der signalerer til fodgængere at krydse vejen, men kun nogle mikrometer høje, ”Forklarer Strackharn.
Med denne teknik, funktionelle aspekter ved komplekse proteinmaskiner - såsom hvordan kombinationer af forskellige enzymer interagerer, og hvor tæt de skal være for at udføre koblede reaktioner - kan testes direkte. Et yderligere mål er at udvikle kunstige multimolekylære forsamlinger modelleret efter naturlige "cellulosomer", som kunne bruges til at omdanne plantebiomasse til biobrændstoffer. Strackharn påpeger konsekvenserne:"Hvis vi effektivt kan efterligne disse 'enzymatiske samlebånd' ved at bringe individuelle proteiner sammen, vi kunne måske yde et væsentligt bidrag til udnyttelsen af bæredygtige energikilder. "
 Varme artikler
Varme artikler
-
 Hvordan plantevirus kan bruges til at afværge skadedyr og holde planter sundeNicole Steinmetz, UC San Diego professor i nanoteknik, holder en forstørret model af Tobacco mild green mosaic virus. Hun undersøger, hvordan plantevirussen kan bruges til målrettet levering af pestic
Hvordan plantevirus kan bruges til at afværge skadedyr og holde planter sundeNicole Steinmetz, UC San Diego professor i nanoteknik, holder en forstørret model af Tobacco mild green mosaic virus. Hun undersøger, hvordan plantevirussen kan bruges til målrettet levering af pestic -
 Billede:Ny spektroskopi ved hjælp af afvigelserNår livet giver dig citroner, lav limonade. På Oak Ridge National Laboratory og Uppsala University, forskere har gjort den videnskabelige ækvivalent ved at bruge, frem for at fjerne, fejl forbundet me
Billede:Ny spektroskopi ved hjælp af afvigelserNår livet giver dig citroner, lav limonade. På Oak Ridge National Laboratory og Uppsala University, forskere har gjort den videnskabelige ækvivalent ved at bruge, frem for at fjerne, fejl forbundet me -
 Nano -gennembrud øger datasikkerheden(Phys.org)-Det voksende e-sikkerhedsproblem løses gennem nanoteknologi på Swinburne University of Technology. Gennembrudsforskning i fællesskab afsluttet af forskerne professor Min Gu og Dr. Xiangpin
Nano -gennembrud øger datasikkerheden(Phys.org)-Det voksende e-sikkerhedsproblem løses gennem nanoteknologi på Swinburne University of Technology. Gennembrudsforskning i fællesskab afsluttet af forskerne professor Min Gu og Dr. Xiangpin -
 Kvanteprikker viste sig at reducere fibriller i Parkinsons musemodellerTEM-billeder af præformede α-syn-fibriller på forskellige tidspunkter (6 og 12 h, 1, 3 og 7 dage) i fravær (øverst) og tilstedeværelse (nederst) af GQDer. Kredit: Natur nanoteknologi (2018). DOI:10.1
Kvanteprikker viste sig at reducere fibriller i Parkinsons musemodellerTEM-billeder af præformede α-syn-fibriller på forskellige tidspunkter (6 og 12 h, 1, 3 og 7 dage) i fravær (øverst) og tilstedeværelse (nederst) af GQDer. Kredit: Natur nanoteknologi (2018). DOI:10.1
- Rabies trick kunne hjælpe med at behandle Parkinsons sygdom
- Emner med sjov biologi-præsentation
- Sjælden byzantinsk mosaik afsløret i Jerusalems gamle bydel
- Nordøstlige guvernører er langsomme til at omfavne regional klimapagt
- Ambidextrous robotter kunne dramatisk fremskynde e-handel
- Advarselsskilte på en Blizzard


