Nanosilicon splitter hurtigt vand uden lys, varme, eller elektricitet
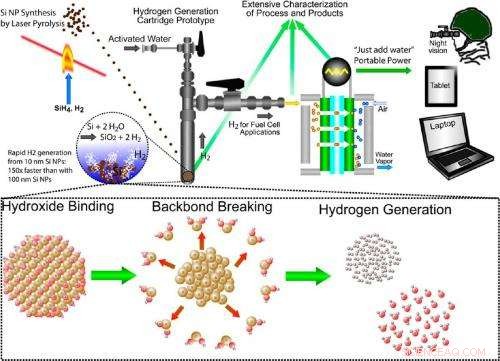
Illustration af den tværfaglige tilgang til fremstilling af brint gennem siliciumoxidation. Fremgangsmåden indebærer syntetisering af siliciumnanopartikler, silicium-vand-reaktionen, der genererer hydrogen efter behov og brug af brint i en brændselscelle til bærbar strøm. Kredit:Folarin Erogbogbo, et al. © 2013 American Chemical Society
(Phys.org) - Selvom forskere ved, at når silicium blandes med vand, hydrogen dannes ved oxidation, ingen forventede, hvor hurtigt silicium -nanopartikler kan udføre denne opgave. Som en ny undersøgelse har afsløret, 10-nm silicium nanopartikler kan generere brint 150 gange hurtigere end 100-nm silicium nanopartikler, og 1, 000 gange hurtigere end bulk silicium. Opdagelsen kan bane vejen mod hurtige "bare tilføj vand" brintgenereringsteknologier til bærbare enheder uden behov for lys, varme, eller elektricitet.
Forskerne, Folarin Erogbogbo ved University of Buffalo og medforfattere, har udgivet deres papir om brug af nanosilicium til at generere brint i en nylig udgave af Nano bogstaver .
Hvis der nogensinde skal bruges brint til at levere energi til store kommercielle anvendelser, et af kravene er at finde en hurtig, billig måde at producere brint på. En af de mest almindelige brintproduktionsteknikker er at splitte vand i hydrogen og ilt. Der er flere måder at dele vand på, f.eks. med en elektrisk strøm (elektrolyse), varme, sollys, eller et stof, der kemisk reagerer med vand. Sådanne stoffer omfatter aluminium, zink, og silicium.
Som forskerne forklarede, oxidation af silicium-vand-reaktioner har hidtil været langsomme og ukonkurrerende med andre vandspaltningsteknikker. Imidlertid, silicium har nogle teoretiske fordele, såsom at være rigelig, være let at transportere, og har en høj energitæthed. Yderligere, ved oxidation med vand, silicium kan teoretisk frigive to mol hydrogen pr. mol silicium, eller 14% af sin egen masse i brint.
Af disse grunde, forskerne besluttede at se nærmere på silicium, specifikt silicium nanopartikler, som ikke tidligere er blevet undersøgt for hydrogenproduktion. Fordi silicium nanopartikler har et større overfladeareal end større partikler eller bulk silicium, det forventes, at nanopartiklerne kan generere brint hurtigere end de større stykker silicium.
Men de forbedringer, forskerne opdagede med siliciumnanopartikler, overgik langt deres forventninger. Reaktionen af 10 nm siliciumpartikler med vand producerede i alt 2,58 mol hydrogen pr. Mol silicium (endda overstiger teoretiske forventninger), tager 5 sekunder at producere 1 mmol hydrogen. Sammenlignet med, reaktionen med 100 nm siliciumpartikler producerede i alt 1,25 mol hydrogen pr. mol silicium, tager 811 sekunder at producere hver mmol hydrogen. For bulk silicium, den samlede produktion var kun 1,03 mol hydrogen pr. mol silicium, tager hele 12,5 timer at producere hver mmol brint. For en sats sammenligning, 10-nm silicium genererede brint 150 gange hurtigere end 100-nm silicium og 1, 000 gange hurtigere end bulk silicium.
"Jeg tror, at den største betydning af dette arbejde er demonstrationen af, at silicium kan reagere med vand hurtigt nok til at være praktisk praktisk til on-demand brintproduktion, "medforfatter Mark Swihart, Professor i kemisk og biologisk teknik ved University of Buffalo, fortalt Phys.org . "Dette resultat var både uventet og af potentiel praktisk betydning. Selvom jeg ikke tror, at oxidation af siliciumnanopartikler snart vil blive en gennemførlig metode til storstilet brintproduktion, denne proces kan være ganske interessant for bærbare applikationer i mindre skala, hvor der er vand tilgængeligt. "

En sammenligning af hydrogengenereringshastigheder for forskellige former for silicium. Maksimumshastigheder er i venstre kolonne med billeder af prøverne på dem. Gennemsnitspriser er i den højre kolonne. Den røde linje angiver den maksimalt rapporterede hastighed for hydrogen, der genereres fra aluminium. Kredit:Folarin Erogbogbo, et al. © 2013 American Chemical Society
Ud over at producere brint hurtigere end større siliciumstykker, 10-nm silicium producerer også brint betydeligt hurtigere end aluminium og zink nanopartikler. Som Swihart forklarede, forklaringen på denne ulighed er forskellig for de to materialer.
"Sammenlignet med aluminium, silicium reagerer hurtigere, fordi aluminium danner et tættere og mere robust oxid (Al 2 O 3 ) på dens overflade, som begrænser reaktionen, "sagde han." I nærvær af en base som KOH [kaliumhydroxid], silicium producerer for det meste opløselig kiselsyre (Si (OH) 4 ). Sammenlignet med zink, silicium er simpelthen mere reaktivt, især ved stuetemperatur. "
Selvom det større overfladeareal af 10-nm silicium sammenlignet med større siliciumstykker bidrager til dets hurtige brintproduktionshastighed, overfladeareal alene kan ikke stå for den enorme hastighedsstigning, som forskerne observerede. Overfladearealet på 10 nm silicium er 204 m 2 /g, omkring 6 gange større end overfladearealet på 100 nm silicium, som er 32 m 2 /g.
For at forstå, hvad der forårsager den meget større stigning i brintproduktionshastigheden, forskerne gennemførte eksperimenter under silicium -ætsningsprocessen. De fandt ud af, at for partiklerne på 10 nm, ætsning involverer fjernelse af et lige antal gitterplaner i hver retning (isotrop ætsning). I modsætning, for 100 nm partikler og mikropartikler, ulige antal gitterplaner fjernes i hver retning (anisotrop ætsning).
Forskerne tilskriver denne ætsningsforskel til de forskellige geometrier af krystaller af forskellig størrelse. Som følge af denne forskel, de større partikler antager ikke-sfæriske former, der udsætter mindre reaktive overflader i forhold til de mindre partikler, som forbliver næsten sfæriske, udsætte alle krystalfacetter for reaktion. Større partikler udvikler også tykkere lag af oxiderede siliciumbiprodukter, gennem hvilke vand skal diffundere. Begge disse faktorer begrænser reaktionshastigheden på større partikler.
For at bekræfte, at 10-nm silicium-vand-reaktionen genererer hydrogen uden biprodukter, der kan forstyrre applikationer, forskerne brugte det siliciumgenererede brint til at drive en brændselscelle. Brændselscellen fungerede meget godt, producerer mere strøm og spænding end den teoretiske mængde rent brint, hvilket skyldes, at 10-nm partiklerne genererede mere hydrogen end de teoretiske 14 vægtprocent.
Forskerne håber, at denne overraskende evne af siliciumnanopartikler til hurtigt at splitte vand og generere brint kan føre til udviklingen af en hydrogen-on-demand-teknologi, der kan gøre det muligt at anvende brændselsceller i bærbare enheder. Denne teknologi ville kræve en storstilet, energieffektiv metode til fremstilling af siliciumnanopartikler, men kunne have nogle fordele i forhold til andre brintgenereringsteknikker.
"Den vigtigste fordel ved siliciumoxidation til brintproduktion er dens enkelhed, "Sagde Swihart." Med denne tilgang, brint produceres hurtigt, ved stuetemperatur, og uden behov for nogen ekstern energikilde. Den energi, der er nødvendig til brintproduktion, lagres effektivt i silicium. Al den energiindgang, der kræves til fremstilling af silicium, kan leveres på et centralt sted, og silicium kan derefter bruges i bærbare applikationer.
"Den væsentligste ulempe ved siliciumoxidation er dens relative ineffektivitet. Den energitilførsel, der kræves for at skabe siliciumnanopartiklerne, er meget større end den energi, der er tilgængelig fra det brint, der endelig produceres. Til store applikationer, dette ville være et problem. Til bærbare applikationer, det er ikke. For eksempel, omkostningerne ved elektricitet leveret af et almindeligt husholdningsbatteri kan let være 10 til 100 gange højere end omkostningerne ved elektricitet fra et forsyningsselskab, men batterier spiller stadig en vigtig rolle i vores liv. "
I fremtiden, forskerne planlægger yderligere at øge hydrogenproduktionskapaciteten ved siliciumoxidation ved at eksperimentere med forskellige blandinger.
"En retning, vi forfølger i øjeblikket, er brugen af blandinger af siliciumnanopartikler med metalhydrider, som også reagerer med vand for at producere brint, "Sagde Swihart." Forbindelser som lithiumhydrid og natriumhydrid reagerer med vand for at producere den base (LiOH eller NaOH), der er nødvendig for at katalysere siliciumoxidationen. Imidlertid, de kan reagere for hurtigt med vand (eksplosivt) og er ikke stabile i luften. Blanding af dem med siliciumnanopartikler eller belægning med siliciumnanopartikler kan tjene til både at dæmpe deres reaktivitet og øge systemets brintgenereringskapacitet ved at erstatte den ekstra base (f.eks. KOH i det publicerede papir) med et materiale, der også genererer brint. "
Copyright 2013 Phys.org
Alle rettigheder forbeholdes. Dette materiale må ikke offentliggøres, udsende, omskrevet eller omfordelt helt eller delvist uden udtrykkelig skriftlig tilladelse fra Phys.org.
 Varme artikler
Varme artikler
-
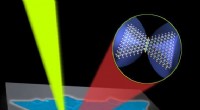 Metode registrerer defekter i 2-D materialer til fremtidig elektronik, sensorerEn laserstråle (gul) reflekterer et 2D -materiale (orange), der fremhæver en korngrænsefejl i atomgitteret. Kredit:MRI/Penn State For yderligere at skrumpe elektroniske enheder og reducere energif
Metode registrerer defekter i 2-D materialer til fremtidig elektronik, sensorerEn laserstråle (gul) reflekterer et 2D -materiale (orange), der fremhæver en korngrænsefejl i atomgitteret. Kredit:MRI/Penn State For yderligere at skrumpe elektroniske enheder og reducere energif -
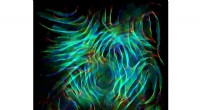 Topologien af uordnede 3-D grafener:Rosalind Franklins præ-DNA-problem løst udUordnet tredimensionelt grafennetværk (1,5 g/cc, en tæthed svarende til trækul). Vist som et overfladenet konstrueret af grafenringene med krumningen farvet rød til sadelformer, blå til skålformer. Kr
Topologien af uordnede 3-D grafener:Rosalind Franklins præ-DNA-problem løst udUordnet tredimensionelt grafennetværk (1,5 g/cc, en tæthed svarende til trækul). Vist som et overfladenet konstrueret af grafenringene med krumningen farvet rød til sadelformer, blå til skålformer. Kr -
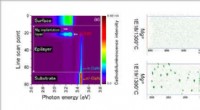 Nanoskala visualisering af fordelingen og optisk adfærd af dopingmiddel i GaNResultater af katodoluminescensanalyse anvendt på Mg-ionimplanteret GaN (venstre) og tredimensionel fordeling af Mg-atomer indført i GaN som visualiseret ved atomprobe-tomografi (højre). Kredit:NIMS
Nanoskala visualisering af fordelingen og optisk adfærd af dopingmiddel i GaNResultater af katodoluminescensanalyse anvendt på Mg-ionimplanteret GaN (venstre) og tredimensionel fordeling af Mg-atomer indført i GaN som visualiseret ved atomprobe-tomografi (højre). Kredit:NIMS -
 Forskere skaber forudsigelige mønstre ud fra uforudsigelige carbon nanorørEt omfarvet optisk billede opnået af MIT-forskere viser en hjerteformet carbon nanorørcelle. En version af billedet findes på forsiden af den 14. februar trykte udgave af Physical Chemistry Chemical
Forskere skaber forudsigelige mønstre ud fra uforudsigelige carbon nanorørEt omfarvet optisk billede opnået af MIT-forskere viser en hjerteformet carbon nanorørcelle. En version af billedet findes på forsiden af den 14. februar trykte udgave af Physical Chemistry Chemical
- Jeans lavet med børnearbejde? Folk vælger bevidst uvidenhed
- Forskere foreslår ny kilde til sjældne subatomære partikler
- Næste Mars-rover vil have 23 øjne
- Sådan kalibrerer du et opkaldstermometer
- Episk hårde baobabtræer, der dør i Afrika
- Beskedenhedens logik - hvorfor det kan betale sig at være ydmyg


