Hjernetumorceller penetreret af nedbrydelige nanopartikler, der bærer genetiske instruktioner
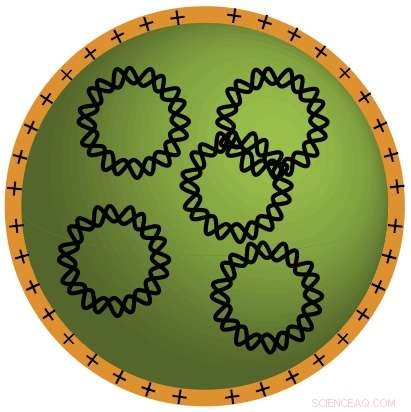
Biologisk nedbrydelige plastikmolekyler (orange) samles selv med DNA-molekyler (sammenflettet, sorte cirkler) for at danne små nanopartikler, der kan bære gener til kræftceller. Kredit:Stephany Tzeng
Arbejde sammen, Johns Hopkins biomedicinske ingeniører og neurokirurger rapporterer, at de har skabt små, bionedbrydelige "nanopartikler", der er i stand til at transportere DNA til hjernekræftceller hos mus.
Holdet siger, at resultaterne af deres proof-of-princip-eksperiment tyder på, at sådanne partikler fyldt med "dødsgener" en dag kan blive givet til hjernekræftpatienter under neurokirurgi for selektivt at dræbe eventuelle resterende tumorceller uden at beskadige normalt hjernevæv.
Et resumé af forskningsresultaterne udkom online den 26. april i tidsskriftet ACS Nano .
"I vores eksperimenter, vores nanopartikler leverede med succes et testgen til hjernekræftceller hos mus, hvor den så blev tændt, " siger Jordan Green, Ph.D., en assisterende professor i biomedicinsk teknik og neurokirurgi ved Johns Hopkins University School of Medicine. "Vi har nu beviser for, at disse små trojanske heste også vil være i stand til at bære gener, der selektivt inducerer død i kræftceller, mens de efterlader sunde celler sunde."
Green og hans kolleger fokuserede på glioblastomer, den mest dødelige og aggressive form for hjernekræft. Med standardbehandlinger af kirurgi, kemoterapi og stråling, den gennemsnitlige overlevelsestid er kun 14,6 måneder, og forbedring vil kun komme med evnen til at dræbe tumorceller, der er resistente over for standardbehandlinger, ifølge Alfredo Quiñones-Hinojosa, M.D., en professor i neurokirurgi ved Johns Hopkins University School of Medicine og medlem af forskerholdet.
Fordi naturen beskytter hjernen ved at gøre det vanskeligt at nå dens celler gennem blodet, indsatsen vendte sig mod brugen af partikler, der kunne bære tumorødelæggende DNA-instruktioner direkte til kræftceller under operationen.
De indledende eksperimenter gjorde brug af kræftceller, som Quiñones-Hinojosa og hans team fjernede fra villige patienter og voksede i laboratoriet, indtil de dannede små cellekugler, kaldet onkosfærer, sandsynligvis den mest modstandsdygtige over for kemoterapi og stråling, og i stand til at skabe nye tumorer.
Quiñones-Hinojosa arbejdede derefter sammen med Green for at finde et køretøj til gener, der ville forårsage død i onkosfærerne. Greens laboratorium har specialiseret sig i at producere bittesmå, runde partikler lavet af bionedbrydelig plast, hvis egenskaber kan optimeres til at udføre forskellige medicinske missioner. Ved at variere atomerne i plastikken, holdet kan lave partikler, der har forskellige størrelser, stabilitet og affinitet for vand eller olie. Til denne undersøgelse, Greens team skabte snesevis af forskellige typer partikler og testede deres evne til at bære og levere en testsekvens af DNA - specifikt et gen for et rødt eller grønt glødende protein - til onkosfærerne.
Ved at vurdere overlevelsen af de celler, der opsluger partiklerne, og måle niveauet af rødt eller grønt lys, som de udsender, forskerne fastslog, hvilken formulering af partikler der klarede sig bedst, testede derefter formuleringen i mus med human hjernekræft, der stammede fra deres patienter.
De injicerede partiklerne direkte i mus med en eksperimentel human hjernekræft, og ind i hjernen på raske mus til brug som sammenligning. Overraskende nok, raske celler producerede sjældent de glødende proteiner, selvom de DNA-bærende partikler trængte ind i tumorceller og ikke-tumorceller i lignende antal. "Det er præcis, hvad man gerne vil se, cancer specificitet, men vi forsker stadig i den mekanisme, der tillader dette at ske, " siger Green. "Vi håber, at vores fortsatte eksperimenter vil kaste lys over dette, så vi kan anvende det, vi lærer, til andre scenarier."
"Det er spændende at have fundet en måde at selektivt målrette genlevering til kræftceller, " siger Quiñones-Hinojosa. "Det er en metode, der er meget mere gennemførlig og sikrere for patienter end traditionel genterapi, som bruger modificerede vira til at udføre behandlingen."
Han tilføjer, at partiklerne kan frysetørres og opbevares i mindst to år uden at miste deres effektivitet. "Nanopartikler, der forbliver stabile i så lang tid, giver os mulighed for at fremstille formuleringer i god tid og i store partier, " siger Stephany Tzeng, Ph.D., medlem af Greens team. "Dette gør dem nemme at bruge konsekvent i eksperimenter og operationer; vi tilføjer vand til partiklerne, og de er gode til at gå."
I en relateret undersøgelse, offentliggjort online den 27. marts i samme tidsskrift, Greens gruppe viste også, at en anden partikelformulering effektivt kunne bære og levere såkaldte siRNA'er til hjernekræftceller. siRNA'er er meget små molekyler, der bærer genetisk information til celler, men i modsætning til DNA, der kan tænde gener, siRNA forstyrrer produktionen af bestemte proteiner og kan slå kræftgener fra.
Green forklarer, at siRNA'er skal indkapsles i partikler, der er forskellige fra dem, der bruges til at bære DNA, fordi siRNA'er er omkring 250 gange mindre end de DNA-molekyler, der normalt bruges til genterapi. "siRNA'er er også meget stivere end DNA, og de behøver ikke at gå ind i cellekernen, fordi de udfører deres arbejde uden for den, i cytoplasmaet, " han siger.
Et indledende bibliotek af 15 bionedbrydelige partikelformuleringer blev testet for deres evne til at bære siRNA'er ind i humane glioblastomceller, der var gensplejset til at lave grønt fluorescerende protein (GFP). SiRNA'erne tilføjet til partiklerne indeholdt GFP-koden, så vellykkede målrettede celler ville holde op med at lyse grønt.
Ved at justere partiklernes kemiske egenskaber, holdet var i stand til at finde en sammensætning, der reducerede GFP's glød i de menneskelige hjernekræftceller med 91 procent. For at teste partiklernes evne til at levere dødsinducerende siRNA'er, holdet fyldte partiklerne med en blanding af siRNA-koder designet til at forhindre vigtige proteiner i at blive fremstillet. De tilføjede derefter disse partikler til hjernekræftceller og til ikke-kræftfremkaldende hjerneceller, der voksede i laboratoriet.
Som i deres musestudie, siRNA var mere effektivt - i dette tilfælde til at forårsage celledød - i hjernekræftcellerne (op til 97 procent effektive) end i de ikke-kræftceller (0 til 27 procent, afhængig af nanopartikeltype).
Green understreger, at for nanopartikel-baserede genetiske terapier, der er sikre for patienter, det specifikke siRNA eller DNA, der leveres i en klinisk behandling, vil blive omhyggeligt udvalgt, således at selvom der var levering uden for målet til raske celler, det ville kun være skadeligt for kræftceller. Green er opmuntret af resultaterne indtil videre. "Ved at kombinere det, vi har lært i disse to undersøgelser, vi kan endda være i stand til at designe partikler, der kan levere DNA og siRNA på samme tid, " siger han. "Det ville give os mulighed for at finjustere den genetiske selvdestruktionskode, som vores partikler leverer, så kræftceller dør, og raske celler ikke gør det."
"Dr. Green og hans kolleger har taget vigtige skridt i udviklingen af polymere nanopartikler til DNA og siRNA levering, med lovende specificitet for tumorceller og øget stabilitet, " sagde Jessica Tucker, Ph.D., programdirektør for lægemiddel- og genleveringssystemer og enheder ved National Institute of Biomedical Imaging and Bioengineering, som gav delvis finansiering til disse undersøgelser. "Selvom der stadig er mange udfordringer, et sådant arbejde kan potentielt ændre behandlingsresultater for patienter med glioblastom og relaterede hjernetumorer, for hvilke nuværende behandlinger giver begrænsede fordele."
Sidste artikelForskere udvikler hårdere keramik til panservinduer
Næste artikelGrafen kun så stærk som det svageste led
 Varme artikler
Varme artikler
-
 Plantevira kan bruges til at forebygge og behandle menneskelige autoimmune sygdommeKredit:John Innes Center Forskere har taget positive skridt hen imod at bruge plantevirus-baserede partikler til behandling af humane autoimmune sygdomme som type 1 diabetes og leddegigt. Virus e
Plantevira kan bruges til at forebygge og behandle menneskelige autoimmune sygdommeKredit:John Innes Center Forskere har taget positive skridt hen imod at bruge plantevirus-baserede partikler til behandling af humane autoimmune sygdomme som type 1 diabetes og leddegigt. Virus e -
 Forskere skaber solceller med rekordstor energiydelseSolcelle med en sort siliciumoverfladebehandling Forskere ved Department of Electronic Engineering ved Universitat Politècnica de Catalunya (UPC) har opnået en rekordeffektiv effektivitet på 22 %
Forskere skaber solceller med rekordstor energiydelseSolcelle med en sort siliciumoverfladebehandling Forskere ved Department of Electronic Engineering ved Universitat Politècnica de Catalunya (UPC) har opnået en rekordeffektiv effektivitet på 22 % -
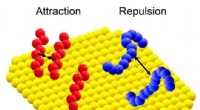 Lille molekyle spiller en stor rolle i at kontrollere nanopartiklerLigander kan tiltrække og hjælpe hinanden med at adsorbere på nogle overfladesteder, men kan ofte også forringe hinandens indsats. Kredit:Cornell University Ligander er meget som nanostørrelser, b
Lille molekyle spiller en stor rolle i at kontrollere nanopartiklerLigander kan tiltrække og hjælpe hinanden med at adsorbere på nogle overfladesteder, men kan ofte også forringe hinandens indsats. Kredit:Cornell University Ligander er meget som nanostørrelser, b -
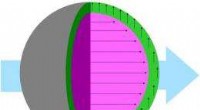 Forskere får ny kerneforståelse for nanopartiklerSkematisk af en sfærisk magnetitnanopartikel viser den uventede variation i magnetisk moment mellem partiklens indre og ydre, når den udsættes for et stærkt magnetfelt. Kernens øjeblik (sorte linjer i
Forskere får ny kerneforståelse for nanopartiklerSkematisk af en sfærisk magnetitnanopartikel viser den uventede variation i magnetisk moment mellem partiklens indre og ydre, når den udsættes for et stærkt magnetfelt. Kernens øjeblik (sorte linjer i
- Radar afslører detaljer om bjergkollaps efter Nordkoreas seneste atomprøvesprængning
- Når sælgere advokerer for sælgere og kunder
- Hvad er tre hovedelementer, der omfatter strukturen af organiske molekyler?
- Fordele og ulemper ved metoder til kvadratiske ligninger
- Kriminalteknisk puslespil revnet via flydende mekaniske principper
- Hvordan at slippe af med lortejobs og produktivitetsmålingen kan bekæmpe klimaændringer


