Nanocontainere til nanocargo:Levering af gener og proteiner til cellulær billeddannelse, genetisk medicin og kræftbehandling

Det T4 capsid-afledte specifikke eksogene DNA plus proteinpakning og eukaryot celleleveringsskema. (A) DNA, der koder for et 10-aminosyre N-terminalt CTS-peptid fusioneret til fagen P1 Cre tillader syntese af CTS-Cre og målretning af enzymet ind i det tidlige kerne-stillads af T4-procapsidet in vivo. Procapsid-samling og modningsspecifik viral protease stabiliserer procapsiden, fjerne det meste af stilladsets kerne som peptider, og fjern CTS-peptidet fra Cre. Mutationer i den virale terminase blokerer DNA-pakning og tillader et modent, men DNA-tomt stort Cre-holdigt procapsid at blive stærkt oprenset fra virusinficerede bakterier. (B) In vitro-pakning i det modne kapsid af plasmid-DNA indeholdende mCherry drevet af en CMV-promotor og to loxP-steder, der flankerer et SfiI-restriktionsenzymsted, der tillader den linearisering, der kræves til pakning. DNA'et pakkes ind i procapsidet af det ATP-drevne terminase motorprotein (gp17) med høj effektivitet. (C) Det pakkede Cre-enzym recirkulariserer det pakkede lineære plasmid-DNA mellem de to loxP-steder. Det DNA-holdige kapsid optages af eukaryote celler, her uden at vise et specifikt peptidmål, eller ind i eukaryote celler specifikt ved hjælp af Soc og Hoc viste peptider, der har høj affinitet for RP1 og RP2 receptorerne, henholdsvis. Kredit:Liu JL, et al. (Offentliggjort online inden tryk 26. august, 2014) Viralt nanopartikel-indkapslet enzym og omstruktureret DNA til cellelevering og genekspression. Kredit:Liu JL, et al. (2014) Viralt nanopartikel-indkapslet enzym og omstruktureret DNA til cellelevering og genekspression. Proc Natl Acad Sci USA Udgivet online før tryk 26. august, 2014. doi:10.1073/pnas.1321940111
(Phys.org) —Ved at indlæse et hvilket som helst specifikt protein og nukleinsyre i en icosaedrisk fag T4 capsid-baseret nanopartikel, den resulterende celleleveringsvehikels ligander kan binde til overfladen af specifikke målvæv for at levere protein/DNA-lasten. (Icosaedriske virale nanopartikler er evolutionære proteinskaller samlet i en hierarkisk rækkefølge, der resulterer i et stabilt proteinlag og et indre rum til at rumme nukleinsyrer og proteiner; et kapsid er proteinskallet af en virus.) Teknikken har lægemiddel- og gen- leveringsapplikationer til humane sygdomme, diagnostisk og cellulær billeddannelse, og andre medicinske områder. For nylig, forskere ved US Naval Research Laboratory, Washington, DC og University of Maryland i Baltimore pakkede T4 nanopartikler in vivo med aktiv cyklisk rekombination, eller Cre, rekombinase (et genetisk rekombinationsenzym, der bruges til at manipulere genomstruktur og kontrollere genekspression) og in vitro med fluorescerende mCherry (et fluorescerende protein, der bruges som markør, når det er mærket til molekyler og cellekomponenter) ekspressionsplasmid-DNA, og leverede disse nanopartikler til kræftceller:Når de blev frigivet til celler i nærværelse af både DNA og protein, rekombinasen øger mCherry-ekspression ved cirkularisering (dvs. at ændre det pakkede lineære DNA til en cirkulær løkke). Forskerne fastslår, at denne effektive og specifikke pakning i capsider og udpakning af både DNA og protein med frigivelse af de enzymatisk ændrede protein/DNA-komplekser fra nanopartiklerne til celler har potentiale i adskillige downstream-applikationer såsom genetiske og cancerterapeutiske midler.
Dr. Jinny L. Liu diskuterede papiret, at hun, Prof. Lindsay W. Black og deres medforfattere udgivet i Proceedings of the National Academy of Sciences USA . "Icosaedriske virale nanopartikler er i det væsentlige 100 nm gange 80 nm nanocontainere, der gør det muligt at pakke eksogent genetisk materiale in vitro gennem nukleinsyremaskineri, der generelt kun tillader lineær DNA/RNA at blive pakket gennem en portalkanal, " fortæller Liu Phys.org . "Imidlertid, in vitro proteinemballage er generelt umuligt, fordi der for de fleste virale nanopartikler ikke er noget proteinpakkemaskineri, der kan sammenlignes med nukleinsyrepakkemaskineri." Mens protein kan være kemisk tværbundet til kapsidets indre overflade, dette forventes at føre til proteindenaturering og tab af enzymatisk aktivitet.
Når det er sagt, naturen har udviklet løsninger på denne proteinemballage gåde. I løbet af in vivo viral capsid samling, Liu forklarer, nogle bakterielle vira, eller bakteriofager, målproteiner i procapsiderne Før nukleinsyren er pakket for at udstøde proteinerne med nukleinsyren, derved lette infektion i forbindelse med nukleinsyren. (En procapsid, eller prohead, er en umoden viral kapsidstruktur dannet i de tidlige stadier af selvsamling af nogle bakteriofager. Produktion og samling af stabile proheads er en væsentlig forløber for bakteriofag-genompakning.) Kun nogle få fager har velkarakteriseret in vivo proteinpakkesystemer, og fag T4 er bedst karakteriseret. "Prof. Blacks laboratorium på UMB og mit laboratorium på NRL har vist, at ikke kun et specifikt fremmed enzym – cyklisk rekombinations (Cre) rekombinase – kan pakkes ind i capsidet in vivo , men også at det er aktivt i kapsiden." Denne aktivitet blev demonstreret ved at vise religeringen (gensammenføjningen af to DNA-strenge eller andre molekyler ved hjælp af en fosfatesterbinding) af pakket lineært DNA flankeret med to Cre-rekombinationssteder.
Papiret viser, at den betydelige plads i en T4 nanocontainer rummer det aktive Cre-enzym sammen med eksogent DNA. "For potentielle anvendelser, T4 kan pakke op til 50 kb eksogent lineært DNA indeholdende ønskede gener i fuld længde sammen med rekombinaser, enten Cre eller λ-røde proteiner, for specifik homolog rekombination i kromosomet, " noterer Liu. ( Homolog rekombination er en type genetisk rekombination, hvor nukleotidsekvenser udveksles mellem to ens eller identiske DNA-molekyler.) "Vi forventer, at cas9-enzymet kan indkapsles på en sammenlignelig måde - og faktisk, mindst otte forskellige proteiner er blevet indkapslet på denne måde. Gennem homolog rekombination, vores system kan tillade det korrigerede gen at erstatte det muterede gen på dets oprindelige placering i kromosomet eller ved præcist at slå de overaktive gener i stamceller ud." Liu påpeger, at T4 leveringsvektoren er sikrere og bedre kontrolleret end andre virale leveringsgener terapi, såsom dem, der leverer gener ved hjælp af infektiøse animalske virale vektorer til tilfældigt at indsætte genet i kromosomet.
I deres papir, forfatterne rapporterer, at T4 capsid NP-genekspression og proteinleveringssystemet kan være komplementært til eller anvendes i forbindelse med genterapi baseret på RNA Cas og taran nuklease. (Cas-gener koder for proteiner relateret til DNA-loci, der indeholder korte gentagelser af basesekvenser kendt som Clustered Regularly Interspaced Short Palindromic Repeats, eller CRISPRs.) "T4 nanopartikelekspressionssystemet kan nemt komplementere Cas9 og taran nuklease-baseret rekombination ved at pakke det lineære cas9, target-sgRNA plasmid DNA, og Cre rekombinase – eller endda ligase, et enzym, der letter sammenføjningen af DNA-strenge – og leverer de resulterende T4-nanopartikler ind i de modtagende eukaryote celler med høj specificitet ved at anvende SOC og HOC, " fortæller Liu Phys.org . (SOC og HOC er dispensable T4 capsidproteiner.) "Ved at vise de målrettede ligander (bindingsmolekyler) på overfladen, T4 capsid-genekspressionen og proteinsystemet vil være i stand til effektivt at levere Cas9- og sgRNA-plasmiderne sammen til de ønskede modtagerceller. Relevante enzymatisk aktive proteiner Cas9, lambda exonuklease, lambda beta-protein og andre kan leveres direkte på samme tid fra T4-nanopartiklerne."

Måling af inhibering af endocytosehæmmere og kolokalisering med lysosomer i A546-T4-behandlede A549-celler. (A) Forbehandling med amantadin, specifikt stabilisering af de clathrin-belagte gruber, reducerede optagelsen af A546-T4 NP'er af A549-celler på en koncentrationsafhængig måde. (B) Forbehandling med PI3-kinaseinhibitoren, wortmannin, reducerede også optagelsen af A546-T4 på en koncentrationsafhængig måde. (C) Et overlappende konfokalt cellebillede opnået med et 60× objektiv med de internaliserede A546-T4 procapsider (gul), lysosomer farvet med LysoTracker Blue (blå), og de overlappende pletter (hvide). (Skalalinje, 10 μm.) (D) Et konfokalt billede viser det brede billede af behandlede celler, der indeholder overlappende dele (hvide pletter) af lysosomer (blå) med A546-T4 procapsider (gul). Billedet blev taget med et 20× objektiv. (Skalalinje, 50 μm.) Kredit:Liu JL, et al. (Offentliggjort online inden tryk 26. august, 2014) Viralt nanopartikel-indkapslet enzym og omstruktureret DNA til cellelevering og genekspression. Kredit:Liu JL, et al. (2014) Viralt nanopartikel-indkapslet enzym og omstruktureret DNA til cellelevering og genekspression. Proc Natl Acad Sci USA Udgivet online før tryk 26. august, 2014. doi:10.1073/pnas.1321940111
Liu tilføjer, at hendes laboratorium også har studeret cellebilleddannelse og lægemiddel/genlevering til eukaryote celler ved hjælp af T4 haleløse nanopartikler, som forskerne påviste kan trænge ind i de eukaryote celler uden at forårsage celledød.
Et specifikt eksempel på potentielle downstream-lægemiddel- og genterapeutiske anvendelser som følge af den nye tilgang er levering af det toksiske protein og lineære plasmid, der producerer neutraliserende peptider eller antistoffer til målrettede cancerceller, der viser specifikke cancermarkører ved hjælp af højaffinitets-SOC + HOC-markørbindende proteiner på overflade af kapsider, mens et andet eksempel er at bruge systemet til HIV-genterapi.
Liu tilføjer, at der er flere veje til at bruge dette system til genterapi:
- Levering af T4-nanopartikler pakket med rekombinasen (eller ligasen) og lineært plasmid-DNA for at producere gp120 eller interferon for at generere eller booste immunresponset hos patienter
- Leverer T4-nanopartikler pakket med rekombinase (ligase) og det lineære opløselige CD40-ekspressionsplasmid-DNA til T-lymfocytter eller hæmatopoietiske celler for at blokere infektionen af HIV-1
- Inhibering af RNA ved at levere det konstruerede plasmid-DNA, der kan producere lokke-RNA til binding af viral sense-DNA
- Hæmmer protein ved at levere pakkede anti-virale antistoffer og anti-HIV antistof plasmid DNA
Ud over diagnostisk og cellulær billeddannelse, T4 nanopartikelgen-proteinsystemet kan levere reparerede gener til at korrigere menneskelige genetiske sygdomme – f.eks. reversering af adenosindeaminase (ADA) mangel ved at introducere protein-DNA-komplekset til at udtrykke ADA i stamceller. Andre brede forskningsområder påvirket af genterapiteknologier, såsom genetiske defekter, Kræft, neurologiske sygdomme hos voksne, og selve ældningen, kan også have gavn af denne undersøgelse.
Bevæger sig fremad, forskerne ønsker at udvikle flere T4-procapsider, der pakker exonuklease og andre rekombinaser sammen med manipuleret mål-DNA for at demonstrere, at de resulterende T4-capsider kan indsætte genet i en stamcellelinje med en genetisk mangel. "Ud over, " konkluderer Liu, "Vi arbejder på at tilpasse vores system til at levere terapeutiske peptider eller antistoffer til celler udsat for eller inficeret med biotrusselsmidler, såsom proteintoksiner eller vira, effektiv neutralisering af toksineffekter. Behandling og helbredelse af celler og væv udsat for sådanne midler er af stor interesse for vores bioforsvarsforskningssamfund."
© 2014 Phys.org
 Varme artikler
Varme artikler
-
 Forskere udvikler grafensensorer, der kan revolutionere tingenes internetKredit:University of Manchester Forskere ved University of Manchester har udviklet grafensensorer indlejret i RFIDer, som har potentiale til at revolutionere tingenes internet (IoT). Ved at lægge
Forskere udvikler grafensensorer, der kan revolutionere tingenes internetKredit:University of Manchester Forskere ved University of Manchester har udviklet grafensensorer indlejret i RFIDer, som har potentiale til at revolutionere tingenes internet (IoT). Ved at lægge -
 Forskere udvikler anti-bakterielle ansigtsmasker af grafenDe fleste kulstofholdige materialer kan omdannes til grafen ved hjælp af et kommercielt CO2 infrarødt lasersystem. Kredit:City University of Hong Kong Ansigtsmasker er blevet et vigtigt redskab i
Forskere udvikler anti-bakterielle ansigtsmasker af grafenDe fleste kulstofholdige materialer kan omdannes til grafen ved hjælp af et kommercielt CO2 infrarødt lasersystem. Kredit:City University of Hong Kong Ansigtsmasker er blevet et vigtigt redskab i -
 Hvor uigennemtrængeligt er den uigennemtrængelige grafen?Denne visualisering viser lag af grafen, der bruges til membraner. Kredit:University of Manchester Nye eksperimenter udført af forskere ved University of Manchester har sat de bedste grænser endnu
Hvor uigennemtrængeligt er den uigennemtrængelige grafen?Denne visualisering viser lag af grafen, der bruges til membraner. Kredit:University of Manchester Nye eksperimenter udført af forskere ved University of Manchester har sat de bedste grænser endnu -
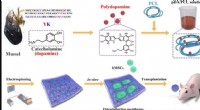 Knoglevævsteknik - nano-lim polymermembraner til robust knogleregenereringSkematisk tegning af fremstillingen af de konstruerede membraner via elektrospinning af PCL og PDA NPer. Kredit:NPG Asia Materials, doi:10.1038/s41427-019-0139-5 I en ny undersøgelse nu offentli
Knoglevævsteknik - nano-lim polymermembraner til robust knogleregenereringSkematisk tegning af fremstillingen af de konstruerede membraner via elektrospinning af PCL og PDA NPer. Kredit:NPG Asia Materials, doi:10.1038/s41427-019-0139-5 I en ny undersøgelse nu offentli
- Hvad er forskellen mellem en rose og en blomst?
- Hvordan fungerer en magneto?
- Solceller:UQAM-forsker løser to 20-årige problemer
- Etnisk frygt udhuler demokratiske holdninger blandt republikanere, nye forskningsfund
- Midt i landsdækkende tørke, Rom søger måder at undgå rationering på
- Endelig datafrigivelse fra DESI Legacy Imaging Surveys udgivet


