Små konjugerede polyelektrolyt-nanopartikelsonder fremstillet ved ultralyd viser sig at være overlegen i forhold til kommercielle produkter
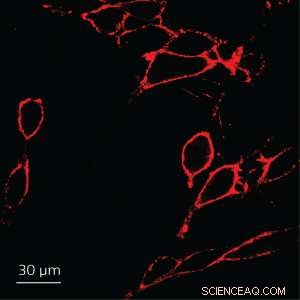
En let og effektiv metode er blevet udviklet til at fremstille lyse enkeltkædede konjugerede polyelektrolytprober i kvante-prikstørrelse til specifik ekstracellulær mærkning og billeddannelse. Kredit:gengivet, med tilladelse, fra Ref. 1 © 2014 WILEY-VCH Verlag GmbH &Co. KGaA, Weinheim
James Bond kunne godt lide, at hans martini blev 'rystet, ikke rørt', og nu har A*STAR -forskere fundet ud af, at rysten, frem for omrøring, producerer også bedre nanopartikler til bioimaging - med vigtige konsekvenser for spionage på kræft.
Fluorescerende prober, der i øjeblikket bruges til bioimaging (f.eks. cadmium selenid quantum dots) fluorescerer stærkt nok til at dukke op på detektorer, men kan være giftigt og dermed uegnet til brug i kroppen. Nu, Bin Liu og hendes kolleger fra A*STAR Institute of Materials Research and Engineering har med succes fremstillet nanopartikelsonder, der er biokompatible og også har en høj specificitet og fotostabilitet. Desuden, disse nye prober har fremragende ydeevne i det langt røde til nær-infrarøde område i det elektromagnetiske spektrum, som er af særlig interesse for kræftbilleddannelse.
Teamets metode er elegant i sin enkelhed - det forbedrer probernes optiske egenskaber ved blot at variere nanopartiklernes størrelse og form. "Dette giver os mulighed for at omgå komplicerede molekylære design- og synteseprocesser, "forklarer Liu." Det giver en let, men effektiv metode til udvikling af stærkt langt røde-nær-infrarøde fluorescerende sonder. "
Forskerne producerede nanopartiklerne i vand ved to metoder - omrøring og ultralyd (dvs. 'ryster' ved meget høje frekvenser). Ultralydning gav nanopartikler med en gennemsnitlig størrelse på 4 nanometer, som er betydeligt mindre end deres omrørte modparter. Disse nanopartikler var også meget lysere, med et kvanteudbytte på 26 procent i vand - mere end fem gange lysere end nanopartiklerne produceret ved omrøring.
Liu forklarer, at ultralydning producerer polymerkæder, der er tættere på hinanden, resulterer i "kompakte strukturer, der effektivt kan forhindre invasion af vand og dermed undertrykke slukning, giver forbedret fluorescens. "
Forskerne testede derefter opførsel af nanopartikler produceret ved sonikering i biologiske omgivelser for at afgøre, om de ville være effektive sonder for et specifikt biologisk mål. De valgte streptavidin, et protein, der har en høj affinitet for epithelcelleadhæsionsmolekyle (EpCAM) - en fælles biomarkør for forskellige kræftformer. Efter konjugering af streptavidin til overfladerne af nanopartiklerne, forskerne undersøgte nanopartiklernes effektivitet som en ekstracellulær sonde for EpCAM ved at anvende MCF-7 brystkræftceller som en modelcellelinje (se billede). Nanopartiklerne udviste en fremragende fotostabilitet og en meget højere fluorescens end en kommercielt tilgængelig probe (Cy3-SA).
Liu bemærker, at ved at skifte streptavidin med et andet protein kan de samme nanopartikler bruges til at målrette mod andre biomarkører. "Dette vil føre til en ny generation af fluorescerende sonder til billedstyret terapi, " hun siger.
 Varme artikler
Varme artikler
-
 Kemiprofessor er den første til at bruge lys til at lave guldkrystalnanopartiklerKredit:University of Florida Et team af forskere fra University of Florida har fundet ud af, hvordan guld kan bruges i krystaller, der dyrkes af lys til at skabe nanopartikler, en opdagelse, der h
Kemiprofessor er den første til at bruge lys til at lave guldkrystalnanopartiklerKredit:University of Florida Et team af forskere fra University of Florida har fundet ud af, hvordan guld kan bruges i krystaller, der dyrkes af lys til at skabe nanopartikler, en opdagelse, der h -
 Forskere udvikler trådløst, ultratynde og batterifrie belastningssensorer, der er 10 gange mere fø…NUS-forskere har udviklet trådløse, ultratynde og batterifrie belastningssensorer, der er 10 gange mere følsomme end konventionelle teknologier. Disse lette belastningssensorer kan indbygges i rehabil
Forskere udvikler trådløst, ultratynde og batterifrie belastningssensorer, der er 10 gange mere fø…NUS-forskere har udviklet trådløse, ultratynde og batterifrie belastningssensorer, der er 10 gange mere følsomme end konventionelle teknologier. Disse lette belastningssensorer kan indbygges i rehabil -
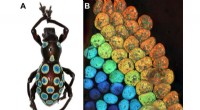 Ny farvegenereringsmekanisme opdaget i regnbuesnudebillenTil venstre:Et fotografi af regnbue-snudebillen, med de regnbuefarvede pletter på thorax og elytra (vingehylstre). Til højre:Et mikroskopbillede af kanten af en enkelt regnbueplet, viser de forskell
Ny farvegenereringsmekanisme opdaget i regnbuesnudebillenTil venstre:Et fotografi af regnbue-snudebillen, med de regnbuefarvede pletter på thorax og elytra (vingehylstre). Til højre:Et mikroskopbillede af kanten af en enkelt regnbueplet, viser de forskell -
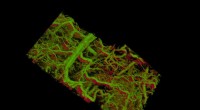 Forskere udvikler ny teknik til billeddannelse af celler og væv under hudenGuldnanoroder i blodårerne i et musøre virker grønne. Nederst til højre viser kar i en svulst, der ligger under huden. Kredit:de la Zerda lab Forskere har mange værktøjer til rådighed til at se på
Forskere udvikler ny teknik til billeddannelse af celler og væv under hudenGuldnanoroder i blodårerne i et musøre virker grønne. Nederst til højre viser kar i en svulst, der ligger under huden. Kredit:de la Zerda lab Forskere har mange værktøjer til rådighed til at se på
- Nigerianere kræver luftkvalitetsdata på grund af frygt for forurening
- Computermodellering af WNK-kinasehæmmere kunne tilbyde nye værktøjer til at forstå hypertension
- Hvad er en decibel, og hvordan måles den?
- Cybersikkerhedstest på ISS
- Sensorer gjorde denne virksomhed til verdens førende inden for værktøjsproduktion
- Sådan beregnes procentforskel med tre beløb


