Ny tilgang til nanopartikler til levering af lægemidler har potentiale til behandling af fedme
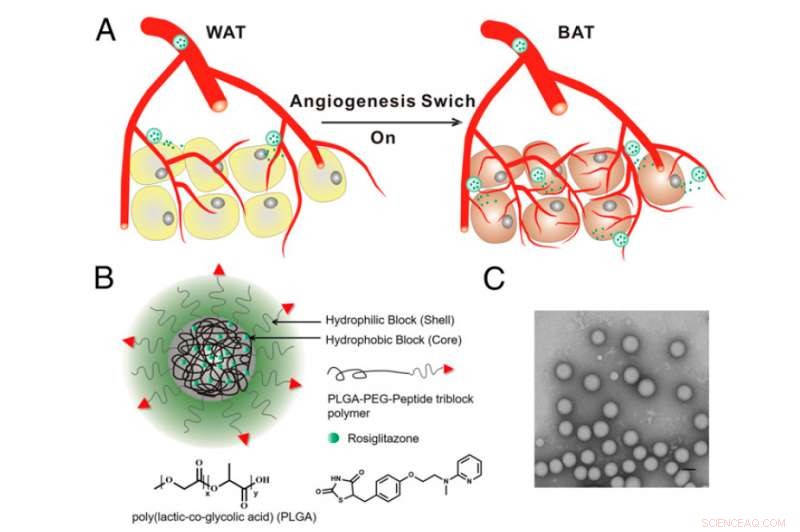
(Top) Stimulering af væksten af nye blodkar (angiogenese) i fedtvæv omdanner vævet fra fedtopbevarende hvidt væv til fedtforbrændende brunt væv. Et skema af nanopartiklerne (nederst til venstre), som forskere fra MIT og Brigham og Women's Hospital brugte til at levere angiogenesemedicin til fedtvæv. (Nederst til højre) Nanopartiklerne afbildet ved transmissionselektronmikroskopi.
Forskere ved MIT og Brigham and Women's Hospital har udviklet nanopartikler, der kan levere medicin mod fedme direkte til fedtvæv. Overvægtige mus behandlet med disse nanopartikler tabte 10 procent af deres kropsvægt i løbet af 25 dage, uden at vise nogen negative bivirkninger.
Lægemidlerne virker ved at transformere hvidt fedtvæv, som er lavet af fedtlagrende celler, ind i brunt fedtvæv, som forbrænder fedt. Lægemidlerne stimulerer også væksten af nye blodkar i fedtvæv, som positivt forstærker målretningen efter nanopartikler og hjælper med den hvid-til-brune transformation.
Disse stoffer, som ikke er FDA-godkendt til behandling af fedme, er ikke nye, men forskerholdet udviklede en ny måde at levere dem på, så de akkumuleres i fedtvæv, hjælper med at undgå uønskede bivirkninger i andre dele af kroppen.
"Fordelen her er, at du nu har en måde at målrette det til et bestemt område og ikke give kroppen systemiske effekter. Du kan få de positive effekter, som du ønsker med hensyn til antifedme, men ikke de negative, der nogle gange opstår, "siger Robert Langer, David H. Koch Institute Professor ved MIT og medlem af MIT's Koch Institute for Integrative Cancer Research.
Langer og Omid Farokhzad, direktør for Laboratory of Nanomedicine and Biomaterials på Brigham and Women's Hospital, er de ledende forfattere af undersøgelsen, som fremgår af Proceedings of the National Academy of Sciences ugen den 2. maj. Bladets hovedforfattere er tidligere MIT postdoc Yuan Xue og tidligere BWH postdoc Xiaoyang Xu.
Målretning mod fedt
Langer og hans kolleger har tidligere vist, at fremme væksten af nye blodkar, en proces kendt som angiogenese, kan hjælpe med at omdanne fedtvæv og føre til vægttab hos mus. Imidlertid, lægemidler, der fremmer angiogenese, kan være skadelige for resten af kroppen.
For at prøve at overvinde det, Langer og Farokhzad vendte sig mod nanopartikel-medikamentleveringsstrategien, de har udviklet i de senere år til behandling af kræft og andre sygdomme. Ved at målrette disse partikler til sygdomsstedet, de kan levere en kraftig dosis og samtidig minimere lægemidlets ophobning i andre områder.
Forskerne designet partiklerne til at bære stofferne i deres hydrofobe kerner, bundet til en polymer kendt som PLGA, som bruges i mange andre lægemiddelleveringspartikler og medicinsk udstyr. De pakkede to forskellige lægemidler i partiklerne:rosiglitazon, som er godkendt til behandling af diabetes, men som ikke er meget udbredt på grund af uønskede bivirkninger, og en analog af prostaglandin (en type humant hormon). Begge lægemidler aktiverer en cellulær receptor kendt som PPAR, som stimulerer angiogenese og fedttransformation.
Nanopartiklernes ydre skal består af en anden polymer, PEG, indlejret med målmolekyler, der leder partiklerne til den korrekte destination. Disse målrettede molekyler binder sig til proteiner, der findes i foringen af blodkarrene, der omgiver fedtvæv.
Forskerne testede partiklerne i mus, der var blevet overvægtige efter at have fået en kost med højt fedtindhold. Musene tabte omkring 10 procent af deres kropsvægt, og deres niveauer af kolesterol og triglycerider (molekyler, der er hovedbestanddelen af kropsfedt hos mennesker) faldt også. Musene blev også mere følsomme over for insulin. (Fedme fører ofte til insulinfølsomhed, som er en risikofaktor for type 2-diabetes).
Musene viste ingen bivirkninger af behandlingen, som blev leveret hver anden dag i 25 dage.
Leveringsudfordringer
Med det nuværende system, partiklerne injiceres intravenøst, hvilket kunne gøre denne tilgang velegnet til sygeligt overvægtige patienter, som er i betydelig risiko for fedme-relaterede sygdomme, siger Farokhzad.
"For at det skal være mere bredt anvendeligt til behandling af fedme, vi er nødt til at finde på nemmere måder at administrere disse målrettede nanopartikler på, såsom oralt, " han siger.
Udfordringen ved at levere nanopartikler oralt er, at det er svært for dem at trænge ind i tarmens slimhinde. I en tidligere undersøgelse, imidlertid, Langer og Farokhzad udviklede en nanopartikel belagt med antistoffer, der binder til receptorer, der findes på overflader af celler, der beklæder tarmen, tillader nanopartiklerne at blive absorberet gennem fordøjelseskanalen. For nylig, Farokhzad og kolleger har udviklet en anden oralt leveret nanopartikel, der bruger transferrin, et protein involveret i transporten af jern i kroppen, at lette aktiv transport af nanopartikler over tarmen.
Forskerne håber også at finde mere specifikke fedtvævsmål for nanopartiklerne, hvilket yderligere kunne reducere muligheden for bivirkninger, og de kan også undersøge brugen af andre lægemidler med lavere toksicitet.
"Dette er en proof-of-concept tilgang til selektivt at målrette det hvide fedtvæv og 'brune det' for at give kroppen mulighed for at forbrænde fedt. Teknologien kan derefter bruges sammen med andre lægemiddelmolekyler, der kan udvikles eller andre mål, der kan komme op, " siger Farokhzad.
Forskningen blev finansieret af National Institutes of Health og en Koch-Prostate Cancer Foundation Award i nanoterapeutik.
Denne historie er genudgivet med tilladelse fra MIT News (web.mit.edu/newsoffice/), et populært websted, der dækker nyheder om MIT-forskning, innovation og undervisning.
 Varme artikler
Varme artikler
-
 Nye tilgange er nødvendige for at måle sikkerheden ved nanoteknologibaserede pesticiderDisse titandioxid nanopartikler, set gennem et scanningselektronmikroskop, er den type ekstraordinært små partikler, der studeres i et program ved Oregon State University om sikkerheden ved nanoteknol
Nye tilgange er nødvendige for at måle sikkerheden ved nanoteknologibaserede pesticiderDisse titandioxid nanopartikler, set gennem et scanningselektronmikroskop, er den type ekstraordinært små partikler, der studeres i et program ved Oregon State University om sikkerheden ved nanoteknol -
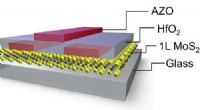 Klart fører til fuldt gennemsigtige enhederiEn fuldt gennemsigtig tyndfilmstransistor bestående af et molybdænsulfid (MoS2) monolag; hafniumdioxid (HfO2), som bruges til belægning; og aluminium-doteret zinkoxid (AZO) kontakter. Kredit:2017 WIL
Klart fører til fuldt gennemsigtige enhederiEn fuldt gennemsigtig tyndfilmstransistor bestående af et molybdænsulfid (MoS2) monolag; hafniumdioxid (HfO2), som bruges til belægning; og aluminium-doteret zinkoxid (AZO) kontakter. Kredit:2017 WIL -
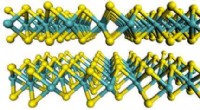 Et molekyle tykt materiale har store fordele:Forskere producerer komplekse kredsløb fra molybdændi…Diagram viser den flade struktur af det materiale, der bruges af MIT-teamet, molybdændisulfid. Molybdæn atomer er vist i krikand, og svovlatomer i gult. Billede udlånt af Wang et al. Opdagelsen af
Et molekyle tykt materiale har store fordele:Forskere producerer komplekse kredsløb fra molybdændi…Diagram viser den flade struktur af det materiale, der bruges af MIT-teamet, molybdændisulfid. Molybdæn atomer er vist i krikand, og svovlatomer i gult. Billede udlånt af Wang et al. Opdagelsen af -
 Forskere udvikler en tilgang til at syntetisere ukonventionelle nanolegeringer til elektrokatalytisk…Kredit:CC0 Public Domain Metalliske legeringer på nanometerskala (nanolegeringer) har et stort potentiale i elektrokatalyse. Interaktionen mellem forskellige komponenter i nanolegeringer kan ændre
Forskere udvikler en tilgang til at syntetisere ukonventionelle nanolegeringer til elektrokatalytisk…Kredit:CC0 Public Domain Metalliske legeringer på nanometerskala (nanolegeringer) har et stort potentiale i elektrokatalyse. Interaktionen mellem forskellige komponenter i nanolegeringer kan ændre
- Socialt dilemma følger efter udbruddet af Kilauea-vulkanen i 2018
- Porøse grafenbånd doteret med nitrogen til elektronik og kvanteberegning
- Energifri superhurtig computing opfundet af forskere, der bruger lysimpulser
- Trump-administrationen kaster koldt vand på klimaforandringstruslen mod koralrevene
- Svenske virksomheder afviser udvisninger af faglærte arbejdere
- Potentielt store økonomiske konsekvenser af klimaændringer kan undgås ved menneskelige handlinger


