AFM filmer levende nukleare porekomplekser på arbejde for første gang

Videobilleddannelse ved højhastigheds-AFM fanger native nukleare porekomplekser på arbejde; den indsatte skalabjælke er 10 nanometer. Kredit:Universitetet i Basel
Ved hjælp af et ultrahurtigt scannende atomkraftmikroskop, et team af forskere fra universitetet i Basel har for første gang filmet "levende" nukleare porekomplekser på arbejde. Nukleare porer er molekylære maskiner, der styrer trafikken, der kommer ind eller ud af cellekernen. I deres artikel offentliggjort i Natur nanoteknologi , forskerne forklarer, hvordan passage af uønskede molekyler forhindres ved hurtigt at flytte molekylære "tentakler" inde i poren.
Atomkraftmikroskopet (AFM) er ikke et mikroskop at se igennem. Som en blind mand bruger sine fingre, det "føler" en overflade med en ekstremt fin spids til at løse små mobilstrukturer på kun en milliontedel af en millimeter i størrelse, såsom porerne i den nukleare kappe. Imidlertid, denne proces er normalt langsom og kan tage op til et minut at tage et billede. Sammenlignet med, moderne high-speed AFM'er er i stand til at optage film af molekyler i aktion ved at tage flere hundrede billeder i minuttet.
Brug af højhastigheds AFM, Roderick Lim, Argovia professor ved Biozentrum og Swiss Nanoscience Institute ved University of Basel, har ikke kun direkte visualiseret den nukleare pores selektive barriere, men også dens dynamiske adfærd for at løse et mangeårigt mysterium om, hvordan uønskede molekyler forhindres i at komme ind i kernen.
Nukleare porekomplekser regulerer transporten af molekyler
Den overordnede struktur af de nukleare porer er almindelig kendt. Det er ikke simple huller, men er massive transportknudepunkter, der inkorporerer i tusindvis af kernemembranen. De har en donut-formet struktur bestående af omkring tredive forskellige proteiner, kaldet nukleoporiner, og en central transportkanal. Indenfor poren, flere uordnede proteiner (FG Nups) danner en selektivitetsbarriere eller filter. Mens små molekyler nemt kan passere denne barriere, store molekyler såsom proteiner forhindres i at trænge ind i kerneporen. En undtagelse fra dette er de proteiner, der er nødvendige i cellekernen, for eksempel, til reparation eller replikation af genetisk materiale. Deres translokation fra cytoplasmaet til kernen assisteres af transportreceptorer, der genkender et specifikt "adressemærke" båret af disse proteiner.
Højhastigheds-AFM afslører dynamiske processer
"Med højhastigheds-AFM kunne vi for første gang, kigger inde i indfødte nukleare porekomplekser, kun fyrre nanometer i størrelse", siger Lim. "Denne metode er en ægte game changer. Vi kunne se de enkelte FG Nups og filme dem i aktion. Dette var ikke muligt indtil nu!"
Derudover Yusuke Sakiyama, den ph.d.-studerende, der udførte forsøgene, var nødt til at dyrke superskarpe kulstof nanofibre på hver højhastighedssonde for at nå ind i NPC. Dette genererer derefter en videosekvens fra flere billeder, der gør det muligt for forskeren at observere den "sandt til liv" dynamikken i biologiske processer på nanometerniveau.
En barriere af bølgende molekylære "tentakler"
På grund af den høje rumlige og tidsmæssige opløsning, forskerne var i stand til at vise, at FG Nup-filamenterne er meget fleksible. "De er ikke stive børster, men tværtimod. Ligesom de tyndeste fangarme, FG Nups svinger hurtigt, forlænge og trække sig tilbage, og undertiden blander sig kortvarigt i poren ", siger Lim. Hastigheden af deres bevægelse bestemmer, hvilke molekyler der kan passere gennem poren. "Store partikler bevæger sig meget langsommere end FG Nups og forhindres dermed i at komme ind i NPC ved gentagne kollisioner", forklarer Lim. "Små molekyler, imidlertid, gennemgår hurtig diffusion og har stor sandsynlighed for at passere FG Nup-barrieren."
Ved at forstå, hvordan NPC'er fungerer som transportknudepunkter i levende celler, Lim, som er medlem af NCCR Molecular Systems Engineering, undersøger nu, hvordan NPC-inspirerede selektive filtre kan regulere molekylær trafik i ikke-biologiske systemer.
 Varme artikler
Varme artikler
-
 Kvante nanodiamanter kan hjælpe med at opdage sygdom tidligereEn kunstners opfattelse af nanodiamanter brugt til in vitro-diagnostik. Kredit:Ella Maru Studio/ UCL Nanodiamanters kvantesansevner kan bruges til at forbedre følsomheden af papirbaserede diagno
Kvante nanodiamanter kan hjælpe med at opdage sygdom tidligereEn kunstners opfattelse af nanodiamanter brugt til in vitro-diagnostik. Kredit:Ella Maru Studio/ UCL Nanodiamanters kvantesansevner kan bruges til at forbedre følsomheden af papirbaserede diagno -
 Forbedring af nanosikkerhed gennem forskningKredit:Shutterstock Nanoteknologi forventes at være en af de vitale teknologiske drivere til at omdanne EU til en ægte innovationsunion. Fra at forbedre kosmetik og tekstiler til at hjælpe med a
Forbedring af nanosikkerhed gennem forskningKredit:Shutterstock Nanoteknologi forventes at være en af de vitale teknologiske drivere til at omdanne EU til en ægte innovationsunion. Fra at forbedre kosmetik og tekstiler til at hjælpe med a -
 Carbon nanotråde opnået ved at temperere diamantandicarboxylsyre inde i carbon nanorør(Phys.org) —Kulstofbaserede nanomaterialer har unikke egenskaber, der gør dem nyttige til mange tekniske applikationer, herunder let konstruktion, elektronik, energiproduktion, miljøteknologi, og medi
Carbon nanotråde opnået ved at temperere diamantandicarboxylsyre inde i carbon nanorør(Phys.org) —Kulstofbaserede nanomaterialer har unikke egenskaber, der gør dem nyttige til mange tekniske applikationer, herunder let konstruktion, elektronik, energiproduktion, miljøteknologi, og medi -
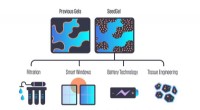 Nanopartikelgel forener olie og vand i en fremstillingsvenlig tilgangI modsætning til andre gel-fremgangsmåder, hvor nanopartikler forbliver ved grænsefladen mellem gelens to opløsningsmidler (øverst til venstre), den nye tilgang koncentrerer nanopartikler i det indre
Nanopartikelgel forener olie og vand i en fremstillingsvenlig tilgangI modsætning til andre gel-fremgangsmåder, hvor nanopartikler forbliver ved grænsefladen mellem gelens to opløsningsmidler (øverst til venstre), den nye tilgang koncentrerer nanopartikler i det indre
- Vektorbårne sygdomme formede menneskets historie og afslører raceforskelle
- Venlighed er vigtigere i en ny ven, end hvilken gruppe hun tilhører
- Kina rapporterer ingen større kollaps efter kraftigt jordskælv
- Forskere får det første fuldstændige kig på protein bag følesansen
- Menneskelig aktivitet på floder overskrider, sammensatte virkninger af klimaændringer
- Poop knive, araknofobe entomologer vinder 2020 Ig Nobels


