Forskere forbedrer computermodellering til design af nanobærere til lægemiddellevering

Forskernes nye model tager højde for, hvordan cytoskeletal pinning påvirker bølgerne i en celles membran. Kredit:University of Pennsylvania
Et hold forskere fra University of Pennsylvania har udviklet en computermodel, der vil hjælpe med design af nanobærere, mikroskopiske strukturer, der bruges til at lede lægemidler til deres mål i kroppen. Modellen redegør bedre for, hvordan overfladerne af forskellige celletyper bølger på grund af termiske udsving, informerende funktioner i nanobærerne, der vil hjælpe dem med at holde sig til celler længe nok til at levere deres nyttelast.
Undersøgelsen blev ledet af Ravi Radhakrishnan, en professor i afdelingerne for bioteknik og kemisk og biomolekylær teknik på Penns School of Engineering and Applied Science, og Ramakrishnan Natesan, et medlem af hans laboratorium.
Richard Tourdot bidrog også til undersøgelsen, et Radhakrishnan lab medlem; David Eckmann, Horatio C. Wood-professor i anæstesiologi og kritisk pleje ved Penns Perelman School of Medicine; Portonovo Ayyaswamy, Asa Whitney professor i maskinteknik og anvendt mekanik i Penn Engineering; og Vladimir Muzykantov, en professor i farmakologi i Penn Medicine.
Det blev offentliggjort i tidsskriftet Royal Society Open Science .
Nanobærere kan designes med molekyler på deres ydre, der kun binder til biomarkører, der findes på en bestemt type celle. Denne type målretning kan reducere bivirkninger, som når kemoterapimedicin ødelægger sunde celler i stedet for kræftceller, men biomekanikken i denne bindingsproces er kompleks.
Tidligere arbejde fra nogle af forskerne afslørede et kontraintuitivt forhold, der antydede, at tilføjelse af flere målrettede molekyler på nanocarrierens overflade ikke altid er bedre.
En nanobærer med flere af disse målrettede molekyler kan finde og binde til mange af de tilsvarende biomarkører på én gang. Selvom en sådan konfiguration er stabil, det kan mindske nanobærerens evne til at skelne mellem sundt og sygt væv. At have færre målrettede molekyler gør nanobæreren mere selektiv, da det vil have sværere ved at binde sig til sundt væv, hvor de tilsvarende biomarkører ikke er overudtrykt.
Holdets nye undersøgelse tilføjer nye dimensioner til modellen for samspillet mellem den cellulære overflade og nanobæreren.
"Selve celleoverfladen er som et campingvognstelt på en blæsende dag i en ørken, " sagde Radhakrishnan. "Jo mere overskydende i kluden, jo mere flagren af teltet. Tilsvarende jo mere overskydende cellemembranareal på 'teltpælene, cellens cytoskelet, jo mere flagren af membranen på grund af termisk bevægelse."
Penn-teamet fandt ud af, at forskellige celletyper har forskellige mængder af dette overskydende membranareal, og at denne mekaniske parameter styrer, hvor godt nanobærere kan binde til cellen. Regnskab for flagrende membraner i deres computermodeller, ud over mængden af målrettede molekyler på nanobæreren og biomarkører på celleoverfladen, har fremhævet vigtigheden af disse mekaniske aspekter i, hvor effektivt nanocarriers kan levere deres nyttelast.
"Disse designkriterier, " sagde Radhakrishnan, "kan bruges til skræddersyet design af nanobærere til en given patient eller patient-kohorte, viser derfor en vigtig vej frem for tilpasset nanocarrier-design i en æra med personlig medicin."
 Varme artikler
Varme artikler
-
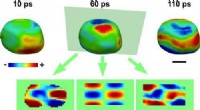 Guld nanokrystal vibration fanget på milliard-billeder-per-sekund film (m/ video)De akustiske fononer kan visualiseres på overfladen som områder med sammentrækning (blå) og ekspansion (rød). Der er også vist todimensionelle billeder, der sammenligner de eksperimentelle resultater
Guld nanokrystal vibration fanget på milliard-billeder-per-sekund film (m/ video)De akustiske fononer kan visualiseres på overfladen som områder med sammentrækning (blå) og ekspansion (rød). Der er også vist todimensionelle billeder, der sammenligner de eksperimentelle resultater -
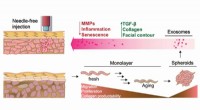 Solbruner, helbred dig selv:Exosomterapi kan muliggøre bedre reparation af solen, aldersskadet hudDermale monolag fibroblaster blev dyrket til sfæroider, derefter blev exosomer opsamlet og leveret af en nålefri injektor til behandling af hudens aldring. Kredit:North Carolina State University I
Solbruner, helbred dig selv:Exosomterapi kan muliggøre bedre reparation af solen, aldersskadet hudDermale monolag fibroblaster blev dyrket til sfæroider, derefter blev exosomer opsamlet og leveret af en nålefri injektor til behandling af hudens aldring. Kredit:North Carolina State University I -
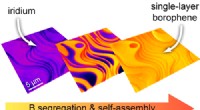 Syntese af 2D-materiale med stort område:Atomlag skubber overfladetrin vækAt studere kinetikken af borophendannelse i lavenergielektronmikroskopi viser, at overfladetrin samles under borophendannelsen, hvilket resulterer i aflange og udvidede borophendomæner med exception
Syntese af 2D-materiale med stort område:Atomlag skubber overfladetrin vækAt studere kinetikken af borophendannelse i lavenergielektronmikroskopi viser, at overfladetrin samles under borophendannelsen, hvilket resulterer i aflange og udvidede borophendomæner med exception -
 Nanomaterialer ændrer verden - men vi har stadig ikke tilstrækkelige sikkerhedstests for demKredit:joker1991/Shutterstock Nanoteknologi kan meget vel være en af de mest omtalte industrier i de sidste par år. Forudsagt at værdien 173,95 milliarder USD globalt i 2025, denne hurtige sekto
Nanomaterialer ændrer verden - men vi har stadig ikke tilstrækkelige sikkerhedstests for demKredit:joker1991/Shutterstock Nanoteknologi kan meget vel være en af de mest omtalte industrier i de sidste par år. Forudsagt at værdien 173,95 milliarder USD globalt i 2025, denne hurtige sekto
- Hvedegluten kan bruges til at lave bæredygtigt blemateriale
- Forskningsstudie forbedrer solstrålingsprognoser med 30%
- Guld nanopartikler afslører amyloid fibriller
- Ændrer vores kost for at redde planeten
- Naturlig kapital nøglen til global velstand, Oxfords økonomer advarer
- Mars ændrede beboelighed registreret af gamle klitmarker i Gale-krateret


