Multifunktionelle lægemiddelbærere i nanostørrelse baseret på reaktive polypept(o)ider
Bæresystemer i nanostørrelse har medicinsk anvendelse til at forbedre bioaktive midlers farmakologiske egenskaber. For mange terapeutiske tilgange, det er vigtigt, at bæresystemet stabilt kan inkorporere lasten under cirkulation uden at fremkalde aggregering, mens last ideelt set kun skal frigives efter vellykket cellulær optagelse. Disse krav er hidtil kun blevet opfyldt af kemitilgange med nanopartikler, som er svære at karakterisere. Følgelig, klinisk oversættelse af disse systemer har været meget vanskelig at opnå.
Kemikere fra Mainz og samarbejdspartnere har vist, at reaktive polypept(o)ider udgør ideelle byggesten til at kontrollere morfologi og funktion af bærersystemer på en enkel, men præcis måde. Polypept(o)ider (polysarcosin-blok-polypeptid-copolymerer) er dukket op som interessante hybridmaterialer til lægemiddelbærersystemer, da de kombinerer proteinresistens og høj vandopløselighed af polysarcosin med stimuliernes reaktionsevne, iboende multifunktionalitet, og sekundær strukturdannelse af polypeptider.
I dette samarbejdsarbejde, forskerne viste for første gang, at dannelsen af β-sheets af det syntetiske polypeptidsegment kan udnyttes til bevidst at manipulere morfologien af polymere miceller (Klinker K et al. Angew. Chem. Int. Ed . 2017, 56 (32), 9608-9613 &Angew. Chem. 2017, 129 (32), 9737-9742), som muliggør syntesen af enten sfæriske eller ormelignende miceller fra den samme blokcopolymer. Ved at anvende reaktive grupper i polypeptidsegmentet af blokcopolymeren, miceller kan kerne-tværbundes af dithioler, resulterer i bio-reversible disulfidbindinger. På grund af en forskel i redoxpotentiale, disulfider anses for at være stabile ekstracellulært, mens de hurtigt reduceres til frie dithioler intracellulært, hvilket fører til en opløsning af bæresystemet og frigivelse af lasten.
"På denne måde en række nanobærere med forskellige funktioner bliver let tilgængelige fra en enkelt blokcopolymer og et meget selektivt postpolymerisationstrin. Denne modulære tilgang til nanopartikler med forskellig funktion og morfologi adresserer vigtige spørgsmål med god sammenlignelighed, såsom indflydelsen af størrelse og form på in vivo cirkulationstider, biodistribution, tumor ophobning, celleoptagelse og terapeutisk respons, da det samme udgangsmateriale anvendes, " siger Matthias Barz.
De første in vivo eksperimenter har allerede vist, at disse kernestabiliserede micellære nanobærere udviser stabil cirkulationsadfærd, hvilket indikerer, at interaktioner med serumkomponenter eller blodkar er fraværende. Kun ved at sikre, at der ikke forekommer uspecifikke interaktioner inden for de komplekse biologiske omgivelser, cellulær optagelse i ønskede specifikke cellepopulationer synes mulig. Det terapeutiske potentiale af den beskrevne nanopartikelplatform vil blive yderligere undersøgt med hensyn til immunterapi af malignt melanom i SFB 1066.
 Varme artikler
Varme artikler
-
 Klemt mellem superledere, grafen vedtager eksotiske elektroniske tilstandeMIT -fysikere har fundet ud af, at en flage grafen, når de bringes tæt på med to superledende materialer, kan arve nogle af disse materialers supraledende kvaliteter. Da grafen er klemt mellem superle
Klemt mellem superledere, grafen vedtager eksotiske elektroniske tilstandeMIT -fysikere har fundet ud af, at en flage grafen, når de bringes tæt på med to superledende materialer, kan arve nogle af disse materialers supraledende kvaliteter. Da grafen er klemt mellem superle -
 Metalblæk kunne lette vejen mod fleksible elektroniske bøger, viserForskere rapporterer udviklingen af en ny metalblæk lavet af små kobberplader, der kan bruges til at skrive en funktion, fleksibelt elektrisk kredsløb på almindeligt printerpapir. Deres rapport om d
Metalblæk kunne lette vejen mod fleksible elektroniske bøger, viserForskere rapporterer udviklingen af en ny metalblæk lavet af små kobberplader, der kan bruges til at skrive en funktion, fleksibelt elektrisk kredsløb på almindeligt printerpapir. Deres rapport om d -
 Vand, vand - de to typer flydende vandKredit:George Hodan/public domain Der er to typer flydende vand, ifølge forskning udført af et internationalt videnskabeligt samarbejde. Denne nye ejendommelighed føjer til den voksende liste over
Vand, vand - de to typer flydende vandKredit:George Hodan/public domain Der er to typer flydende vand, ifølge forskning udført af et internationalt videnskabeligt samarbejde. Denne nye ejendommelighed føjer til den voksende liste over -
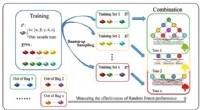 Forskere foreslår maskinlæringsmetode til 2-D materialespektroskopiGrundlæggende arkitektur for indlæringsproceduren i random forest-metoden. Kredit:SIOM Machine learning er en vigtig gren inden for kunstig intelligens. Dens grundlæggende idé er at bygge en stati
Forskere foreslår maskinlæringsmetode til 2-D materialespektroskopiGrundlæggende arkitektur for indlæringsproceduren i random forest-metoden. Kredit:SIOM Machine learning er en vigtig gren inden for kunstig intelligens. Dens grundlæggende idé er at bygge en stati
- Droneobservation gør kortvarigt fly i Frankfurt lufthavn
- Hvorfor skruer vi ned for radioen, når de gik tabt?
- Saturn overgår Jupiter efter opdagelsen af 20 nye måner - og du kan hjælpe med at navngive dem
- Solbrint:Fotoanoder lover høj effektivitet
- Tidlig eksponering for banker påvirker livslang økonomisk sundhed
- Showtime for Stadia skyspiltjeneste


