Målretningsstrategi kan åbne døren til bedre kræfttilførsel
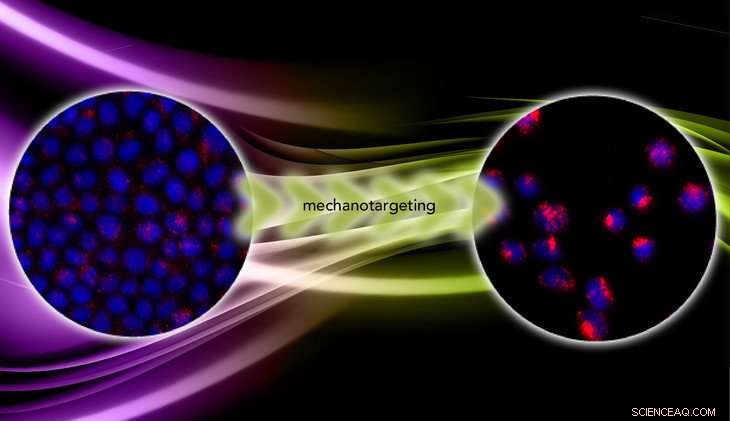
I overgangen fra godartet til ondartet, kræftceller går fra stive til bløde. Mechanotargeting udnytter mekanikken til at forbedre målretningseffektiviteten af nanpartikelbaserede terapeutiske midler. Kredit:Zhang lab/vecteezy.com
Bioingeniører kan muligvis bruge de unikke mekaniske egenskaber af syge celler, såsom metastatiske kræftceller, at hjælpe med at forbedre leveringen af lægemiddelbehandlinger til de målrettede celler, ifølge et team af forskere ved Penn State.
Mange laboratorier rundt om i verden udvikler nanopartikel-baserede, lægemiddelleveringssystemer til selektivt at målrette tumorer. De er afhængige af et nøgle-og-lås-system, hvor proteinnøgler på overfladen af nanopartiklerne klikker ind i låsene af et højt udtrykt protein på overfladen af kræftcellen. Cellemembranen vikler derefter nanopartiklerne og indtager den. Hvis der indtages nok af nanopartiklerne og deres medikamentlast, kræftcellen vil dø.
Låsens og nøglens klæbekraft er det, der driver nanopartiklerne ind i cellen, sagde Sulin Zhang, professor i ingeniørvidenskab og mekanik.
"Det er næsten universelt, at når der er en drivkraft for en proces, der er altid en modstandskraft, " sagde Zhang. "Her, drivkraften er biokemisk - protein-protein-interaktionen."
Modstandskraften er den mekaniske energiomkostning, der kræves for, at membranen kan vikle sig rundt om nanopartiklerne. Indtil nu, bioingeniører overvejede kun drivkraften og designede nanopartikler for at optimere de kemiske interaktioner, en målretningsstrategi kaldet "kemotargeting". Zhang mener, at de også bør tage hensyn til cellernes mekanik for at designe nanopartikler for at opnå forbedret målretning, som danner en ny målretningsstrategi kaldet "mechanotargeting".
"Disse to målretningsstrategier er komplementære; du kan kombinere kemotargeting og mekanotargeting for at opnå det fulde potentiale af nanopartikel-baserede diagnostiske og terapeutiske midler, " sagde Zhang. "Faktum er, at målretningseffektivitet kræver en delikat balance mellem drivkræfter og modstandskræfter. For eksempel, hvis der er for mange taster på nanopartikeloverfladen, selvom disse nøgler kun svagt interagerer med de ikke-matchende låse på normale celler, disse svage, interaktioner uden for målet kan stadig give tilstrækkelig adhæsionsenergi til, at nanopartiklerne kan trænge ind i cellemembranen og dræbe de raske celler."
På den anden side, hvis adhæsionsenergien ikke er høj nok, nanopartiklerne kommer ikke ind i cellen.
I "Mechanotargeting:Mekanikafhængig cellulær optagelse af nanopartikler, " offentliggjort online forud for tryk i tidsskriftet Avancerede materialer , Zhang og holdet rapporterer resultaterne af eksperimenter på kræftceller dyrket på hydrogeler med variabel stivhed. På bløde hydrogeler forblev cellerne sammenhængende og godartede og oplevede en næsten konstant stress, der begrænsede optagelsen af nanopartiklerne. Men på stive hydrogeler blev cellerne metastatiske og antog en tredimensionel form, tilbyde mere overfladeareal for nanopartikler at klæbe, og blev mindre stresset. Under denne betingelse, cellerne optog fem gange antallet af nanopartikler som de godartede celler.
"Nanopartiklerne er fluorescerende, så vi tæller antallet af nanopartikler, der kommer ind i cellen ved hjælp af fluorescensintensiteten. Vi fandt ud af, at i de ondartede celler er intensiteten fem gange højere, " sagde Zhang. "Det beviser, at mechanotargeting virker."
 Varme artikler
Varme artikler
-
 Universal transistor tjener som grundlag for at udføre enhver logisk funktionDen rekonfigurerbare transistors kerne består af en nanotrådstruktur indlejret i en siliciumdioxidskal. Elektroner eller huller strømmer fra kilden i den ene ende af nanotråden gennem to porte til afl
Universal transistor tjener som grundlag for at udføre enhver logisk funktionDen rekonfigurerbare transistors kerne består af en nanotrådstruktur indlejret i en siliciumdioxidskal. Elektroner eller huller strømmer fra kilden i den ene ende af nanotråden gennem to porte til afl -
 Hurtigt roterende kugler viser nanoskala systemhemmelighederMagnetiske partikler i mikronstørrelse er sat til at gå på tur i en brugerdefineret rig, der bruges af Rice University til at studere virkningerne af et roterende magnetfelt på materialer. Kredit:Jeff
Hurtigt roterende kugler viser nanoskala systemhemmelighederMagnetiske partikler i mikronstørrelse er sat til at gå på tur i en brugerdefineret rig, der bruges af Rice University til at studere virkningerne af et roterende magnetfelt på materialer. Kredit:Jeff -
 Nanosvampe opsuger olie igen og igenDen superhydrofobe carbon nanorørsvamp viser en bemærkelsesværdig evne til at opsuge olie fra vand. Forskere fandt ud af, at tilføjelse af bor til vækstprocessen skaber kovalente bindinger i nanorøren
Nanosvampe opsuger olie igen og igenDen superhydrofobe carbon nanorørsvamp viser en bemærkelsesværdig evne til at opsuge olie fra vand. Forskere fandt ud af, at tilføjelse af bor til vækstprocessen skaber kovalente bindinger i nanorøren -
 Hall-fejls afsløringer rejser forhåbninger om 2-D materialerScanning af elektronmikroskopbillede af en 2D Hall-enhed med fire par elektroder for at teste fire forskellige geometrier med en 2D InAs-prøve. Kredit:Adam Micolich En af de første ting, folk gør,
Hall-fejls afsløringer rejser forhåbninger om 2-D materialerScanning af elektronmikroskopbillede af en 2D Hall-enhed med fire par elektroder for at teste fire forskellige geometrier med en 2D InAs-prøve. Kredit:Adam Micolich En af de første ting, folk gør,
- Skru op for varmen for at skabe nye nanostrukturerede metaller
- Rumprøver forbinder NASAs Apollo 11 og Mars 2020
- Nebulær hypotese
- Hvordan man skriver en testbar hypotese
- Der er 8 millioner grunde til, at du skal være ligeglad, hvis Magic Leap lykkes
- Den asymmetriske syntese af halogenerede forbindelser fra carboxylsyrer er verdensførste


