Udvikling af en 3-D kollagenmodel til at teste magnetisk assisteret osteogenese in vitro

a) Mikrostruktur af cellefyldte kollagen stilladser undersøgt under TEM. Celler er omgivet af kollagenmatrixen. Kollagenfibrillerne viste ingen foretrukken retning omkring cellerne under kontrolforhold, b) IONP'er kan identificeres i kollagenmatrixen og c) tæt på cellemembranerne. Efter 14 dage blev en ny matrix syntetiseret af cellerne, d) uden SMF'er og e) med SMF'er. Begge tilstande førte til ny matrixsyntese efter 14 dage, uden væsentlig forskel. Kredit: Videnskabelige rapporter , doi:10.1038/s41598-018-33455-2.
De cellulære og molekylære mekanismer af magnetisk stimulations-baseret knogleregenerering kræver yderligere forståelse på nuværende tidspunkt. For at evaluere fænomenet i laboratoriet, en tredimensionel (3-D) naturlig kollagenmodel blev for nylig udviklet via plastisk kompression for at producere en cellulær, tæt og mekanisk stærk kollagenstruktur. For at producere celleladede modeller i undersøgelsen, Zhiyu Yuan og kolleger inkorporerede osteoblastceller (MG-63 cellelinje) og magnetiske jernoxidnanopartikler (IONP'er) i kollagengelerne. Ved at bruge 3D-print, en magnetisk bioreaktor blev designet og fremstillet til at understøtte cellevækst under statiske magnetiske felter (SMF'er). Ved hjælp af polymerasekædereaktion (PCR), forskerne fastslog SMF'ers indvirkning på regulering og ekspression af gener relateret til osteogenese, herunder runt-relateret transkriptionsfaktor 2 (Runx2), osteonectin (ON) og knoglemorfogenetiske proteiner 2 og 4 (BMP-2 og BMP-4).
Nu udgivet i Videnskabelige rapporter , resultaterne viste, at SMF'er, IONP'er og kollagenmatrixen var i stand til at stimulere spredningen, produktion af alkalisk fosfatase og mineralisering af osteoblaster. Processen blev aktiveret ved at påvirke matrix-celle-interaktioner til at påvirke ekspressionen af Runx2, PÅ, BMP-2 og BMP-4. Kollagenmodellen tilbød indsigt i progressivt at danne en ny mineraliseret 3-D knoglemodel og forstå magnetisk stimulering på osteogenese. Yderligere undersøgelser kan udføres med modellen til anvendelser inden for vævsteknologi og regenerativ medicin.
Alene i Storbritannien, antallet af patienter, der lider af knoglebrud, har en væsentlig økonomisk indvirkning på livskvaliteten, hvilket fremgår af omkostningerne til National Health Services (NHS). Under knogleskade, den biologiske og mekaniske proces med fysiologisk regenerering erstatter den skadede knogle med ny knogle på skadestedet. Den metaboliske proces er kompliceret og kræver interaktion af mange faktorer, herunder vækst- og differentieringsfaktorer såsom hormoner, cytokiner og ekstracellulære komponenter; i mellemtiden kan utilstrækkelige eller afbrudte faktorer føre til forsinket heling eller svækket/ikke-sammenføjning af knogler.
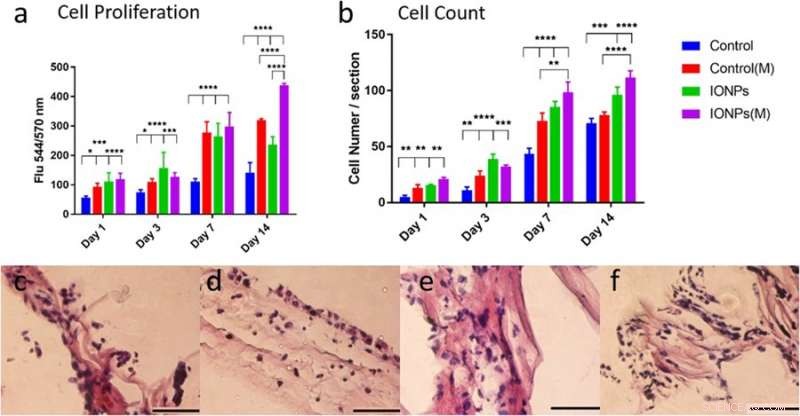
a) sammenligning af MG-63-celleproliferation, når den dyrkes med/uden inkorporering af IONP'er med eksponering af SMF'er (M) og uden eksponering af SMF'er. Celleproliferation kan forbedres med SMF'er ved at inkorporere IONP'er, angiver en stimulerende effekt, b) Sammenligning af celleantallet af MG-63-cellelinjerne fra histologibilleder med eller uden SMF'er. De cellulære responser af MG-63-cellelinjen dyrket på PC-kollagenstillads blev også undersøgt via histologi for betingelser c) uden SMF'er og uden IONP'er, d) med SMF'er, e) med IONP'er og e) at kombinere SMF'er og IONP'er. Kredit: Videnskabelige rapporter , doi:10.1038/s41598-018-33455-2.
I undersøgelsen, forfatterne brugte en roman, multifunktionel biomimetisk 3-D kollagenmodel til brug som en in vitro platform til undersøgelse af mekanismer for magnetisk stimulering ved osteogenese. For at producere en række celleladede modeller, forskerne introducerede interne stimuli (jernoxidnanopartikler) og eksterne (statiske magnetfelter, SMF'er) stimuli ind i systemet. Det biomimetiske materiale blev konstrueret ved fremstilling af nano- og mikrostrukturer ved hjælp af plastisk kompression, i henhold til en tidligere fastsat protokol. For at evaluere osteoblasters biologiske adfærd, herunder deres spredning, differentiering, mineralisering, genekspression og mikrostrukturanalyse, forskerne dyrkede kollagenmodellen i en magnetisk bioreaktor i op til 42 dage.
I undersøgelsen, celleproliferation af osteoblastcellelinjen MG-63 blev vurderet ved anvendelse af alamarBlue-assayet. På dag 14, forskerne observerede en signifikant forskel mellem SMF'er alene, IONP'er alene og i deres kombination på celleproliferation. Histologi teknikker blev anvendt til at undersøge cellulære reaktioner inden for collagen stilladser og forstå SMFs og IONPs rolle på celleproliferation. Visualisering blev efterfulgt af kvantitativ analyse af celletal, resultater indikerede, at inkorporering af IONP'er forlængede effekten af SMF'er.
Tilsvarende celledifferentiering blev observeret med alkalisk fosfatase (ALP) aktiviteter for kollagen stilladser, med eller uden inkorporering af IONP'er. Som før, når effekten af IONP'er og SMF'er blev kombineret, blev ALP-produktionen signifikant stimuleret sammenlignet med behandling med SMF'er alene og IONP'er alene. Cellemineralisering blev også observeret derefter og kvantificeret i det celle-frøede kollagen stillads. Efter 42 dage blev alle prøver farvet med ARS-farvning for at angive fuldstændig mineralisering. I modsætning, kombination af SMF'er og IONP'er var ikke i stand til at fremme mineralisering.
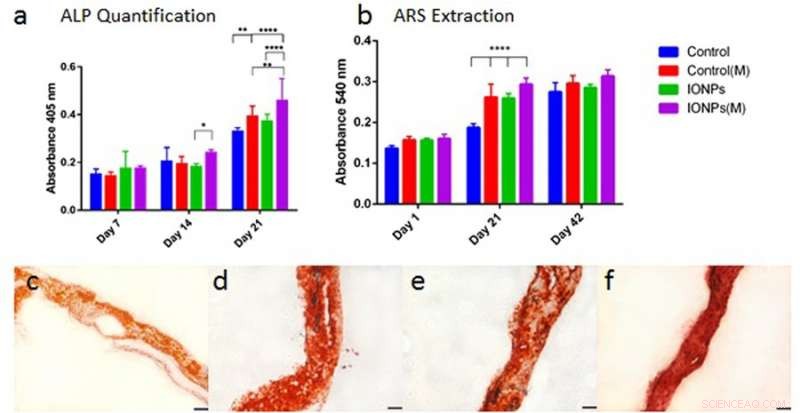
a) sammenligning af ALP-produktion af MG-63-cellelinje, når den dyrkes i kollagen-stilladser med eller uden inkorporering af IONP'er, med eksponering for SMF'er (M) og uden eksponering for SMF'er. b) Sammenligning af cellemineralisering ved at ekstrahere og kvantificere ARS-farvning fra stilladser behandlet med eller uden SMFs eksponering. Cellefyldte kollagen stilladser blev integreret med IONP'er (100 µg/ml) resultater blev indsamlet på tværs af 1, 21 og 42 dages kultur. c) ARS -farvning af kollagenstillads i fravær af SMF'er og IONP'er, d) med SMF'er, e) med IONP'er, og f) med SMF'er og IONP'er. Kredit: Videnskabelige rapporter , doi:10.1038/s41598-018-33455-2.
Derefter, forskerne gennemførte undersøgelser for at forstå reaktioner fra celle-frø kollagen stilladser på SMF'er og IONP'er på molekylært niveau. For det, ekspressionsniveauerne for Runx2, PÅ, BMP-2 og BMP-4 blev kvantificeret ved hjælp af kvantitativ polymerasekædereaktion i realtid (RT-qPCR). En 7-dages behandling af SMF'er alene havde ikke en effekt på ekspressionen af Runx2, der henviser til, at øget ekspression blev fundet, når SMF'er blev kombineret med IONP'er, demonstrerer kollagenmatrix -medieret Runx2 -ekspression under osteogenese. På dag 7 blev niveauet af ON -ekspression i prøverne behandlet med IONP'er, SMF'er og begge var højere end i kontrollen inden for en kort periode. Under ekspressionen af BMP-2 og BMP-4, lignende resultater blev observeret over 7-14 dage.
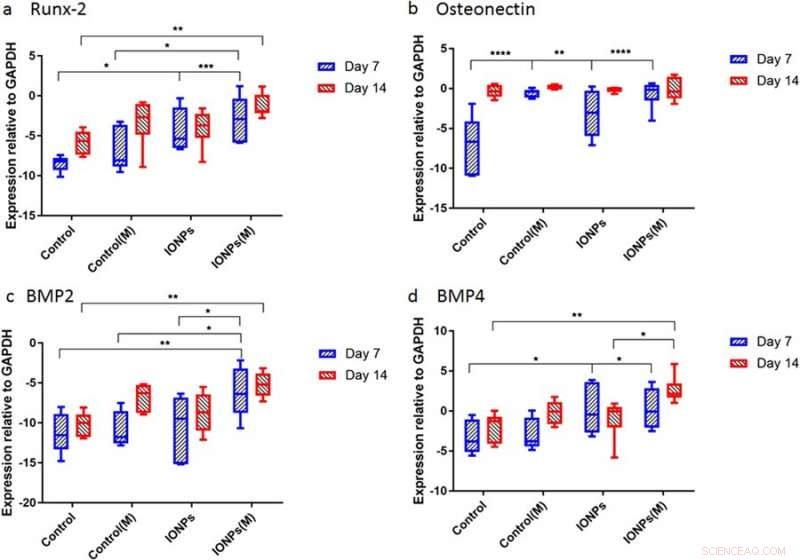
Genekspression for a) Runx2, b) osteonectin (ON), c) BMP-2 og d) BMP-4 normaliseret med kontrol-GAPDH efter 7 og 14 dages cellekultur. Kredit: Videnskabelige rapporter , doi:10.1038/s41598-018-33455-2.
Undersøgelsen demonstrerede hovedsageligt osteogenese som en kompleks proces medieret af successiv aktivering og ekspression af flere nøglegener, herunder Runx2, PÅ, BMP-2 og BMP-4. Typisk, Runx2 opregulerer ekspressionen af proteingener relateret til knoglematricen for at fremme knogledannelse in vitro og in vivo. Derfor, undersøgelsen viste, at SMF-eksponering kan få cellelinjen til at proliferere ved at modulere tidlig ekspression af Runx2, at fremskynde osteogenese. Da IONP'er blev indarbejdet under SMF'er, ekspressionen af osteonectin (ON) genet steg, forbinder kollagenfaser med knoglemineral for at starte normal skeletvævsmineralisering. Tilsvarende både BMP-2 og BMP-4 blev kun øget i undersøgelsen under kombineret cellekultur med SMF'er og IONP'er.
På denne måde forfatterne udviklede og testede en biomimetisk 3-D kollagenmodel, der gradvist kunne mineraliseres til efterfølgende at danne en ny knoglemodel in vitro. Modellen blev inkorporeret med osteoblastceller og nanopartikler med evnen til at reagere på eksterne magnetiske stimulationer. Den biomimetiske kollagenmodel blev konstrueret via plastisk kompression til at integrere MG-63-cellelinjen og demonstrere reproducerbare og konsistente resultater kombineret med SMF'er og IONP'er. Celle-matrix-interaktionerne opregulerede med succes ekspressionen af nøglegener relateret til osteogenese. Forfatterne har til hensigt at udvikle 3-D-modellen yderligere for at tjene som en overlegen platform til at undersøge biologisk adfærd in vitro med potentielle anvendelser inden for vævsteknologi og regenerativ medicin.
© 2018 Science X Network
 Varme artikler
Varme artikler
-
 Miljøvenlig produktion af silicium nanotrådeDisse silicium nanotråde blev opnået ved hjælp af en ny miljøvenlig metode udviklet af russiske videnskabsmænd. Giftig flussyre erstattes af uskadelig ammoniumfluorid. Kredit:Kirill Gonchar Fysike
Miljøvenlig produktion af silicium nanotrådeDisse silicium nanotråde blev opnået ved hjælp af en ny miljøvenlig metode udviklet af russiske videnskabsmænd. Giftig flussyre erstattes af uskadelig ammoniumfluorid. Kredit:Kirill Gonchar Fysike -
 Nanoteknologi sætter gang i energilagring på papir og kludBing Hu, en post-doc stipendiat i Yi Cuis forskningsgruppe ved Stanford, forbereder en lille firkant af almindeligt papir med en blæk, der vil afsætte nanorør på overfladen, som derefter kan oplades m
Nanoteknologi sætter gang i energilagring på papir og kludBing Hu, en post-doc stipendiat i Yi Cuis forskningsgruppe ved Stanford, forbereder en lille firkant af almindeligt papir med en blæk, der vil afsætte nanorør på overfladen, som derefter kan oplades m -
 Ny tilgang forbedrer grafen-baserede superkondensatorerEn effektiv vej til at forbedre ydeevnen af superkondensatorer. Kredit:Dawei Su Efterspørgslen efter integrerede energilagringsenheder vokser hurtigt, efterhånden som folk stoler mere og mere på
Ny tilgang forbedrer grafen-baserede superkondensatorerEn effektiv vej til at forbedre ydeevnen af superkondensatorer. Kredit:Dawei Su Efterspørgslen efter integrerede energilagringsenheder vokser hurtigt, efterhånden som folk stoler mere og mere på -
 Kulstof nanorør højttalere kunne være drevet af lasere, Forvandl støjende rum til fredelige hell…Nanorørenheden bruger et princip, der først blev identificeret af Alexander Graham Bell. (PhysOrg.com) -- Et UT Dallas teams undersøgelse offentliggjort i Journal of Applied Physics udvider nano
Kulstof nanorør højttalere kunne være drevet af lasere, Forvandl støjende rum til fredelige hell…Nanorørenheden bruger et princip, der først blev identificeret af Alexander Graham Bell. (PhysOrg.com) -- Et UT Dallas teams undersøgelse offentliggjort i Journal of Applied Physics udvider nano


