Skæve mikrokapsler frigiver last ved lavere osmotiske tryk, der kræves til lægemiddellevering

Mikrokapsler med skaller af varierende tykkelse (rød) kan stabilt indkapsle last og frigive den ved præcist kalibreret, lavt osmotisk tryk, tillader sikker levering af lægemidler og andre stoffer inde i den menneskelige krop. Kredit:Wyss Institute ved Harvard University
At knække et æg for at frigøre dets blommer kræver ydre kraft (som at blive slået mod kanten af en skål) for at overvinde styrken af æggeskallen. Tilsvarende at levere mikrokapselholdige terapeutiske biomolekyler til den menneskelige krop kræver, at deres beholdere brydes, efter at de er blevet injiceret, så lasten kan leveres på det rigtige sted på det rigtige tidspunkt. En række eksterne stimuli kan bruges til at udløse frigivelsen af indkapslede molekyler, en af de nemmeste er osmotisk tryk, da det blot kræver indføring af vand for at få mikrokapslerne til at svulme og briste. Imidlertid, for at skabe nok indre tryk til at bryde kapselskallen, store mængder af et osmotisk middel skal tilsættes til mikrokapslen for at tiltrække vandet, og det resulterende høje sprængtryk kan beskadige væv eller forårsage blodpropper.
En løsning på denne anstødssten er nu blevet udviklet af forskere ved Harvard's Wyss Institute for Biologically Inspired Engineering og John A. Paulson School of Engineering and Applied Sciences (SEAS), som udtænkte en måde at skabe mikrokapsler med skaller af ujævn tykkelse, der tillader dem at briste ved lavere osmotisk tryk, gør dem mere sikre til brug i den menneskelige krop. Forskningen er publiceret i Lille .
"Vores skallers svageste del er 40 gange tyndere end deres stærkeste del, hvilket gør det meget lettere for dem at bryde og frigive deres last, " sagde førsteforfatter Weixia Zhang, Ph.D., en postdoc ved Wyss Institute og SEAS. "På bagsiden, disse mikrokapsler er ekstremt holdbare og lækker ikke, hvis de ikke udsættes for forhøjet osmotisk tryk, gør dem meget stabile og i stand til at opbevare deres indhold i lang tid."
For at fremstille deres inhomogene mikrokapsler, forskerne brugte en glaskapillær mikrofluidisk enhed, der brugte en vand-i-olie-i-vand-metode til at indkapsle en vandopløsning indeholdende saccharose, et osmotisk middel, i en skal af monomerer suspenderet i olie. Når monomererne udsættes for UV-lys, de reagerer med hinanden og tværbinder for at danne et fast stof, polymerskal omkring saccharoseopløsningen. Ved at variere de hastigheder, hvormed saccharoseopløsningen "last" og monomerolie-"skallen" strømmer gennem anordningen, holdet opdagede, at de kunne introducere variationer i tykkelsen af de skaller, der blev dannet, skabe skæve kapsler med tykkere vægge på den ene side og tyndere på den anden.
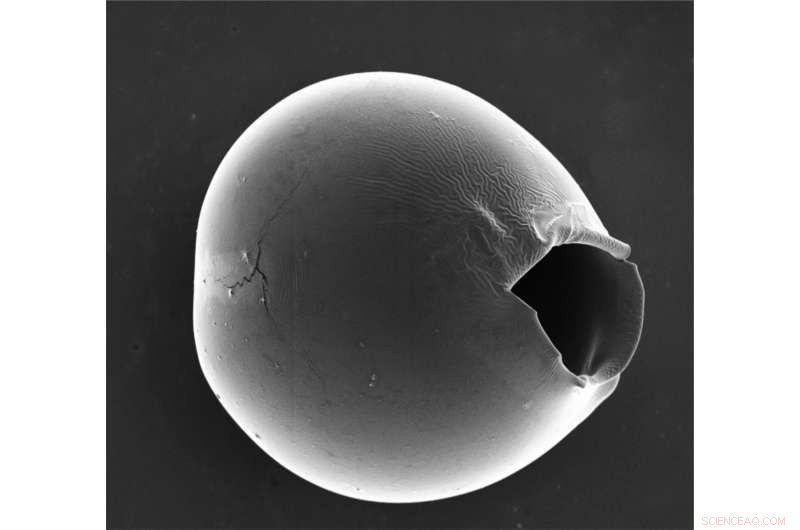
Mikrokapslerne brister i den tyndeste del af skallen, efterlader en åbning på ti mikrometer i størrelse, der tillader de fleste biomolekyler og lægemidler at blive frigivet. Kredit:Wyss Institute ved Harvard University
Forskerne udsatte derefter deres mikrokapsler for osmotisk shock ved at tilsætte vand, som diffunderede ind i mikrokapslerne og fik dem til at svulme op på den tyndeste del af skallen. Efter cirka 20-30 minutter, den fortyndede skal revnede, dannede en åbning, der var titusvis af mikrometer stor, som er stor nok til, at de fleste biomolekyler og nanomaterialer kan frigives med succes. Forøgelse af forskellen mellem den tyndeste og den tykkeste del af skallen førte til et større antal sprængte mikrokapsler, bekræfter, at graden af inhomogenitet påvirkede effektiviteten af godsfrigivelsen.
"At være i stand til at skabe mikrokapsler med høj grad af inhomogenitet ved at ændre skaltykkelsen under fremstillingsprocessen og frigive lasten med meget mindre osmotisk tryk, åbner op for en ny anvendelse i kontrolleret frigivelse, hvilket er meget vigtigt for lægemiddellevering i medicin, såvel som andre områder, " sagde co-first forfatter Liangliang Qu, Ph.D., en postdoc ved Wyss Institute og SEAS.
For at teste mikrokapslernes holdbarhed, holdet indkapslede en fluorescerende polymer i dem og målte ændringen i fluorescerende intensitet i deres kerner over tid. De observerede ingen ændring i intensitet i 30 dage efter indkapsling, demonstrerer, at mikrokapslerne beholdt deres last uden at lække. Desuden, polymerens størrelse er meget mindre end de fleste biomolekyler, såsom antistoffer og enzymer, tyder på, at skallerne kunne bruges til at beskytte og opbevare biomolekyler eller lægemidler i længere perioder.
Endelig, forskerne co-indkapslede en protease (et enzym, der nedbryder proteiner) og saccharose i deres mikrokapsler i 37 dage, derefter påført osmotisk shock for at udløse frigivelsen af deres indhold. Proteasen bibeholdt 91% af sin oprindelige aktivitet, demonstrerer, at denne opbevaringsmetode ikke væsentligt forringede dens biologiske funktion.
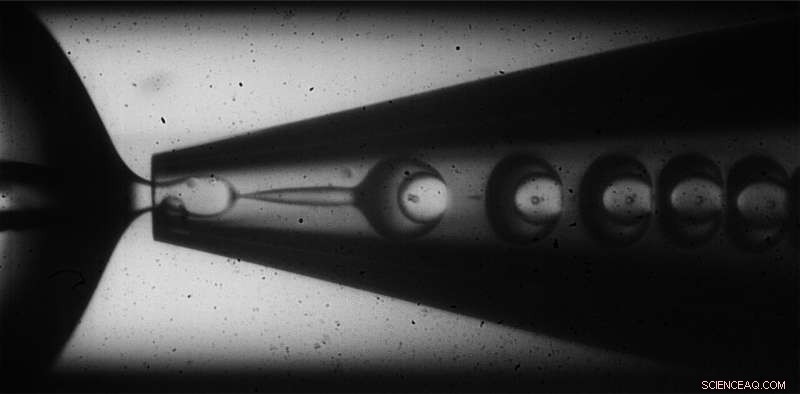
Mikrokapslerne er fremstillet ved hjælp af en olie-i-vand-i-olie-teknik, der opnår inhomogen skaltykkelse ved at variere strømningshastighederne af skal- og lastmaterialerne. Kredit:Wyss Institute ved Harvard University
"Sammenlignet med andre styrede frigivelsesbærere, såsom celler, nanopartikler, eller vesikler, dette system er meget alsidigt, stabil, og kan tilpasses, gør det til et attraktivt alternativ til sikker og effektiv levering af lægemidler og andre biomolekyler til menneskers sundhed og andre applikationer, " sagde den tilsvarende forfatter David Weitz, Ph.D., et kernefakultetsmedlem ved Wyss Institute, som også er Mallinckrodt-professor i fysik og anvendt fysik ved SEAS.
Holdet fortsætter med at udvikle deres mikrokapsler ved at optimere skalmaterialet for yderligere at reducere det osmotiske tryk, der kræves for at sprænge dem. De planlægger først at anvende deres teknologi til levering af lægemidler, såsom terapeutiske antistoffer, med det mål at kunne bruge menneskekroppens høje vandindhold til at fungere som brududløser efter injektion.
"Dette projekt er et godt eksempel på, hvordan enklere løsninger ofte kan være bedre end komplicerede, da det eneste input, der er nødvendigt for at sprænge mikrokapslerne, er mekanisk tryk, snarere end komplekse kemier eller molekylære switches, " sagde medforfatter Donald Ingber, M.D., Ph.D., hvem er Wyss Institutes stiftende direktør, Judah Folkman professor i vaskulær biologi ved HMS og Vascular Biology Program på Boston Children's Hospital, og professor i bioingeniør ved SEAS.
 Varme artikler
Varme artikler
-
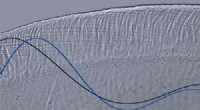 Nanopores ligger til grund for vores evne til at stille ind på en enkelt stemmeDette optiske mikroskopbillede viser bølgebevægelse i et tværsnit af tektorialmembranen, del af det indre øre. Denne membran er en gel i mikroskala, mindre i bredden end et enkelt menneskehår, og det
Nanopores ligger til grund for vores evne til at stille ind på en enkelt stemmeDette optiske mikroskopbillede viser bølgebevægelse i et tværsnit af tektorialmembranen, del af det indre øre. Denne membran er en gel i mikroskala, mindre i bredden end et enkelt menneskehår, og det -
 Brug naturen til at producere et revolutionerende optisk materialeEt internationalt team af forskere har rapporteret om en ny måde at beskytte droner, overvågningskameraer og andet udstyr mod laserangreb, som kan deaktivere eller ødelægge udstyret. Kredit:Pexels
Brug naturen til at producere et revolutionerende optisk materialeEt internationalt team af forskere har rapporteret om en ny måde at beskytte droner, overvågningskameraer og andet udstyr mod laserangreb, som kan deaktivere eller ødelægge udstyret. Kredit:Pexels -
 Grafen i nul G lover succes i rummetFlyet, hvor Flagship-forskere udførte et eksperiment i mikrotyngdekraft. Drives af Novespace, flyet laver særlige manøvrer for at skabe nulgravitationsforhold inde i flyet Kredit:Graphene Flagship
Grafen i nul G lover succes i rummetFlyet, hvor Flagship-forskere udførte et eksperiment i mikrotyngdekraft. Drives af Novespace, flyet laver særlige manøvrer for at skabe nulgravitationsforhold inde i flyet Kredit:Graphene Flagship -
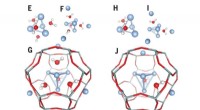 Forskere opdager, hvorfor sølvklynger udsender lysForskningen gav afgørende bevis for, at kun små klynger af fire sølvatomer i form af et tetraeder og omgivet af vandmolekyler udsender lys (se blå pyramideform i figuren). Kredit:© KU Leuven Klyng
Forskere opdager, hvorfor sølvklynger udsender lysForskningen gav afgørende bevis for, at kun små klynger af fire sølvatomer i form af et tetraeder og omgivet af vandmolekyler udsender lys (se blå pyramideform i figuren). Kredit:© KU Leuven Klyng
- Hvordan det gamle land Blob Gondwana blev dagens kontinenter
- Gårdafstrømning og den forværrede algepest
- Tavlecomputerlærer er international konferencestjerne
- Utrolig vision i ældgamle havdyr drev et evolutionært våbenkapløb
- Sådan kalibreres en WeighMax-skala
- Narrativ tilgang kan ændre mening om børnepasningsudgifter


