Katalytisk immunterapi til cancer:Nanopartikler fungerer som kunstige enzymer
Kredit:Wiley
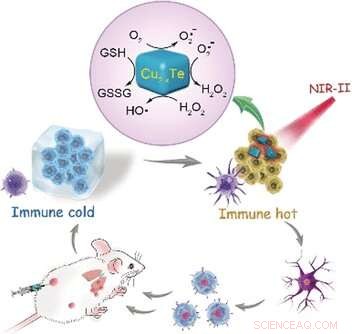
Teoretisk set, vores immunsystem kunne opdage og dræbe kræftceller. Desværre, tumorer er godt bevæbnet til at bekæmpe disse angreb. På trods af moderne kræftbehandlinger, metastaser og tilbagefald er fortsat et stort problem. Øget antitumorimmunitet kan nu blive muliggjort, takket være kobbertellurid-nanopartikler, der efterligner enzymer, især under NIR-II lysbestråling. Dette inducerer oxidativt stress i tumorceller, ophævelse af deres immunsuppressive status og udløser inflammatoriske processer, som kinesiske videnskabsmænd rapporterer i tidsskriftet Angewandte Chemie .
Såkaldte nanoenzymer er varme kandidater til behandlinger kaldet katalytisk immunterapi. Disse nanopartikler har strukturer helt anderledes end biologiske enzymer, men efterligner enzymernes katalytiske aktivitet. De er lettere at tilberede end naturlige enzymer, samt at være billigere og mere stabil.
Forskere, der arbejder med Wansong Chen og You-Nian Liu ved Central South University (Changsha, Hunan, Kina) har nu introduceret et nyt nanoenzym:kobbertellurid-nanopartikler (Cu2-xTe) efterligner aktiviteterne af enzymerne glutathionoxidase og peroxidase. Aktiviteten af dette nanoenzym skyldes kobberionerne, som skifter mellem to oxidationstilstande. Substratet er glutathion, en antioxidant, der findes i væsentligt højere koncentrationer i tumorceller end i raske. Det er derfor, nanoenzymerne kun er aktive i tumorceller. Ud over, de absorberer NIR-II-lys (nær-infrarødt lys med en bølgelængde mellem 1000 og 1350 nm), får deres lokale miljø til at varme op. Denne effekt øger kraftigt nanoenzymernes enzymlignende aktivitet. I behandling, NIR-II-bestrålingen kunne selektivt påføres tumoren.
Eksperimenter i tumorcellekulturer og med tumorbærende mus viste, at brugen af nanoenzymer og NIR-II-bestråling udløser en hel kaskade af cellulære responser, der i høj grad øger det oxidative stress i tumoren, som i sidste ende fører til celledød. På samme tid, undertrykkelsen af immunologiske processer i mikromiljøet omkring tumoren ophæves. I stedet, stoffer, der fremmer inflammation, frigives, og et immunrespons udløses. Dette understøttes af den forhøjede koncentration af effektor-T-celler, som forskerne har observeret. Immunsystemet er således i stand til at lære at forsvare sig mod metastaser og at opbygge en "immunologisk hukommelse" for at forhindre tilbagefald.
 Varme artikler
Varme artikler
-
 Nanoprintede optiske lineære perceptroner med høj neurondensitet udfører nær-infrarød inferens …Kredit:CC0 Public Domain I dag, maskinlæring gennemsyrer hverdagen, med millioner af brugere, der hver dag låser deres telefoner op gennem ansigtsgenkendelse eller passerer gennem AI-aktiverede au
Nanoprintede optiske lineære perceptroner med høj neurondensitet udfører nær-infrarød inferens …Kredit:CC0 Public Domain I dag, maskinlæring gennemsyrer hverdagen, med millioner af brugere, der hver dag låser deres telefoner op gennem ansigtsgenkendelse eller passerer gennem AI-aktiverede au -
 Supersolder udviser uovertrufne termiske egenskaberPh.D. studerende Wei Gong og lektor i maskinteknik Sheng Shen i laboratoriet. Kredit:College of Engineering, Carnegie Mellon University Inden for elektronik, loddemetal bruges til at forbinde to d
Supersolder udviser uovertrufne termiske egenskaberPh.D. studerende Wei Gong og lektor i maskinteknik Sheng Shen i laboratoriet. Kredit:College of Engineering, Carnegie Mellon University Inden for elektronik, loddemetal bruges til at forbinde to d -
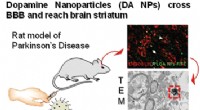 Nanopartikelmedicin vender Parkinsons-lignende symptomer hos rotterNår babyboomerne bliver ældre, Antallet af mennesker med diagnosen Parkinsons sygdom forventes at stige. Patienter, der udvikler denne sygdom, begynder normalt at opleve symptomer omkring 60 år eller
Nanopartikelmedicin vender Parkinsons-lignende symptomer hos rotterNår babyboomerne bliver ældre, Antallet af mennesker med diagnosen Parkinsons sygdom forventes at stige. Patienter, der udvikler denne sygdom, begynder normalt at opleve symptomer omkring 60 år eller -
 Gyldent køretøj til medicinafgivelse har skjulte omkostningerJeremy Larson (til venstre) maler en prøve for at teste for hormonproduktion med sine rådgivere Michael Carvan, lektor i ferskvandsvidenskab (center), og Reinhold Hutz, professor i biologiske videnska
Gyldent køretøj til medicinafgivelse har skjulte omkostningerJeremy Larson (til venstre) maler en prøve for at teste for hormonproduktion med sine rådgivere Michael Carvan, lektor i ferskvandsvidenskab (center), og Reinhold Hutz, professor i biologiske videnska
- 3 innovationer, der hjælper de hjemløse i Eugene, Oregon
- Hvordan memer bruger humor til at miskreditere afroamerikansk engelsk
- Billede:Sagaing Division i det nordvestlige Myanmar
- Som plastfolie, nyt biomateriale kan dække vanskelige forbrændingssår og blokere infektion
- Hvordan er skoven påvirket af surregn?
- Liste over indfødte stammer fra 1500 til 1600


