Jernselenid kvanteprikker til in vivo multifoton biomedicinsk billeddannelse
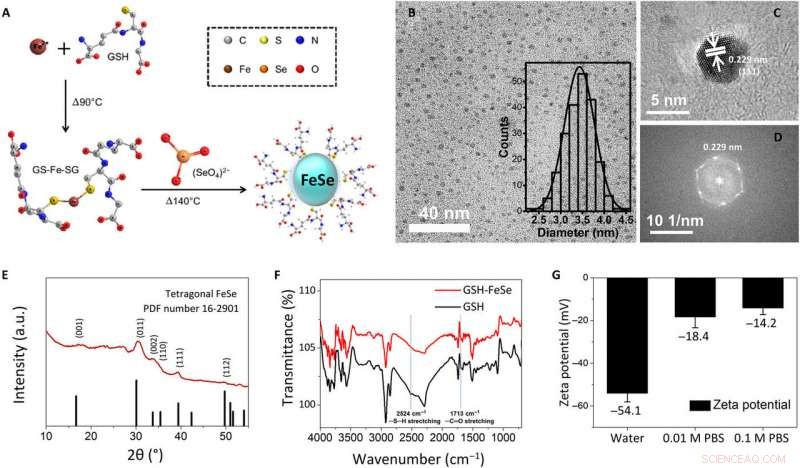
Fysisk-kemisk karakterisering af one-pot-syntetiserede vandopløselige FeSe QD'er. (A) Skematisk illustration af one-pot synteseproceduren for GSH-kapslede FeSe QD'er, (B) lysfelt TEM-billede (indsat:histogram over størrelsesfordeling), (C) TEM-billede i høj opløsning, (D) hurtig Fourier-transformation af TEM-billede i høj opløsning, (E) GIXRD mønstre, (F) FTIR-spektre, og (G) zeta-potentiale af FeSe QD'er. a.u., vilkårlige enheder. Kredit:Science Advances, doi:10.1126/sciadv.aay0044
Fotoluminescerende sonder med høj biokompatibilitet, kvanteudbytte og multifotonabsorptionsydelse er af væsentlig interesse i biomedicinsk billeddannelse, forventes at opnå forbedret penetrationsdybde og rumlig opløsning. Jærnselenid (FeSe) kvantepunkter (QD'er) rapporteres at opfylde disse kriterier baseret på en ny rapport offentliggjort i Videnskabens fremskridt af J. Kwon og et team af forskere i de tværfaglige afdelinger for kemi, Biomaterialevidenskab og Cogno-Mechantronics Engineering i Korea og Kina. Kvanteprikker er nanometerskala luminescerende halvlederkrystaller med unikke kemiske og fysiske egenskaber i forhold til deres struktur og sammensætning.
De syntetiske QD'er i denne undersøgelse kan udvise to- og tre-foton excitationsegenskaber ved 800- og 1800 nm bølgelængder med et højt kvanteudbytte (40 procent) til billeddannelse i andet vindue. Materialerne var også biokompatible og verificeret af Kwon et al. da de koblede poly(ethylenglycol)-konjugerede QD'er med human epidermal vækstfaktor receptor 2 (HER2) antistoffer til in vitro og in vivo to-foton billeddannelse. Forskerne har med succes afbildet overfladerne i en dybde på op til 500 µm fra hudoverfladen ved hjælp af en ikke -lineær femtosekundlaser ved en excitationsbølgelængde på 800 nm. Resultaterne kan åbne en ny vej til at bruge biokompatible FeSe QD'er til multiphoton -vævsbilleddannelse under sygdomsdiagnose.
Chalcogenider af overgangsmetal er attraktive på tværs af en række forskningsområder inden for nanovidenskab med anvendelser som magnetiske halvledere, superledere, solceller, elektrokatalysatorer, sensorer og kvanteprikker. Lagdelte jernbaserede materialer er lovende superlederkandidater med lav toksicitet og pris, med uventet høj superledende overgangstemperatur. Jernchalcogenidmaterialer kan blive fluorescerende nanohalvledere, når deres dimensioner reduceres til nul. Disse har unikke optoelektroniske egenskaber, der er relevante i biologisk billeddannelse og solenergikonvertering. Fluorescerende biomedicinsk billeddannelse med halvledende nanokrystaller er en lovende detektionsteknik på grund af høj fotostabilitet og afstemning af nanokrystallerne under absorptions- og emissionsspektre sammenlignet med konventionelle organiske farvestoffer. QD'er kan også udvise multiphoton-eksiteret fotoluminescens (PL), hvor en luminofor samtidigt kan absorbere mere end to fotoner via en virtuel tilstand for at udsende synligt lys.
Fænomenet kan tillade større penetrationsdybde for reduceret vævsautofluorescens og spredning med fordele for in situ biomedicinsk fluorescensbilleddannelse under cancerkirurgi. Forskere ser derfor multifotonmikroskopi (MPM) som en ikke-invasiv, in vivo, værktøj til billeddannelse af dybt væv. I nærværende undersøgelse, Kwon et al. blev motiveret af forudgående arbejde med at syntetisere biokompatible QD'er med to- og tre-foton luminescerende egenskaber ved hjælp af jern (Fe) og selen (Se) elementer. Generelt, de to (Fe- og Se-prækursorer) forekommer naturligt i menneskekroppen og udviser lav toksicitet i nanopartikelform. Forskerholdet testede in vitro tumorcellemålretningsspecificitet med humaniseret monoklonalt HER2 (human epidermal vækstfaktor receptor 2) antistof - konjugeret jernselenid (FeSe) kvanteprikker (anti-HER2-QD'er). Til in vitro-forsøg, de brugte en HER2-overudtrykt MCF-7 (Michigan Cancer Foundation) xenograft-model (podninger fra en anden donorart) af brystkræftcellelinje. De udførte derefter in vivo MPM (multifotonmikroskopi) billeddannelse i en levende xenograft-model af human brysttumor.
For at udvikle de vandopløselige FeSe QD'er, forskerne brugte en one-pot syntetisk strategi. De dannede QD'er, der tilnærmelsesvis var 3,4 ± 0,3 nm i størrelse og observerede dem ved hjælp af lysfelttransmissionselektronmikroskopi (TEM). Brug af højopløselige TEM- og elektrondiffraktionsmønstre for QD'er, de observerede planet af tetragonal FeSe. Forskerne brugte strukturanalyse med et røntgendiffraktionsspektrometer (GIXRD) og røntgenfotoelektronspektroskopi for omhyggeligt at bevise morfologien af FeSe QD'er. Zeta-potentiale test viste, at FeSe QD'er opløstes i deioniseret vand og i 0,01 M samt 0,1 M phosphat-buffer (PBS) saltvand. Når Kwon et al. overvågede dem ved hjælp af et digitalkamera og fluorescerende mikroskopi efter fem dage, QD'erne aggregerede ikke eller adskilte sig i fluorescens. Båndgabet af FeSe QD'er tilnærmelsesvis 2,44 eV fra det ultraviolette til det synlige (UV-Vis) spektrum.
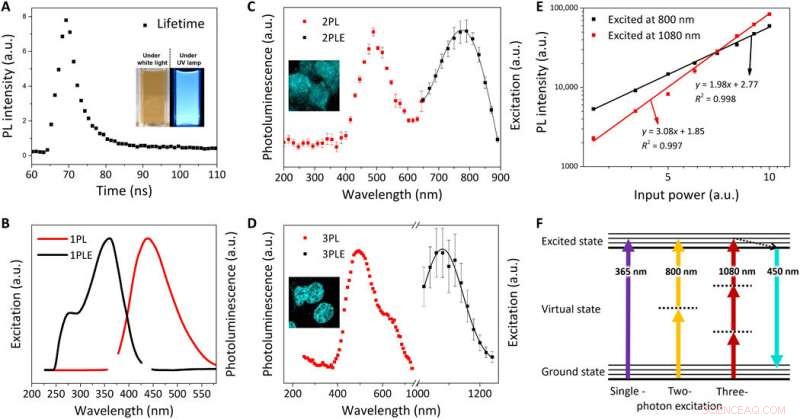
Optisk karakterisering af FeSe QD'er. (A) PL-levetid (τ) for FeSe QD'er ved en excitationsbølgelængde på 380 nm; indsat:digitale billeder af FeSe-dispersion under hvidt lys og UV-lampe (λex =365 nm). Normaliseret PL excitation (PLE) spektrum (sort linje) og PL spektrum (rød linje) ved λem på 440 nm og λex af (B) 365 nm for 1PL, (C) 800 nm for 2PL, og (D) 1080 nm for 3PL. (E) Effektafhængighed af PL-intensitet for 2PL (sort firkant) og 3PL (rød firkant). Hældningen af den effektafhængige funktion er 1,98 og 3,08 for 2PL og 3PL, henholdsvis. (F) Jablonski diagram af enkelt-, to-, og tre-foton luminescens. Kredit:Science Advances, doi:10.1126/sciadv.aay0044
Kwon et al. undersøgte fotoluminescensegenskaberne (PL) af FeSe QD'er ved 25 grader C for at observere en levetid på 3,23 nanosekunder (ns). De bemærkede en to-foton (2PL) og tre-foton (3PL) exciterede PL, efterfulgt af repræsentative fluorescensmikroskopiske billeder af MCF27-celler farvet med FeSe QD'er fra 2PL og 3PL. Denne multifoton excitationsegenskab er bemærkelsesværdig for bioimaging med en længere bølgelængde, der kan trænge igennem en maksimal vævsdybde med reduceret fototoksicitet, observeret inden for det "gyldne vindue" under billeddannelse af hjernevæv.
Forskerholdet testede først QD-indflydelse på cellelevedygtighed, før de anvendte FeSe QD'er til bioimaging-eksperimenter. De brugte forskellige cellelinjer dyrket med forskellige koncentrationer af FeSe QD'er ved forskellige kulturvarigheder og observerede fremragende levedygtighed med syv dage, med> 75 procent cellelevedygtighed. Ved hjælp af fluorescensmikroskopiske billeder af cellekulturerne, Kwon et al. registrerede den overlegne biokompatibilitet af FeSe QD'er, hvor kvanteprikkerne ikke forstyrrede cellevækst. For yderligere at minimere uspecifik binding under samlingen, forskerne indkapslede FeSe QD'er med poly(ethylenglycol) (PEG) før konjugering med HER2-antistoffer for at udvikle anti-HER2-PEG-QD'er.
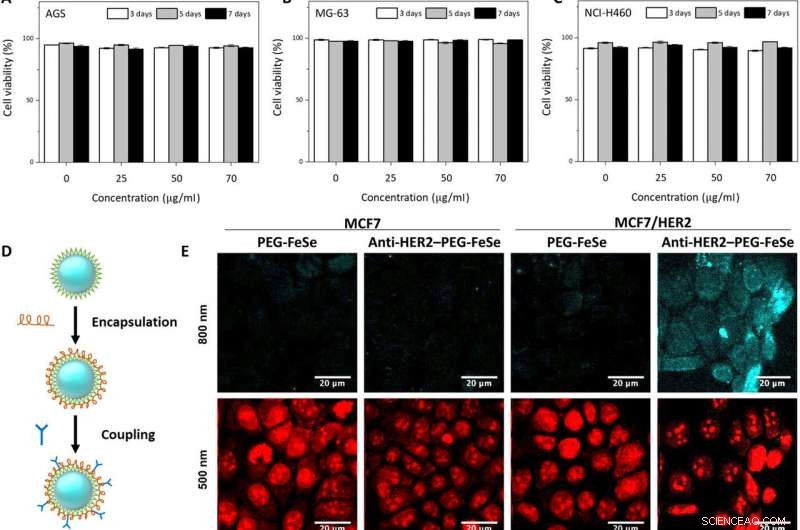
In vitro og in vivo to-foton mikroskopisk billeddannelse af FeSe QD'er målrettet mod brysttumor. Flowcytometri -evaluering af levedygtigheden af (A) AGS, (B) MG-63, og (C) NCI-H460-celler udsat for QD'er i forskellige koncentrationer (0, 25, 50, og 70 μg ml−1) for 3, 5, og 7 dage. (D) Konjugationsprocedure til fremstilling af anti-HER2-PEG-QD'er. (E) In vitro to-foton mikroskopisk billeddannelse af MCF7 og HER2-overudtrykte MCF7-celler (MCF7/HER2) farvet med PEG-belagte FeSe QD'er eller anti-HER2-konjugerede PEG-QD'er (anti-HER2-PEG-QD'er, 2 μg ml−1), hvor kernerne blev farvet med propidiumiodid, og cellemembranen og cellekernerne blev afbildet ved λex på 800 og 500 nm. Lasereffekt =40 mW ved brændplanet. (F) Sammenligning af fotostabiliteten af QD'er og rhodamin 6G (Rh6G) i deioniseret vand under to-foton excitation (λex =800 nm, lasereffekt =50 mW), hvor relativ PL-intensitet blev overvåget i 30 min. (G) Digitalt fotografi af tumor xenograft til in vivo billeddannelse. (H) MPM-system. CH PMT, kanal fotomultiplikator rør; OPO, optisk parametrisk oscillator. (I) In vivo MPM-billeder før og efter anti-HER2-QD-injektion og (J) in vivo MPM-billeder ved forskellige brændvidder (450 til 500 μm). Målestænger, 20 μm. Kredit:Science Advances, doi:10.1126/sciadv.aay0044
Holdet testede den uspecifikke optagelse og selektivitet af konjugaterne under målretning af humane brystkræftceller via propidiumiodidfarvning. Anti-HER2-PEG-QD'erne målrettede specifikt HER2-receptorerne, hvilket angiver potentialet for at bruge PEGylerede QD'er som billeddannelsesmidler in vivo. De fysiologisk stabile molekyler bibeholdt deres optiske egenskaber i syv dage i serum og i en række forskellige bufferopløsninger. FeSe QD'erne var meget fotostabile under to-foton excitation med yderligere egenskaber egnet til biologisk billeddannelse og langsigtet sporing af målrettede celler.
Undersøgelsen gav et nyt perspektiv på diagnosen brystkræft. Brystkræft er den næsthøjeste årsag til kræftdød for kvinder, med betydelige gentagelsesrater, hvor minimalt invasiv kirurgi assisteret med sansnings- og billeddannelsesteknikker er afgørende for at identificere sygdommen. Forskerholdet etablerede en in vivo MPM (multifotonmikroskopi) billeddannelsesmetode med intravenøs injektion af anti-HER2-PEG-QD'er i en MCF xenograft dyremodel. De etablerede derefter en subkutan xenograft-musemodel af brystkræft ved at injicere MCF7-celler og MCF/HER2-celler i flanken af mus. Efter fire uger, når tumorvolumenet nåede 200 mm 3 , forskerne injicerede 100 µL anti-HER2-PEG-QD'er og observerede FeSe QD'erne som et magentasignal. De opnåede derefter 2PL-signaler i forskellige dybder på tværs af tumorområdet med regelmæssige intervaller. Det anden harmoniske generations (SHG) signal syntes blåt at repræsentere kollagen i det overfladiske område, og forskerne skelnede PL-signalet fra QD'er nær brystkræftcellerne.
På denne måde J. Kwon og kolleger syntetiserede biokompatible FeSe QD'er med stærk cellelevedygtighed ved øgede QD-koncentrationer. Holdet brugte QD'er under to- og tre-foton-fluorescensbilleddannelse og med multifoton-billeddannelse i en dybde på op til 500 µm til at overvåge tumorceller med en ikke-lineær femtosekundlaser i levende dyr in vivo. De kombinerede biokompatible FeSe QD'er og multifoton-billeddannelse kan åbne en ny metode til at realisere ikke-invasiv in situ bioimaging inden for levende individer.
© 2019 Science X Network
 Varme artikler
Varme artikler
-
 Tredimensionelt kulstof bliver metalliskDette viser 3D Metallic carbon med sammenlåsende sekskanter. Kredit:Qian Wang, Ph.d. En teoretisk, tredimensionel (3D) form for kulstof, der er metallisk under omgivende temperatur og tryk, er ble
Tredimensionelt kulstof bliver metalliskDette viser 3D Metallic carbon med sammenlåsende sekskanter. Kredit:Qian Wang, Ph.d. En teoretisk, tredimensionel (3D) form for kulstof, der er metallisk under omgivende temperatur og tryk, er ble -
 Fysikere styrer lysspredning i grafenEn flage af grafen blev dyrket på kobber og overført til et isolerende substrat af siliciumdioxid. Fermi-energien i grafenen blev justeret ved at variere gate-spændingen på den overliggende iongel, so
Fysikere styrer lysspredning i grafenEn flage af grafen blev dyrket på kobber og overført til et isolerende substrat af siliciumdioxid. Fermi-energien i grafenen blev justeret ved at variere gate-spændingen på den overliggende iongel, so -
 Ikke længere kun en tilskuer, siliciumoxid kommer ind i elektronikken på computerchipsComputerchips indeholder siliciumoxid, et stof, som videnskabsmænd engang betragtede som en ren isolator, men som nu ser ud til at være en aktiv del af elektroniske processer, der driver mobiltelefone
Ikke længere kun en tilskuer, siliciumoxid kommer ind i elektronikken på computerchipsComputerchips indeholder siliciumoxid, et stof, som videnskabsmænd engang betragtede som en ren isolator, men som nu ser ud til at være en aktiv del af elektroniske processer, der driver mobiltelefone -
 Kemikere rapporterer om ny indsigt om egenskaber af stof på nanoskalaEn væske med en viskositet som vand trænger ind i UCLA-R3, hvor dens viskositet på nanoskala bliver som honning. Kredit:Xing Jiang, Miguel García-Garibay/UCLA Kemi og Biokemi UCLA nanovidenskabsfo
Kemikere rapporterer om ny indsigt om egenskaber af stof på nanoskalaEn væske med en viskositet som vand trænger ind i UCLA-R3, hvor dens viskositet på nanoskala bliver som honning. Kredit:Xing Jiang, Miguel García-Garibay/UCLA Kemi og Biokemi UCLA nanovidenskabsfo
- Krymper et medicinsk laboratorium for at passe på en fingerspids
- Et nyt skridt i retning af at bruge grafen i elektroniske applikationer
- Sådan lavede guldfeberprospektører det originale smarte køleskab
- Ny svovldioxidomdannelsesmetode kan ændre nuværende industrielle teknikker
- Både den berømte Hope -diamant og British Crown Jewel -diamanter, kan være superdyb
- Undersøgelse af gamle klipper tyder på iltsvind i havene førte til ende-trias masseudryddelse


