Hvorfor binder hospitalskim sig stærkere til visse overflader end til andre?
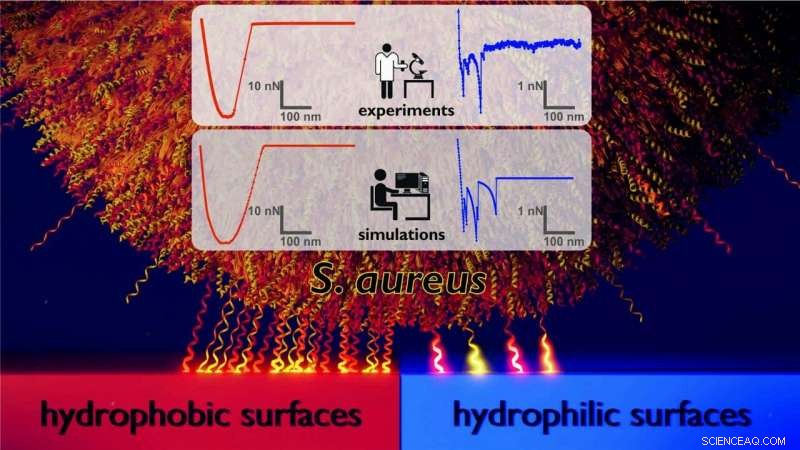
Model af den adhæsionsmekanisme, hvorved bakterien Staphylococcus aureus binder sig til hydrofobe ('lav-energi') overflader (venstre) sammenlignet med hydrofile ('høj-energi') overflader (højre). Til venstre, et stort antal cellevægsmolekyler (vist her som bittesmå komprimerbare fjedre) er involveret i at binde cellen til den hydrofobe overflade. På den hydrofile overflade vist til højre, langt færre molekyler er involveret. Resultaterne blev opnået af et team af eksperimentelle og teoretiske fysikere ved Saarland University, som udførte beregningsmæssige Monte Carlo-simuleringer af kraft-afstandsdata fra atomkraftmikroskopi-eksperimenter. Kredit:Saarlands Universitet
Resultater fra undersøgelser i både eksperimentel og teoretisk fysik kan være med til at forbedre antibakterielle overflader. Forskningsarbejdet blev for nylig offentliggjort i tidsskriftet Nanoskala .
Staphylococcus aureus bakterier er en af de mest almindelige årsager til infektioner erhvervet af patienter under et ophold på hospitalet. Disse patogener er særligt problematiske, fordi de kan danne robuste biofilm på både naturlige og kunstige overflader, hvorfra de er meget svære at fjerne. "De enkelte bakterier i disse biofilm er effektivt beskyttet mod angreb fra antibiotika eller af det menneskelige immunsystem. Det er derfor, det kan være så farligt, når disse bakterier koloniserer medicinske implantater, da de så kan forårsage alvorlige postoperative infektioner, " forklarer Karin Jacobs, Professor i eksperimentel fysik ved Saarlands Universitet. Det er derfor afgørende at forsøge at forhindre, at disse biofilm dannes i første omgang.
Imidlertid, at være i stand til at påvirke biofilmvækst, forskerne skulle forstå de mekanismer, hvorved bakterierne klæber til forskellige materialer. Ved hjælp af et scannende atomkraftmikroskop, de pressede de små bakterieceller på forskellige typer overflader og bestemte derefter den kraft, der var nødvendig for at løfte de vedhæftede celler fra overfladen. Denne eksperimentelle konfiguration gjorde det muligt for forskerne at registrere, hvad der er kendt som kraft-afstandskurver. "Vi brugte ekstremt glatte siliciumoverflader som modeloverflader. I et sæt eksperimenter, siliciumoverfladerne blev forberedt således, at de havde høj vandbefugtningsevne; i et andet sæt eksperimenter blev de behandlet til at være yderst hydrofobe. Vi var i stand til at vise, at bakteriecellerne klæbte langt stærkere til de hydrofobe overflader, hvorfra vandet simpelthen rullede af, end på de hydrofile (vandbefugtelige) overflader, " forklarer Karin Jacobs.
Men det er ikke kun størrelsen af kræfterne, der adskiller sig mellem de to overfladetyper, det samme gør formerne på kraft-afstandskurverne (se figur). "På de hydrofobe overflader, vi ser meget glatte kurver med en karakteristisk skålform. På de hydrofile overflader, i modsætning, vi observerer kraft-afstandskurver med en meget takket profil, siger professor Jacobs.
For at forstå disse resultater, dynamikken i disse komplekse systemer blev modelleret ved hjælp af Monte Carlo-simuleringer, der blev udført i forskningsgruppen ledet af professor Ludger Santen, Professor i teoretisk fysik ved Saarlands Universitet. Modellen behandler bakteriecellen som en stiv kugle og molekylerne i cellevæggen, der binder cellen til overfladen som små fjedre. "Det viser sig, at for at reproducere de eksperimentelle resultater, den rolle, som den tilfældige (stokastiske) karakter af den molekylære bindingsproces spiller, er vigtigere end at forsøge at øge modellens kompleksitet. Vi har nu afdækket, hvorfor bakteriecellerne opfører sig så forskelligt på forskellige typer overflader. På hydrofobe overflader, et stort antal af cellevægsproteinerne klæber til overfladen, hvilket resulterer i en stærk bindingskraft og giver en jævn kraft-afstandskurve, " forklarer Ludger Santen.
I modsætning, på en hydrofil overflade, langt færre cellevægsproteiner er involveret i at binde bakterien til overfladen. Som resultat, bakterierne holdes mindre stærkt på overfladen, og formen på kraft-afstandskurven er mindre ensartet. "Den takkede form af kurverne, som vi ser med hydrofile overflader, er forårsaget af nogle få individuelle cellevægsmolekyler, når de trækkes fra overfladen. Fordi færre cellevægsproteiner er involveret, bakterierne binder sig mindre stærkt til hydrofile overflader, siger Erik Maikranz, som udførte Monte Carlo-simuleringerne som en del af sit doktorgradsforskningsarbejde.
På grund af de forskellige former for kraft-afstandskurverne, fysikerne antager, at der på en hydrofil overflade er færre cellevægsproteiner involveret i bindingsprocessen, fordi disse molekyler først skal overvinde en potentiel barriere, hvilket effektivt reducerer antallet af proteinmakromolekyler, der kan binde cellen til overfladen. "Den potentielle barriere for vedhæftning på hydrofile overflader er relativt høj, så kun få af cellevægsproteinerne er i stand til at overvinde denne energibarriere på et bestemt tidspunkt. På hydrofobe overflader, imidlertid, barrieren er ubetydelig lille, så mange cellevægsproteiner kan klæbe direkte til overfladen, " forklarer Dr. Christian Spengler, som udførte forsøgene i undersøgelsen.
Sidste artikelDyrkning af metalliske krystaller i flydende metal
Næste artikelNy fotoresist muliggør 3D-print af mindste porøse strukturer
 Varme artikler
Varme artikler
-
 Kemikere rapporterer om ny indsigt om egenskaber af stof på nanoskalaEn væske med en viskositet som vand trænger ind i UCLA-R3, hvor dens viskositet på nanoskala bliver som honning. Kredit:Xing Jiang, Miguel García-Garibay/UCLA Kemi og Biokemi UCLA nanovidenskabsfo
Kemikere rapporterer om ny indsigt om egenskaber af stof på nanoskalaEn væske med en viskositet som vand trænger ind i UCLA-R3, hvor dens viskositet på nanoskala bliver som honning. Kredit:Xing Jiang, Miguel García-Garibay/UCLA Kemi og Biokemi UCLA nanovidenskabsfo -
 Elektrokemi til gavn for fotonik:nanorør kan styre laserimpulserKredit:Skolkovo Institut for Videnskab og Teknologi Et internationalt hold af forskere ledet af forskere fra Laboratory of Nanomaterials ved Skoltech Center for Photonics and Quantum Materials (CP
Elektrokemi til gavn for fotonik:nanorør kan styre laserimpulserKredit:Skolkovo Institut for Videnskab og Teknologi Et internationalt hold af forskere ledet af forskere fra Laboratory of Nanomaterials ved Skoltech Center for Photonics and Quantum Materials (CP -
 Grafen plasmoner bliver ballistiskeSimulering og observationer af formerende plasmoner i bornitrid-heterostruktur. Kredit:ICFO At klemme lys ind i små kredsløb og kontrollere dets strøm elektrisk er en hellig gral, der er blevet et
Grafen plasmoner bliver ballistiskeSimulering og observationer af formerende plasmoner i bornitrid-heterostruktur. Kredit:ICFO At klemme lys ind i små kredsløb og kontrollere dets strøm elektrisk er en hellig gral, der er blevet et -
 Quantum dot LED'er bliver lysere, mere effektivtRød, grøn, og blå QLEDer, med de påførte spændinger i øverste venstre hjørne. Den grønne QLED har en luminans på 168, 000 candela per kvadratmeter, hvilket er mere end tre gange højere end den tidlige
Quantum dot LED'er bliver lysere, mere effektivtRød, grøn, og blå QLEDer, med de påførte spændinger i øverste venstre hjørne. Den grønne QLED har en luminans på 168, 000 candela per kvadratmeter, hvilket er mere end tre gange højere end den tidlige
- Sådan rebrander du en fisk, så den lyder mere velsmagende
- Genopretning af coronavirus:hvorfor lokale markeder er nøglen til at genoplive vores aflåste bycen…
- Konvertering af biomasse ved at anvende mekanisk kraft
- Efter coronavirus, universiteter skal samarbejde med lokalsamfund for at støtte social omstilling
- Frisk antimaterialeundersøgelse vil styrke fremtidige indirekte søgninger efter mørkt stof
- En lange to dage:Stor storm støder nordøst med sne


