Nyt nanoteknologisk design giver håb om personlig vaccination til behandling af kræft
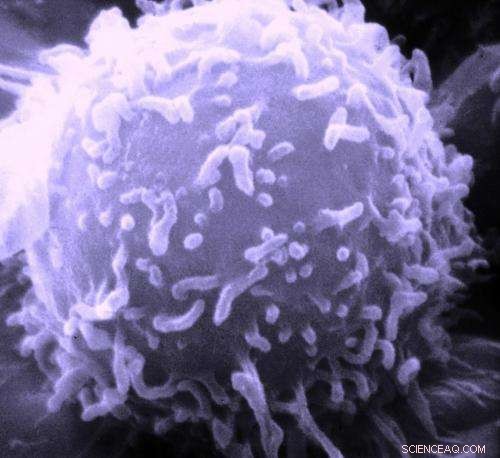
Elektronmikroskopisk billede af en enkelt human lymfocyt. Kredit:Dr. Triche National Cancer Institute
En af de vigtigste udfordringer i at udvikle effektive, målrettede kræftbehandlinger er kræftcellernes heterogenitet. Denne variation gør det svært for immunsystemet at genkende, reagere på og aktivt bekæmpe tumorer. Nu, imidlertid, nye fremskridt inden for nanoteknologi gør det muligt at levere målrettede, personlige "vacciner" til behandling af kræft.
En ny undersøgelse, offentliggjort den 2. oktober, 2020 i Videnskabens fremskridt , demonstrerer brugen af ladede metal-organiske rammer i nanoskala til at generere frie radikaler ved hjælp af røntgenstråler i tumorvæv til at dræbe kræftceller direkte. Desuden, de samme rammer kan bruges til at levere immunsignalmolekyler kendt som PAMP'er til at aktivere immunresponset mod tumorceller. Ved at kombinere disse to tilgange til én let administreret "vaccine, "denne nye teknologi kan give nøglen til bedre lokal og systemisk behandling af svære at behandle kræftformer.
I et samarbejde mellem Lin Group i University of Chicago Department of Chemistry og Weichselbaum Lab ved University of Chicago Medicine, forskerholdet kombinerede ekspertise fra uorganisk kemi og cancerbiologi for at tackle det udfordrende problem med korrekt målretning og aktivering af et medfødt immunrespons mod cancer. Dette arbejde udnyttede de unikke egenskaber ved metal-organiske rammer i nanoskala, eller nMOF'er - strukturer i nanoskala bygget af gentagne enheder i en gitterformation, der er i stand til at infiltrere tumorer.
Disse nMOF'er kan bestråles med røntgenstråler for at generere høje koncentrationer af frie oxygenradikaler, dræber kræftcellerne direkte og producerer antigener og inflammatoriske molekyler, der hjælper immunsystemet med at genkende og fjerne kræftceller, meget som en vaccine. Deres gitterlignende struktur gør også nMOFs ideelle transportører til at levere anti-cancer-lægemidler direkte til tumorer. Så langt, imidlertid, det har været vanskeligt at aktivere medfødte og adaptive immunresponser, der er nødvendige for at eliminere kræftsvulster.
I denne nye undersøgelse, forskerne finjusterede deres tilgang yderligere. Denne gang, de genererede en ny type nMOF-struktur, der kunne lades med lægemidler kendt som patogen-associerede molekylære mønstre, eller PAMP'er. Nu, når nMOF'erne blev anvendt på kræftsvulster, bestråling af vævet havde en dobbelt effekt:det udløste nMOF'erne til at dræbe lokale kræftceller for at producere antigener mod tumoren og frigav PAMP'erne, som derefter udløste en meget stærkere aktivering af immunresponset på tumorantigener. Dette en-to slag var i stand til at dræbe både tyktarms- og bugspytkirtelkræftceller med høj effektivitet, selv i tumormodeller, der er meget resistente over for andre former for immunterapi.
I yderligere forsøg med mus, efterforskerne så, at de kunne udvide virkningerne af nMOF'erne selv til fjerne tumorer med anvendelse af checkpoint-hæmmere, giver nyt håb for behandling af kræft både lokalt og systemisk med denne tilgang.
"Ved at inkludere PAMP-levering med nMOF'erne, det er første gang, vi virkelig var i stand til at forbedre immunresponset på antigenerne, " sagde seniorforfatter Wenbin Lin, Ph.D., James Franck professor i kemi og en primær efterforsker af tumorimmunologi ved Ludwig Cancer Center ved UChicago. "Dette er helt anderledes end alle vores tidligere undersøgelser, fordi vi har vist, at nMOF'erne plus PAMP'er kan påvirke alle de aspekter, der kræves for at aktivere immunsystemet. Vi kan bruge denne nanoformulering til at muliggøre personlige kræftvaccinationer, der vil virke på enhver patient , fordi denne strategi ikke vil være underlagt den heterogenitet, vi ser blandt forskellige patienter."
Effekterne af behandlingen var så udtalte, at forskerne er ivrige efter at bringe teknologien til kliniske forsøg, hvor andre versioner af nMOF-teknologien allerede er ved at blive testet, med lovende resultater indtil videre.
"Det her system er todelt, " sagde medforfatter Ralph Weichselbaum, MD, Daniel K. Ludwig Distinguished Service Professor i stråling og cellulær onkologi og formand for afdelingen for stråling og cellulær onkologi ved UChicago. "Først, det kan forbedre lokal tumorkontrol ved at øge røntgenstrålernes dræbende kraft. Sekund, mens der har været interesse for at bruge stråling til at stimulere immunresponset til at bekæmpe kræft, det har vist sig at være sværere, end vi troede. I dette tilfælde, nMOF'erne er i stand til at aktivere det medfødte og adaptive immunsystem, hvilket gør denne teknologi meget lovende til behandling af kræft i klinikken."
Ser allerede frem til næste skridt, efterforskerne arbejder på at forfine teknologien. "Vi forfiner designet af nMOF og dets levering af PAMP'erne, som forberedelse til at teste det på mennesker, " sagde Lin. "Vi arbejder virkelig på at zoome ind på den bedste formulering, så vi kan få dette ind i kliniske forsøg, forhåbentlig inden for de næste to til tre år, eller endnu før."
Holdet krediterer den tværfaglige og kollaborative karakter af UChicago og University of Chicago Medicines Hyde Park campus for at skabe et rum, hvor kemi og kræftbiologi er kombineret for at producere en så lovende potentiel terapi, samt den støtte, de har modtaget fra Ludwig Cancer Research undervejs.
"Fra idéen om dette projekt og få det finansieret til at starte med kliniske forsøg, hvor vi er i stand til at teste teknologien i kliniske forsøg og få rigtige patientdata, alt dette arbejde er blevet udført lige her på UChicago, " sagde Weichselbaum. "Vi går virkelig fra at opdage noget i laboratoriet til at teste det ved sengen."
 Varme artikler
Varme artikler
-
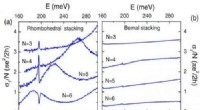 Infrarød absorption forstærket af lagdeling af ark af grafenDen infrarøde absorption på grund af både elektroniske overgange og fononer i få-lags (3 til 6 lag) grafenprøver med rhombohedral (venstre) og Bernal (højre) lagstabling. Det meget asymmetriske fononb
Infrarød absorption forstærket af lagdeling af ark af grafenDen infrarøde absorption på grund af både elektroniske overgange og fononer i få-lags (3 til 6 lag) grafenprøver med rhombohedral (venstre) og Bernal (højre) lagstabling. Det meget asymmetriske fononb -
 Nanomedicinsk aktiveringsprofil bestemmer effektiviteten afhængigt af tumor c-Myc-ekspressionFig. 1:Forskellig lægemiddelfrigivelsesprofil afhængig af linkeren anvendt til blok-copolymerer af nano-miceller FR-JQ1H/m med alifatisk aldehydlinker:Hurtig lægemiddelfrigivelse i gradvist forhøjet s
Nanomedicinsk aktiveringsprofil bestemmer effektiviteten afhængigt af tumor c-Myc-ekspressionFig. 1:Forskellig lægemiddelfrigivelsesprofil afhængig af linkeren anvendt til blok-copolymerer af nano-miceller FR-JQ1H/m med alifatisk aldehydlinker:Hurtig lægemiddelfrigivelse i gradvist forhøjet s -
 Forskere skaber vaskbar sensor, der kan væves i materialerUBC -doktorand Hossein Montazerian ser nærmere på en lille sensor indlejret i en fiber. Kredit:UBCO Okanagan Glem det smarte ur. Tag den smarte skjorte på. Forskere ved UBC Okanagans School of En
Forskere skaber vaskbar sensor, der kan væves i materialerUBC -doktorand Hossein Montazerian ser nærmere på en lille sensor indlejret i en fiber. Kredit:UBCO Okanagan Glem det smarte ur. Tag den smarte skjorte på. Forskere ved UBC Okanagans School of En -
 Forskere udvikler lille gradientchip:System gør det lettere at måle kemisk reaktivitetHollandske nanoteknologer ved University of Twentes MESA+ forskningsinstitut har udviklet en lille chip, der gør det nemt at skabe mikrometerskalagradienter. Gradienter er gradvise overgange i specifi
Forskere udvikler lille gradientchip:System gør det lettere at måle kemisk reaktivitetHollandske nanoteknologer ved University of Twentes MESA+ forskningsinstitut har udviklet en lille chip, der gør det nemt at skabe mikrometerskalagradienter. Gradienter er gradvise overgange i specifi
- Forskere hjælper med at lukke sikkerhedshullet i populær krypteringssoftware
- Videospilsrivaler Microsoft og Sony slår sig sammen i skyen
- Airbus overskud falder, skyder skylden på skrotning af A380
- Google rykker i Hongkong-demonstrantens rollespilsapp
- Afklaring af plasmasvingninger ved hjælp af højenergipartikler
- Forskellen i klasser af stålnødder


