Brystkræft-på-en-chip til test af immunterapi-lægemidler

Brystkræftchip. Kredit:Khademhosseini Lab
Der er mange mekanismer, hvorved kroppen reagerer på fremmede angribere. En af disse involverer immunsystemets T-celler, som har en række forskellige proteiner på deres overflade kaldet 'checkpoint proteiner'. Disse kontrolpunktproteiner binder til proteiner på overfladen af andre celler og kan resultere i enten stimulering eller undertrykkelse af T-celleaktivitet. Normalt, overfladeproteiner på fremmede eller invaderende celler vil producere en stimulering af T-celleaktivitet mod disse celler, mens T-celleundertrykkelse er en indbygget mekanisme til at forhindre immunsystemet i at angribe kroppens egne normale celler.
Tumorceller, imidlertid, kan nogle gange overliste immunsystemet ved at vise overfladeproteiner, der binder med T-celle checkpoint-proteiner for at forårsage undertrykkelse af T-celleaktivitet. I nogle tilfælde, interaktion af disse tumoroverfladeproteiner med T-celler får endda T-cellerne til at briste. I de seneste år, videnskabsmænd har forsøgt at udvikle "checkpoint-hæmmer"-lægemidler, som vil modvirke disse undertrykkende checkpoint-interaktioner for at genaktivere kroppens immunrespons på tumorceller. Et af disse lægemidler er US FDA godkendt til behandling af metastatisk melanom; andre er tilgængelige eller under udvikling til behandling af andre maligne sygdomme.
På trods af disse fremskridt, imidlertid, det er stadig vanskeligt at afgøre, hvilke kræftpatienter der er sandsynlige kandidater til denne type behandling, og hvilke lægemidler der har størst potentiale. Udvikling af en metode til at løse disse udfordringer ville være medvirkende til at bestemme den sikreste, mest effektive lægemidler til kræftpatienter og samtidig spare tid og penge i processen. For at en sådan metode skal være praktisk til klinisk brug, det bør være i stand til at opnå hurtig test af et stort antal potentielle immunterapilægemidler mod levende tumorceller for nøjagtige, let analyserbare data.
Et samarbejdende team fra Terasaki Institute for Biomedical Innovation (TIBI) har med succes designet og testet et sådant system. De begyndte med at dyrke sfæriske aggregater af brystkræftceller i en specialfremstillet, 3-D printet, gennemsigtig chip med koniske mikrobrønde. Disse mikrobrønde blev designet til optimal vækst og stabilitet af de cellulære sfærer. Test udført på mikrobrøndens cellulære sfærer bekræftede cellernes levedygtighed og deres produktion af T-celle deaktiverende overfladeproteiner.
"Funktioner ved vores mikrobrønd-baserede chip er nøglen til vores succesfulde udvikling af en immunoaktiv vævsmodel, " sagde Wujin Sun, Ph.d., fra Terasaki Institutes team. "Chippens gennemsigtighed giver mulighed for direkte mikroskopisk observation. Og dens design giver mulighed for test i høj volumen, som egner sig godt til hurtig screening af immunterapeutiske lægemidler."
For at teste effektiviteten af checkpoint-hæmmermedicin til at aktivere T-cellers antitumorrespons, holdet overvejede derefter, hvordan en T-celle normalt opfører sig under aktivering. Når en T-celle stimuleres til at angribe cellulære angribere, det udskiller proteiner kaldet cytokiner, som mobiliserer andre immunceller til invasionsstedet og stimulerer cellerne til at formere sig og ødelægge angriberne. Måling af disse cytokiner kan derfor indikere niveauet af en T-celles aktivering.
Teamet skabte derefter en effektiv, automatiseret system til at måle cytokinniveauer ved hjælp af deres brystkræftfyldte mikrobrøndschip. Eksperimenter med dette system blev udført under anvendelse af anti-checkpoint proteinlægemidler; resultaterne viste, at efter inkubation af brystkræftcellerne med T-cellerne, cytokinproduktionen blev øget ved brugen af stofferne, demonstrerer deres effektivitet til at aktivere T-cellerne.
En anden måde, holdet brugte deres brystkræftchip på, var at vurdere brystkræftcellernes effekt på stimulerede T-celler. T-cellerne blev fluorescerende mærket og tilføjet til brystcancercellerne i mikrobrøndene; chippens gennemsigtighed tillod direkte observation af deres cellulære interaktion ved hjælp af fluorescerende mikroskopi. Disse brystkræftceller forårsager normalt brud på T-cellerne, men eksperimenter udført med checkpoint-hæmmere viste, at stofferne øgede T-celle-levedygtigheden i kulturerne, visuelt demonstrere, hvordan de kan modvirke virkningerne af T-cellebrud ved tumorcelleinteraktion.
Brystkræftchippen blev også brugt til direkte observation af, hvordan T-cellerne infiltrerede de cellulære brystkræftsfærer; denne type infiltration er et mål for en T-celles antitumoraktivitet og levedygtighed. Efter at have mærket hver gruppe af celler med separate farvestoffer og blandet dem i chippens mikrobrønde, T-celleinfiltration kunne visualiseres direkte ved hjælp af højopløsningsfluorescensmikroskopi. Eksperimenter udført med checkpoint-hæmmere indikerede, at der var et øget antal af T-celler og dybere penetration i brystkræftcellerne i nærvær af lægemidlerne.
Sammenfattende, TIBI-forskerne var i stand til at designe robuste og effektive metoder til at karakterisere interaktionen mellem tumor- og immunceller og til hurtig, højvolumen og klinisk relevante måder at screene immunterapeutiske lægemidler mod tumorceller på. Mikrobrøndchippen og dens relaterede apparat kan også anvendes til at inkludere andre typer tumorceller og individuelle patientceller til optimering af patientrespons og til screening og udvikling af yderligere anticancerlægemidler.
"At bringe måder til at optimere kliniske beslutninger og personlig medicin til patienter er et topmål på vores institut, " sagde Ali Khademhosseini, Ph.d., direktør og administrerende direktør for Terasaki Institute. "Dette arbejde er et vigtigt skridt i retning af at nå dette mål inden for kræftimmunterapi."
 Varme artikler
Varme artikler
-
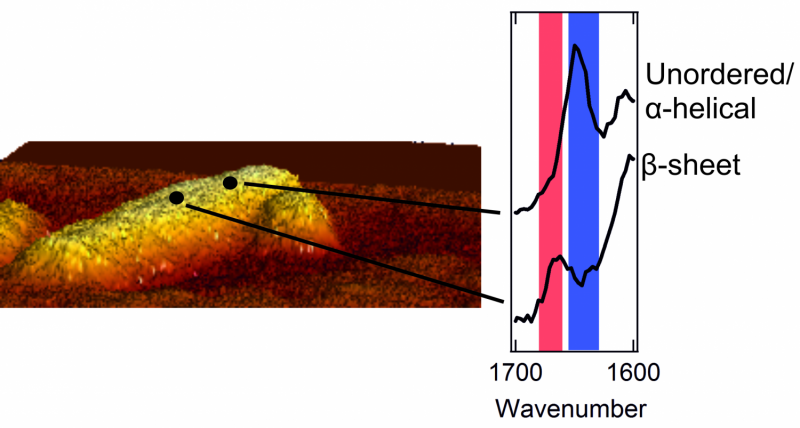 Et biologisk flugtrum:Fysikere får et glimt udefra af proteinaggregater, der forårsager diabetesTil venstre:et atomkraftmikroskopbillede af en fibril med en diameter på nogle få nanometer. Til højre:to spektre, der viser den ydre struktur. En top i det røde område er karakteristisk for et plaste
Et biologisk flugtrum:Fysikere får et glimt udefra af proteinaggregater, der forårsager diabetesTil venstre:et atomkraftmikroskopbillede af en fibril med en diameter på nogle få nanometer. Til højre:to spektre, der viser den ydre struktur. En top i det røde område er karakteristisk for et plaste -
 Forskere udvikler nye nanopartikler, der effektivt og selektivt dræber kræftcellerDe amorfe nanopartikler opløses meget effektivt i cellen. Kredit:von Schirnding et al., Chem 2020 Mange kemoterapeutiske midler, der bruges til at behandle cancer, er forbundet med bivirkninger af
Forskere udvikler nye nanopartikler, der effektivt og selektivt dræber kræftcellerDe amorfe nanopartikler opløses meget effektivt i cellen. Kredit:von Schirnding et al., Chem 2020 Mange kemoterapeutiske midler, der bruges til at behandle cancer, er forbundet med bivirkninger af -
 Filmer den termiske død af elektroner i stofFigur 1. (a) Skematisk repræsentation af eksperimentet:en tunnelstrøm flyder fra en Au STM-spids til en Ag(111)-overfladeexciterende plasmoner, hvis radiative henfald fører til fotonemission. (b) Nive
Filmer den termiske død af elektroner i stofFigur 1. (a) Skematisk repræsentation af eksperimentet:en tunnelstrøm flyder fra en Au STM-spids til en Ag(111)-overfladeexciterende plasmoner, hvis radiative henfald fører til fotonemission. (b) Nive -
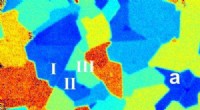 Edgy kig på 2-D molybdendisulfidEn ny SHG-billeddannelsesteknik muliggør hurtig og helt optisk bestemmelse af krystalorienteringerne af 2-D halvledermembraner i stor skala, tilvejebringe den nødvendige viden til brug af disse materi
Edgy kig på 2-D molybdendisulfidEn ny SHG-billeddannelsesteknik muliggør hurtig og helt optisk bestemmelse af krystalorienteringerne af 2-D halvledermembraner i stor skala, tilvejebringe den nødvendige viden til brug af disse materi
- Deep learning forbedrer billedrekonstruktion i optisk kohærenstomografi ved brug af færre data
- Ingeniører vurderer snetørke rundt om i verden
- Elektronisk næse genkender en række forskellige dufte
- Forskere udvikler miljøansvarlig bedste praksis for at finde olie og gas dybt under jordens overfla…
- Fremtiden for planetkølingsteknologi:Undersøgelse skaber køreplan for geoingeniørforskning
- Kemikere viser, hvordan bias kan dukke op i resultater fra maskinlæringsalgoritmer


