Forskere udvikler et lille antistof, der er i stand til at neutralisere coronavirus
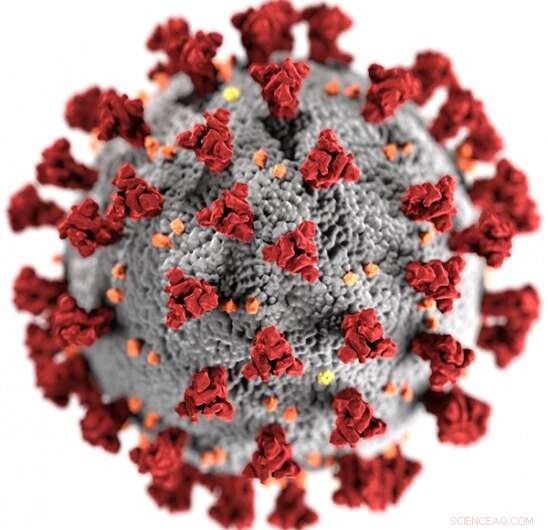
Billede af den ultrastrukturelle morfologi udstillet af 2019 Novel Coronavirus (2019-nCoV). Kredit:CDC
Klokken 02.00 en nat sidste april, Michael Schoof trippeltjekkede tallene på sin skærm, tog en dyb indånding, og fyrede en e-mail af, som han havde ventet hele dagen på at sende.
"Jeg tror, det virker" var den forsigtige formulering af hans besked.
Schoof, en kandidatstuderende i Peter Walters laboratorium, Ph.D., en anerkendt videnskabsmand med speciale i proteinsortering og cellulære membraner, var en del af et lille team på en quixotisk mission:at immobilisere SARS-CoV-2, den nye coronavirus, der forårsager COVID, ved at bruge en syntetisk version af bittesmå antistoffer, der oprindeligt blev opdaget i lamaer og kameler. Disse "nanobodies, "som de er kendt, var kommet fra UC San Francisco laboratoriet i Aashish Manglik, M.D., Ph.D., en fremadstormende proteinforsker, der havde brugt de foregående tre år på at bygge et stort bibliotek af nanokroppe og udvikle nye måder at udnytte deres usædvanlige egenskaber på.
I løbet af den foregående måned, Schoof havde tilbragt det meste af sine vågne timer i klosteret i det ellers tomme laboratoriekompleks på UCSF's Mission Bay-campus. Det var højden af COVIDs stigning i foråret 2020, og kun væsentligt sundhedspersonale og dem, der arbejder med videnskab relateret til pandemien, fik adgang til universitetets faciliteter. Schoof havde draget sin værelseskammerat, en medstuderende ved navn Reuben Saunders, til at arbejde sammen med ham om projektet. Ernærer sig af dampede dumplings og liter te, de havde sorteret gennem de 2 milliarder nanobodies i Mangliks bibliotek i håbet om at identificere et molekyle, der var i stand til at glomme videre til den dødelige SARS-CoV-2 og immobilisere den. Nu, endelig, Schoof var overbevist om, at de havde opnået deres første store gennembrud.
Det første trin i enhver virusinfektion er en cellulær kapring. For at få kontrol over en menneskelig celle, SARS-CoV-2 låser de grappling-krog-lignende pigge på sit eget ydre til proteiner kaldet ACE2-receptorer på ydersiden af en målcelle. Men hvad hvis, forskerne undrede sig, de kunne blokere flykapreren ved at give gribekrogene noget andet at låse fast i?
Den dag, Schoof var begyndt at køre test på hundredvis af kolonier af gær, hver konstrueret til at producere visse nanobodies fra Mangliks bibliotek. Alle disse særlige nanobodies havde demonstreret en evne til at låse sig fast på SARS-CoV-2's pigge. Nu var det tid til at stille nøglespørgsmålene:Hvor tæt var disse nanobodies bundet til spidserne? Var de i stand til at konkurrere med ACE2-receptorerne?
At finde ud af, Schoof havde blandet sine nanobody-udtrykkende gærceller med fluorescerende SARS-CoV-2-spidser. Da han så på resultaterne fra de to første plader, han følte et sus af begejstring, som han hurtigt dæmpede med den videnskabelige skepsis, han var blevet lært at dyrke. Nogle af nanobodies klæbede til SARS-CoV-2-spidserne, men kunne stadig være albuet til side af et overskud af humane ACE2-receptorer:klart bevis på en potentiel neutralisator.
"At, " husker han, "det var, da vi vidste, at vi havde noget."
I dagene efter Schoofs omhyggelige e-mail sent på aftenen, Walter og Manglik udnyttede deres respektive netværk af videnskabelige kontakter, indkalder forstærkninger fra laboratorier på tværs af campus og så langt væk som Paris for at hjælpe i næste fase af deres søgning. Snart, det lille hold havde forvandlet sig til en veritabel hær af tværfaglige forskere og kandidatstuderende. I november, de offentliggjorde deres resultater i det prestigefyldte tidsskrift Science. I avisen, næsten 60 medforfattere beskrev en dristig, innovativ COVID modforanstaltning, foreslår, at deres nanobodies kan bruges på en billig, næsespray, der er nem at transportere, og som er i stand til at neutralisere SARS-CoV-2. Indbyrdes de døbte molekylerne AeroNabs.
Siden da, UCSF-teamet har søgt en industripartner, der er villig til at finansiere den dyre og strenge kliniske forsøgsproces, men i øjeblikket er medicinalvirksomheder fokuseret på vaccineudvikling til forebyggelse og mere traditionelle antistoffer til behandling.
Men nanobody-tilgangen er lovende. På grund af den simple struktur af nanobodies, AeroNabs kunne være langt billigere og hurtigere at masseproducere, langt nemmere at transportere, og langt nemmere at opbevare end de traditionelle antistoffer, der i øjeblikket er i brug og under udvikling.
"Dette er noget, du kan tage efter at have testet positiv, som kan mindske din virale belastning med det samme, " siger Walter. "Så dine chancer for at udvikle alvorlig sygdom ville blive reduceret ved denne behandling."
Han bemærker også, at massevaccination vil tage tid, og at ikke alle i befolkningen kan eller vil blive vaccineret, gør passiv beskyttelse stadig utrolig værdifuld. "Og, " tilføjer han, "Vi ved ikke, hvor bredt vaccinen vil være tilgængelig ud over verdens rigeste lande."
Dynamisk duo
Frøene til AeroNabs-projektet blev plantet i 2017, da Walter hørte Manglik holde en tale om sit arbejde.
Ved første øjekast, de to videnskabsmænd ser ud til at være et mærkeligt par. Med sit fulde hoved af mørkt hår, drengeligt smil, og glatbarberet hage, Manglik kunne forveksles med en kandidatstuderende. Faktisk, han er en stigende stjerne inden for sit felt, som i 2013 lavede Scientific American s "30 under 30" liste. Født i Indien, Manglik tilbragte sine første otte år i Saudi-Arabien, før hans familie immigrerede til Des Moines, Iowa, hvor han opdagede videnskaben på college. Den 60-årige Walter, på den anden side, har et helt hvidt skæg og overskæg og briller med små linser. Han er født og opvokset i Tyskland, kom til USA for sit kandidatarbejde, og har kortlagt en legendarisk karriere. Hans mange hædersbevisninger inkluderer den prestigefyldte Lasker Award, ofte set som en forløber for en Nobelpris. Men på trods af deres forskelle, Walter og Manglik deler en dyb passion for molekylærbiologi og dens uendeligt fleksible organiske byggesten:proteiner.
Mangliks foredrag den dag handlede om hans indsats for at samle et af verdens største biblioteker af nanobodies - en lovende, relativt ny type antistof, der stammer fra blodet fra lamaer, kameler, og andre dyr i kamelfamilien. Han havde først lært om nanobodies på ph.d.-skolen i Stanford, efter at være blevet forelsket i studiet af receptorer, en bred familie af proteiner involveret i intercellulær signalering. Receptorer stikker ud af celler som antenner, hver reagerer på et specifikt kemisk signal. Mens man studerer menneskelige adrenalinreceptorer, Manglik gjorde udstrakt brug af nanobodies, hvilken, takket være deres lille størrelse, kan interagere med receptorer med langt mere præcision end de specialfremstillede antistoffer, han brugte til at udforske receptoregenskaber. Hans eksperimenter afslørede, hvordan forskellige geometriske konfigurationer af receptorer påvirker deres signaleringsadfærd.
"Proteiner er ikke bare simple lego, der passer sammen - de er ligesom lego lavet af gelé eller spartelmasse, " Manglik forklarer. "De bevæger sig konstant. Faktisk, det er bevægelsen af et protein, det viser sig, det har virkelig betydning for, hvordan det fungerer. Og nanobodies kan hjælpe os med at kontrollere den bevægelse."
Nanobodies:En velsignelse for videnskaben
Nanobodies blev opdaget i slutningen af 1980'erne af et par studerende ved det frie universitet i Bruxelles, efter de berømt henvendte sig til deres biologiprofessor, en immunolog ved navn Raymond Hamers, at klage over en opgave. Historien har sløret årsagen til deres klage; en meget citeret beretning hævder, at eleverne var bekymrede for, at opgaven, hvilket krævede, at de analyserede antistofferne i menneskeblod, kan inficere dem med en sygdom. En anden version siger, at eleverne syntes, at eksperimentet var kedeligt og bad deres professor om at tildele dem noget mere originalt.
Uanset sandheden, ingen bestrider, hvad der derefter skete. roder rundt i et laboratoriekøleskab, Hamers fandt et hætteglas med frosset dromedar kamelserum inficeret med parasitter, der menes at forårsage afrikansk sovesyge. Han gav den til eleverne og foreslog, at de isolerede antistofferne i kamelblodet for at se, hvordan de så ud. Da eleverne rensede blodet, de opdagede noget fantastisk.
Ud over de standard antistoffer, der findes i alle hvirveldyr, de rensede prøver indeholdt et afledt antistof, der aldrig før er set i videnskaben - mindre, enklere proteiner, som eleverne i første omgang forvekslede med fragmenter af konventionelle antistoffer. Yderligere undersøgelser viste, at de var en helt ny klasse af immunmidler, mangler en af de proteinkæder, der findes i alle andre tidligere undersøgte antistoffer.
Opdagelsen førte til et banebrydende papir fra 1993 i det prestigefyldte tidsskrift Natur . Hamers og hans elever døbte de nye diminutive proteiner nanobodies. Lignende enkeltkædede antistoffer blev senere identificeret i lamaer, alpakaer, guanacos (et andet langhalset sydamerikansk pattedyr), og endda hajer.
Det blev hurtigt klart, at ikke kun nanostoffer var nyttige immunologisk, men at deres lille størrelse gjorde dem til nyttige eksperimentelle værktøjer – som Manglik og hans UCSF-kolleger til fulde kan bekræfte.
At studere, hvordan disse gelatinøse byggesten på molekylært niveau bevæger sig, snap og frigør, og interagere blev Mangliks fokus, da han kom til UCSF-fakultetet. Han vidste tidligt, at nanobodies ville være en stor del af hans arbejde. Selvom antistoffer og nanostoffer findes for at hjælpe dyr med at bekæmpe infektion, Manglik ser dem også som et uendeligt formbart værktøj, der kan bruges til at hacke sig ind i en bred vifte af processer i den menneskelige krop samt afkode grundlæggende videnskabelige mysterier. Men nanobodies var tidskrævende at lave og krævede adgang til kamelider. Som kandidatstuderende, Manglik havde stolet på en samarbejdspartner i Belgien, som ville injicere et receptorprotein af interesse i en lama, høst derefter nanobodies fra dyrets blod. Hele processen tog måneder med meget specialiseret arbejde, hvilket kun få grupper havde mulighed for.
At demokratisere adgangen til nanobodies for forskere overalt, Manglik slog sig sammen med Andrew Kruse, Ph.D., en nær ven fra kandidatskolen, som var kommet til fakultetet på Harvard Medical School. Sammen, de to laboratorier skabte billioner af unikke nanobody-kodende DNA-sekvenser, hver inspireret af nanobodies, der normalt findes inde i lamaer. DNA-sekvenserne for disse nanobodies er anbragt i en stor pulje af milliarder af diminutive gærceller, som hver især kan lokkes til at sætte en kopi af en individuel nanobody på dens overflade. Helt uden om behovet for en levende lama, et sådant bibliotek giver forskere adgang til gærceller, der rummer nanokroppe, der er specifikke for en given opgave. Manglik og Kruse har åbent delt deres biblioteker med hundredvis af laboratorier rundt om i verden.
"Ideen er, at i et dyr, der er billioner af forskellige nanobodies til at kæmpe mod alt, hvad det kan støde på, " siger han. "Vi ønskede at lave et bibliotek, der kodede for milliarder af individuelle nanokroppe. Dette bibliotek ville være et godt udgangspunkt for at finde en nanobody mod stort set alt - alt i laboratoriet og uden behov for at injicere et dyr."
Efter at have hørt Manglik forklare alt dette, Walter styrede sin kandidatstuderende Michael Schoof til Mangliks laboratorium. Schoof forsøgte at modulere adfærden af et protein relateret til traumatisk hjerneskade, og Walter havde mistanke om, at Mangliks nanobodies kunne være nyttige i den indsats.
Så ramte coronavirus, verden stoppede, og næsten al ikke-COVID-relateret aktivitet på universitetet lukkes ned.
"Så på det tidspunkt, vi sagde, "Godt, vi kan enten sidde hjemme nu, eller vi kan tænke på, hvordan vi virkelig kan hjælpe i dette fremstød for en løsning, " husker Walter.
Inden for få dage, Walter og Schoof var i e-mail-kontakt med Manglik. De kendte nanobodies sygdomsbekæmpende egenskaber. En nanobody-teknologi havde for nylig vundet FDA-godkendelse til at behandle en blodkoagulationsforstyrrelse, og en anden, bruges til at behandle en luftvejsvirus, havde nået et sent stadium i kliniske forsøg.
Var det muligt, at de kunne bygge en til at bekæmpe coronavirus?
Et fantastisk resultat
Fra begyndelsen, holdet vidste, projektets succes ville hvile på deres evne til at finde en nanobody med tilstrækkelig bindingsaffinitet – evnen til at binde sig til og spændetrøje coronaviruss pigge.
Proteiner har bestemte former. Hvor godt to proteiner passer sammen bestemmer deres bindingsaffinitet. Walter og Manglik vidste, at den bindingsaffinitet, der får SARS-CoV-2 til at klæbe til ACE2-proteiner, teoretisk set kunne overmandes af en nanobody formet på den helt rigtige måde.
Manglik havde allerede en nøgleingrediens til sådan et eksperiment. Forskere ved University of Texas (UT) i Austin havde for nylig afsløret den unikke struktur af SARS-CoV-2-spidserne, som gjorde det muligt for virussen at binde sig til humane cellers ACE2-receptorer. Manglik nåede ud til UT's Jason McLellan, Ph.D., som gik med til at sende ham deres "konstruktion" - et stykke DNA, der koder for spidserne, der kunne indsættes i en anden celle, udtrykt i store mængder, renset, og bruges til eksperimenter.
Holdet begyndte at screene de 2 milliarder nanobodies i biblioteket for at se, om de kunne finde forbindelser med den rigtige bindingsaffinitet til SARS-CoV-2-spidserne. Inden for tre uger, de havde identificeret 800 potentielle kandidater, og en uge senere skrev Schoof sin forsigtige e-mail sent om aftenen og informerede Manglik og Walter om, at han havde set nogle indledende positive resultater. I slutningen af april, holdet havde identificeret 21 forskellige nanokroppe, der så ud til at konkurrere med ACE2-receptoren, teoretisk blokerer SARS-CoV-2 fastgørelsesmekanismen.
Det var da det lille hold begyndte at blive større, rekruttering af strukturelle biologer for at finde ud af, hvordan nanobodies bandt sig til SARS-CoV-2-spidsproteinet, og derefter bruge disse oplysninger til at designe ændringer for at gøre dem endnu mere kraftfulde.
Det krævede oprensning af 21 kandidatproteiner, afprøve deres binding, og derefter bruge UCSF's kryo-elektronmikroskopi faciliteter til at afbilde de mest lovende kandidater i næsten-atomar opløsning, mens de var bundet til SARS-CoV-2-spidsen. For at fuldføre denne monumentale opgave, de gik sammen med en parallel indsats kendt som QCRG Structural Biology Consortium – en samlebåndslignende proces, der er sammensat af 12 UCSF-fakultetsmedlemmer og over 60 praktikanter for at tackle SARS-CoV-2. Indsatsen blev drevet af en følelse af at det hastede, og deltagerne arbejdede udmattende timer langt ud på natten.
Når holdet havde billeder af de øverste nanobodies bundet til SARS-CoV-2-spidsen, de begyndte at undersøge hver enkelt nanobodys unikke bindingsmekanisme og brugte den information til at designe en næste generations version. De besluttede sig for at konstruere en tre-armet nanobody bestående af tre kopier af en enkelt nanobody syet sammen, så den kunne binde sig samtidigt til de tre separate arme, der udgør hver coronavirus-spids.
Efter at have syet nanoboderne sammen og testet dem, Bryan Faust, en kandidatstuderende i Mangliks laboratorium, leverede det næste spændende fund:Hver af de tre arme forbedrede bindingen af sine naboer eksponentielt. Den forbedrede versions evne til at binde sig til de virale spidser steg to hundrede tusind gange.
"Dette var et fantastisk resultat - at se denne enorme rækkefølge af forbedringer, Walter husker. "Det var en absolut festtid."
For at teste forbindelsen mod en levende virus, holdet havde brug for et laboratorium med en Biosafety Level 3 (BSL-3) betegnelse. Gruppen rekrutterede Marco Vignuzzi, Ph.D., en tidligere UCSF postdoc, der driver et BSL-3 laboratorium ved Institut Pasteur i Paris. I juni, en af Vignuzzis postdocs kørte UCSF nanobody mod faktisk SARS-CoV-2 for at se, om den var i stand til at neutralisere virussen.
Slutresultatet var både yderst effektivt og stabilt - så stabilt, at det kan leveres i aerosolform ved hjælp af en mesh-forstøver, som Manglik købte på Amazon.
Med Big Pharma laser-fokuseret på at udvikle vacciner og traditionelle antistoffer, at finde en hurtig vej til kommercialisering har vist sig at være udfordrende. Men Manglik, Walter, og deres hold er uafskrækket.
"Det er næsten sikkert, at der vil være flere respiratoriske pandemier i vores levetid, " siger Manglik. "Det kan være influenza, støvfang SARS-pandemi, eller et patogen, vi ikke engang kender til endnu. Til den næste pandemi, håbet er, at forskere ikke kun kunne gå så hurtigt, som vi gjorde, men måske endda hurtigere."
Uden tvivl, det ville være svært at finde et mere potent vidnesbyrd om den dejlige uforudsigelighed og potentiale i moderne videnskab - at en pandemi, der har forårsaget ensomhed, lidelse, og døden gav også anledning til denne eklektiske besætning og deres potentielt livreddende løsning, der for blot et par år siden kunne have virket absurd.
"Det er bare en af de ting, hvor du siger, "Vi vil på dette eventyr, "" siger Walter. "Vi forpligtede os til det, og så fungerede det bare meget bedre, end vi kunne have drømt om."
Sidste artikelEt magnetisk twist til grafen
Næste artikelForskere skaber lave omkostninger, AI-drevet enhed til at måle optiske spektre
 Varme artikler
Varme artikler
-
 Mikrosvømmere er livløse mikropartikler, men de bevæger sig som møl til lysetJanus partikler under elektronmikroskopet. Titandioxid mikrosvømmerne er knapt større end en mikrometer. Copyright:Simmchen Group Freigeist-gruppen ved TU Dresden, ledet af kemiker Dr. Juliane Sim
Mikrosvømmere er livløse mikropartikler, men de bevæger sig som møl til lysetJanus partikler under elektronmikroskopet. Titandioxid mikrosvømmerne er knapt større end en mikrometer. Copyright:Simmchen Group Freigeist-gruppen ved TU Dresden, ledet af kemiker Dr. Juliane Sim -
 Nanorør katode slår stort, dyr laserDet mørke område af denne katode er lavet af millioner af nanorør, der fungerer som små lynafledere. Forskere er et skridt tættere på at bygge en intens elektronstrålekilde uden laser. Brug af ele
Nanorør katode slår stort, dyr laserDet mørke område af denne katode er lavet af millioner af nanorør, der fungerer som små lynafledere. Forskere er et skridt tættere på at bygge en intens elektronstrålekilde uden laser. Brug af ele -
 Pebermynteolie og kanel kan hjælpe med at behandle og hele kroniske sårInfektiøse kolonier af bakterier kaldet biofilm, der udvikler sig på kroniske sår og medicinsk udstyr, kan forårsage alvorlige helbredsproblemer og er svære at behandle. Men nu har forskere fundet en
Pebermynteolie og kanel kan hjælpe med at behandle og hele kroniske sårInfektiøse kolonier af bakterier kaldet biofilm, der udvikler sig på kroniske sår og medicinsk udstyr, kan forårsage alvorlige helbredsproblemer og er svære at behandle. Men nu har forskere fundet en -
 Engineering selvsamlende amyloidfibreAmyloidfibre samler sig selv fra mindre proteiner. UC Davis forskere har konstrueret andre proteiner, så de spontant danner amyloid. Disse nye proteiner kan være nyttige i nanoteknologi. Her, hættestr
Engineering selvsamlende amyloidfibreAmyloidfibre samler sig selv fra mindre proteiner. UC Davis forskere har konstrueret andre proteiner, så de spontant danner amyloid. Disse nye proteiner kan være nyttige i nanoteknologi. Her, hættestr
- Polymerer til undsætning! Redder celler fra at beskadige is
- Forskere finder kun få beviser for teori om knuste vinduer, sige, at naboskabsforstyrrelser ikke fo…
- Ultraviolet lyser på solsystemets oprindelse
- Meteor forårsager panik i pakistanske bjergrige nord
- Syngenta afgør amerikanske landmandssager i en sag om handel med majs i Kina
- Saltaflejringer på Mars har spor til kilder til gammelt vand


