Eliminering af resistente bakterier med nanopartikler
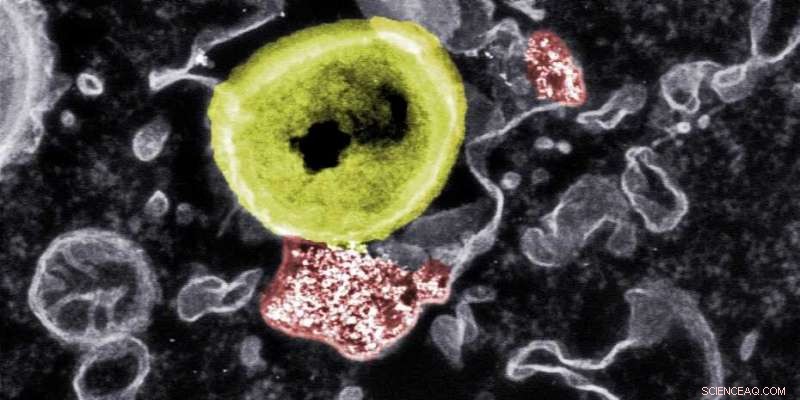
Forskerne har udviklet nanopartikler (røde), der kan dræbe resistente bakterier (gule), der er inkorporeret af kroppens celler (farvet elektronmikroskopibillede). Kredit:Empa
Nye nanopartikler udviklet af forskere ved ETH Zürich og Empa opdager multiresistente bakterier, der gemmer sig i kropsceller, og dræber dem. Forskernes mål er at udvikle et antibakterielt middel, der er effektivt, hvor konventionelle antibiotika forbliver ineffektive.
I våbenkapløbet "menneskeheden mod bakterier, " bakterier er i øjeblikket foran os. Vores tidligere mirakelvåben, antibiotika, fejler oftere og oftere, når bakterier bruger vanskelige manøvrer for at beskytte sig mod virkningerne af disse stoffer. Nogle arter trækker sig endda tilbage til indersiden af menneskelige celler, hvor de forbliver "usynlige" for immunsystemet. Disse særligt frygtede patogener omfatter multiresistente stafylokokker (MRSA), som kan forårsage livstruende sygdomme som sepsis eller lungebetændelse.
For at spore bakterierne i deres gemmesteder og eliminere dem, et team af forskere fra ETH Zürich og Empa udvikler nu nanopartikler, der bruger en helt anden virkemåde end konventionelle antibiotika:Mens antibiotika har svært ved at trænge ind i menneskelige celler, disse nanopartikler kan trænge ind i membranen af berørte celler. Når først der, de kan bekæmpe bakterierne.
Bioglas og metal
Holdet ledet af Inge Herrmann, en professor i nanopartikelsystemer ved ETH Zürich og forsker ved Empa i St. Gallen, brugt ceriumoxid, et materiale med antibakterielle og antiinflammatoriske egenskaber i sin nanopartikelform. Forskerne kombinerede ceriumoxidet med et bioaktivt keramisk materiale kendt som bioglas og syntetiserede nanopartikelhybrider fra de to materialer.
I cellekultur og ved hjælp af elektronmikroskopi, de undersøgte interaktionerne mellem de hybride nanopartikler, menneskelige celler og bakterier. Da forskerne behandlede celler inficeret med bakterier med nanopartiklerne, bakterierne inde i cellerne begyndte at opløses. Imidlertid, hvis forskerne specifikt blokerede optagelsen af hybridpartiklerne i cellerne, den antibakterielle virkning var væk.
Udvikling af resistens mindre sandsynlig
Partiklernes nøjagtige virkemåde er endnu ikke fuldt ud forstået. Det har vist sig, at andre metaller også har antimikrobielle virkninger. Imidlertid, cerium er mindre giftigt for menneskelige celler end, for eksempel, sølv. Forskere antager i øjeblikket, at nanopartiklerne påvirker bakteriens cellemembran, skabe reaktive iltarter, der fører til ødelæggelse af bakterierne. Da cellemembranen i menneskelige celler er struktureret anderledes end bakteriers, vores celler påvirkes ikke af denne proces.
Forskerne mener, at der er mindre sandsynlighed for, at der udvikles resistens mod en mekanisme af denne art. Næste, forskerne sigter mod at analysere partiklernes interaktioner i infektionsprocessen mere detaljeret for yderligere at optimere strukturen og sammensætningen af nanopartiklerne. Deres mål er at udvikle et simpelt og robust antibakterielt middel, der er effektivt inde i inficerede celler.
 Varme artikler
Varme artikler
-
 Et twist bringer nye muligheder for ultratynde 2D-materialerKredit:The Australian National University En ny undersøgelse fra The Australian National University (ANU) viser, hvordan 2D-materialers evne til at omdanne sollys til elektricitet kan styres ved b
Et twist bringer nye muligheder for ultratynde 2D-materialerKredit:The Australian National University En ny undersøgelse fra The Australian National University (ANU) viser, hvordan 2D-materialers evne til at omdanne sollys til elektricitet kan styres ved b -
 Nanosvampe opsuger olie igen og igenDen superhydrofobe carbon nanorørsvamp viser en bemærkelsesværdig evne til at opsuge olie fra vand. Forskere fandt ud af, at tilføjelse af bor til vækstprocessen skaber kovalente bindinger i nanorøren
Nanosvampe opsuger olie igen og igenDen superhydrofobe carbon nanorørsvamp viser en bemærkelsesværdig evne til at opsuge olie fra vand. Forskere fandt ud af, at tilføjelse af bor til vækstprocessen skaber kovalente bindinger i nanorøren -
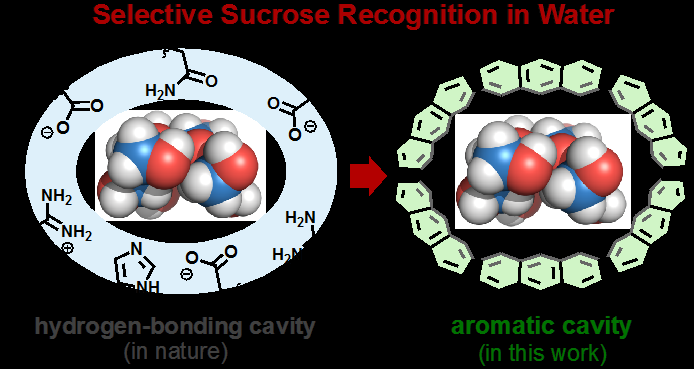 Sød succes:Nanokapsel binder saccharose perfekt i vandKonceptuel tegneserie af, hvordan en bioreceptor (til venstre) og en Yoshizawas nanokapsel (til højre) binder saccharose i deres hulrum. Kredit: Videnskabens fremskridt Forskere over hele verden
Sød succes:Nanokapsel binder saccharose perfekt i vandKonceptuel tegneserie af, hvordan en bioreceptor (til venstre) og en Yoshizawas nanokapsel (til højre) binder saccharose i deres hulrum. Kredit: Videnskabens fremskridt Forskere over hele verden -
 Forskere bygger verdens mindste vandflaskeEt åbent og lukket fullerenbur rummer et enkelt vandmolekyle. Billedkredit:Angewandte Chemie. Forskere har designet og bygget en beholder, der kun rummer et enkelt vandmolekyle. Beholderen består
Forskere bygger verdens mindste vandflaskeEt åbent og lukket fullerenbur rummer et enkelt vandmolekyle. Billedkredit:Angewandte Chemie. Forskere har designet og bygget en beholder, der kun rummer et enkelt vandmolekyle. Beholderen består
- Interstellar besøgende formet som kæmpe ildslukker (Opdatering)
- Alkymien om at fusionere neutronstjerner
- NASA Voyager 2 kan nærme sig det interstellare rum
- Ungdomssexting:Grundlæggende skift i uddannelsestilgang er nødvendig for at ændre kultur
- Musikstreaminggiganten Deezer indsamler 160 millioner euro
- Typer af vejr og ætsning


