Polymersomer leverer effektivt siRNA til behandling af brystkræft i præklinisk model

Eugenia Kharlampieva. Kredit:UAB
Små interfererende RNA'er - eller siRNA'er - lover at behandle tumorer gennem deres evne til specifikt at slå onkogener ned, der fremmer tumorvækst uden den toksicitet, der følger med kemoterapi. Imidlertid har siRNA'erne brug for et transportmiddel for at beskytte dem mod nedbrydning og clearance på deres rejse gennem blodbanen til kræfttumoren.
Eugenia Kharlampieva, Ph.D., og Eddy Yang, M.D., Ph.D., fra University of Alabama i Birmingham har demonstreret et 100 nanometer polymersom, der sikkert og effektivt bærer PARP1 siRNA til triple-negative brystkræfttumorer i mus. Der slog siRNA'et ekspressionen af DNA-reparationsenzymet PARP1 ned og gav bemærkelsesværdigt nok brystkræftbærende mus en firedobling i overlevelse.
PARP-hæmmere har haft succes med at målrette tumorer med defekter i DNA-reparation og kan modulere det tumorimmune mikromiljø. Men grundet knoglemarvssuppression har det været udfordrende at kombinere mange af PARP-hæmmerne med kemoterapi. Specifikt målretning mod PARP1 i tumoren kan give mulighed for nye kombinationsbehandlinger.
"Så vidt vi ved, repræsenterer vores arbejde det første eksempel på bionedbrydelige, ikke-ioniske polymere nanovesikler, der effektivt kan indkapsle og levere PARP1 siRNA til at slå PARP1 ned in vivo," rapporterer de i tidsskriftet ACS Applied Bio Materials . "Vores undersøgelse giver en avanceret platform til udvikling af præcisionsmålrettede terapeutiske bærere, som kan hjælpe med at udvikle effektive nanobærere til lægemiddellevering til genterapi for brystkræft."
Deres hurtige og sikre tilgang til PARP1 siRNA-indkapsling og levering til brystkræftceller bruger polymere nanovesikler, der er samlet af tre bionedbrydelige blokcopolymerer forbundet med hinanden i en lige kæde. Den første blok, en kæde på 14 molekyler af N-vinylpyrrolidon, er knyttet til den anden blok, en kæde på 47 molekyler af dimethylsiloxan, og som er forbundet med en tredje blok af en anden 14-molekyle kæde af N-vinylpyrrolidon.
UAB-forskerne brugte ligefremme metoder, der gør det muligt for disse blokpolymerer at samles til 100 nanometer-diameter, hulkugle-polymersomer, der har en robust skaltykkelse på omkring 13 nanometer. Samlingsmetoden er i stand til produktion i stor skala og ensartet kvalitetskontrol.
Polymersomer samlet i nærværelse af en mikromolær PARP1 siRNA var i stand til at indlæse RNA'et inde i nanobærerne. Da disse blev brudt op ved ultralyd in vitro, blev siRNA'et frigivet uændret. Polymersomerne kunne også fyldes med Cy5.5 fluorescerende farvestof; 18 timer efter injektion af de farvestoffyldte nanobærere i tumorbærende mus havde farvestof ophobet sig i tumorerne gennem passiv målretning.

Eddy Yang. Kredit:UAB
Holdet testede siRNA-ladede polymersomer med HER2-positive, trastuzumab-resistente brystkræftceller i kultur. De reducerede proteinniveauer af PARP1 i cellerne, hvilket hæmmede deres proliferation og undertrykte NF-KB-transkriptionsfaktorvejen, svarende til hvad forskerne tidligere havde rapporteret ved brug af PARP-hæmmere.
Forskere var også i stand til at vedhæfte fluorescerende farvestof kovalent til ydersiden af disse alsidige nanokapsler, og de foreslår, at målrettede molekyler kan tilføjes på samme måde for at gøre polymersomet hjemme i en tumor.
"Disse ikke-ioniske, biologisk nedbrydelige PVPON14 −PDMS47 −PVPON14 nanovesikler, der er i stand til den effektive indkapsling og levering af PARP1 siRNA til succesfuldt at slå PARP1 ned in vivo, har et stærkt potentiale til at blive en avanceret platform for udvikling af præcisionsmålrettede terapeutiske bærere," sagde Yang. "De kunne hjælpe med udviklingen af yderst effektive nanobærere til lægemiddellevering til genterapi for brystkræft."
PVPON er poly(N-vinylpyrrolidon), og PDMS er poly(dimethylsiloxan). De siRNA'er, som polymersomerne kan bære, er meget små, omkring 21 til 25 nukleotider lange, men alligevel kan de specifikt hæmme onkogenekspression gennem nedbrydning af dets messenger-RNA. + Udforsk yderligere
Forskere identificerer nyt relevant mål for PARP-hæmmeren talazoparib
 Varme artikler
Varme artikler
-
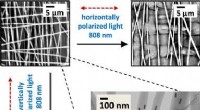 Forskere nanoweld ved at anvende lys på justerede nanoroder i faste materialerPolariseret lys opvarmer og smelter selektivt nanofibre, der indeholder justerede guld-nanoroder i en tværrukket måtte, når polariseringsretningen er parallel med nanofiberretningen. Kredit:Joe Tracy,
Forskere nanoweld ved at anvende lys på justerede nanoroder i faste materialerPolariseret lys opvarmer og smelter selektivt nanofibre, der indeholder justerede guld-nanoroder i en tværrukket måtte, når polariseringsretningen er parallel med nanofiberretningen. Kredit:Joe Tracy, -
 Plasmoniske nanoreaktorer regulerer selektiv oxidation via energiske elektroner og nanobegrænsede t…Karakterisering af Au-Cu2O katalysator og dens katalytiske ydeevne respons på belysning. (A) Skematisk over den SP-regulerede partielle oxidation af propylen på Au-Cu2O plasmonstrukturen. (B) SEM-bill
Plasmoniske nanoreaktorer regulerer selektiv oxidation via energiske elektroner og nanobegrænsede t…Karakterisering af Au-Cu2O katalysator og dens katalytiske ydeevne respons på belysning. (A) Skematisk over den SP-regulerede partielle oxidation af propylen på Au-Cu2O plasmonstrukturen. (B) SEM-bill -
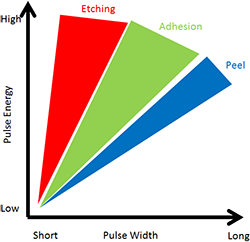 Forbedret vedhæftning og mønsterdannelse af belagt metal tynd film ved lysbestrålingFigur 1:Ændringer i vedhæftningen af en guldbelægningsfilm på en PET-film under forskellige betingelser for pulserende lysbestråling (bestrålingstid og -intensitet). Forskere fra National Instit
Forbedret vedhæftning og mønsterdannelse af belagt metal tynd film ved lysbestrålingFigur 1:Ændringer i vedhæftningen af en guldbelægningsfilm på en PET-film under forskellige betingelser for pulserende lysbestråling (bestrålingstid og -intensitet). Forskere fra National Instit -
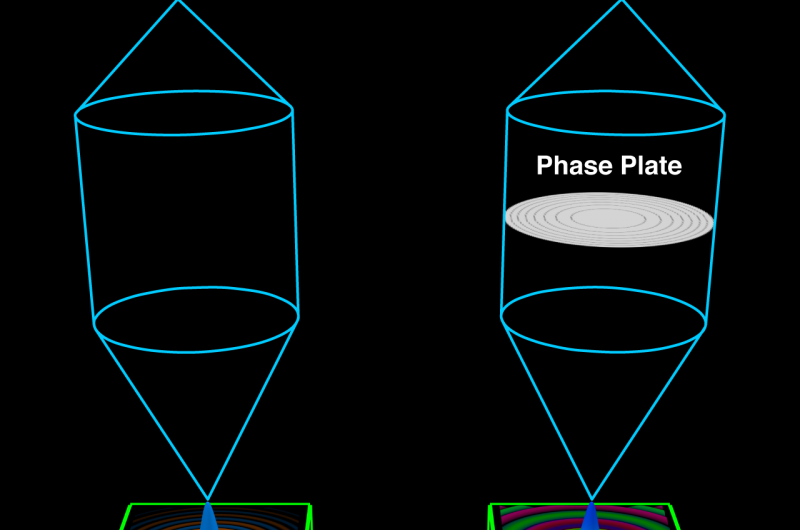 Ny form for elektronstrålebilleddannelse kan se elementer, der er usynlige for almindelige metodern MIDI-STEM (højre), udviklet på Berkeley Lab, en elektronstråle bevæger sig gennem en ringet faseplade, producerer et billede i høj opløsning (nederst til højre), der indeholder detaljer om en prøve,
Ny form for elektronstrålebilleddannelse kan se elementer, der er usynlige for almindelige metodern MIDI-STEM (højre), udviklet på Berkeley Lab, en elektronstråle bevæger sig gennem en ringet faseplade, producerer et billede i høj opløsning (nederst til højre), der indeholder detaljer om en prøve,
- Luftforurening dræber 600, 000 børn hvert år:WHO
- Der er utilstrækkelige beviser for, at din solcreme skader koralrev
- En ramme til at evaluere og sammenligne selvrekonfigurerbare robotsystemer
- Hamstring og hyrning under COVID-19-pandemien
- Nordamerika først:Forskere offentliggør videnskabelig undersøgelse om cannabisproduktion
- Tror du, at du bliver en god chef? Forskning viser, at magt kan korrumpere


