Nanokapsel med et CRISPR-Cas9-redigeringsværktøj, der bruges til ikke-invasiv hjernelevering og tumorcellemålretning
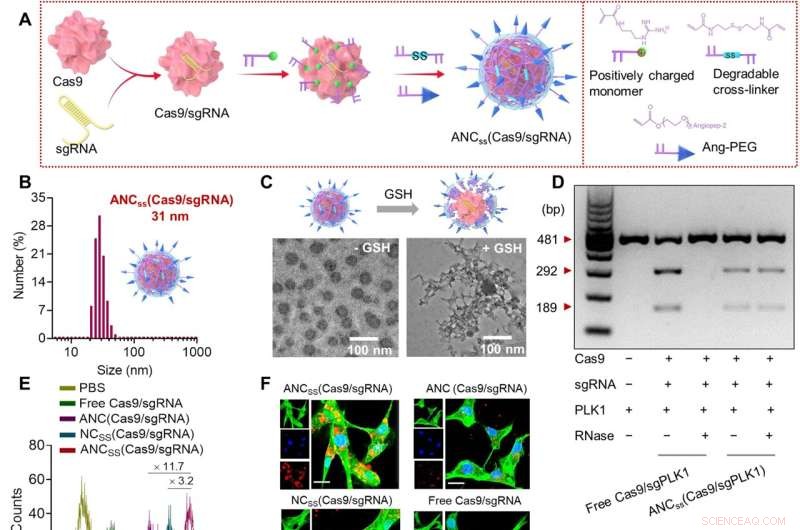
Fremstilling, fysiske egenskaber og cellulær funktion af Cas9/sgRNA nanokapsler. (A) In situ fri-radikal polymerisation blev brugt til at syntetisere disulfid-tværbundne nanokapsler indeholdende Cas9/sgRNA og funktionaliseret med angiopep-2 målretningsligand. (B) Størrelsesfordeling af ANCSS (Cas9/sgRNA) nanokapsler bestemt ved dynamisk lysspredning. (C) TEM-billeder af ANCSS (Cas9/sgRNA) med eller uden GSH-behandling. (D) Gelelektroforeseanalyse af ANCSS (Cas9/sgPLK1) eller fri Cas9/sgPLK1 med eller uden RNase-behandling (1 mg/ml, 30 min). (E) Flowcytometri af U87MG-celler efter 4-timers inkubation med ANCSS (Cas9/sgRNA) eller kontroller. (F) Konfokal laser scanning mikroskopi (CLSM) billeder af U87MG celler efter 4-timers inkubation med ANCSS (Cas9/sgRNA) eller kontroller. Cas9 blev mærket med Alexa Fluor 647 (AF647; rød); cytoskelettet blev farvet med Alexa Fluor 488 (grøn), og kernerne blev farvet med Hoechst 33342 (blå). For (E) og (F) var AF647-Cas9-koncentrationen 20 nM. Skala barer, 20 μm. (G) Luciferase-genredigeringseffektivitet i U87MG-Luc-celler inkuberet med ANCSS (Cas9/sgRNA) eller kontroller i 72 timer. Data præsenteres som middelværdier ± SD (n =5; *P <0,05, **P <0,01 og ***P <0,001). (H) Indeller af PLK1-genet i U87MG-celler transficeret med ANCSS (Cas9/sgPLK1) eller kontroller i 48 timer. (I) Skematisk genredigering i kernen. (J) Ekspressionsniveauer af PLK1 i U87MG-celler efter 72-timers inkubation med ANCSS (Cas9/sgPLK1) eller kontroller. (K) Apoptoseassay af U87MG-celler efter 72-timers inkubation med ANCSS (Cas9/sgRNA) og andre kontroller. For (G) til (K) var Cas9-koncentrationen 20 nM. bp, basepar; PBS, fosfatpufret saltvand. Kredit:Science Advances (2022). DOI:10.1126/sciadv.abm8011
Et internationalt hold af forskere har udviklet en nanokapsel, der er i stand til at krydse blod-hjernebarrieren (BBB) for at bære CRISPR-Cas9-redigeringsværktøjet til behandling af en hjernetumor. I deres papir offentliggjort i tidsskriftet Science Advances, gruppen beskriver, hvordan de skabte deres kapsel, og hvor godt den virkede, når den blev testet på mus med glioblastom.
Glioblastomer er notorisk svære at behandle. Tumorerne opstår i hjernen, og deres vækst beskadiger væv. Behandlingsmuligheder omfatter kirurgisk fjernelse, direkte injektioner af terapier beregnet til at dræbe kræftcellerne eller indsættelse af CRISPR-vira i blodbanen. Hver af disse muligheder har en ulempe, fra beskadiget hjernevæv til ineffektivitet på grund af vanskeligheder med terapier, der krydser BBB. I denne nye indsats har forskerne prøvet en ny tilgang ved at bruge en nanokapsel til at bære CRISPR-Cas9-redigeringsværktøjet til hjernetumoren, hvor det målretter mod et gen, der er ansvarligt for udviklingen af nye celler - en kapsel, der er i stand til sikkert krydser BBB.
Skallen af nanokapslen blev skabt ved hjælp af en disulfid, tværbundet polymer, der derefter blev prikket med et angiopep-2-peptid. Peptidet blev tilsat for at skabe en neutral overfladeladning, så det ikke ville blive angrebet af ribonuklease. Skallen var lige stor nok til at rumme et Cas9-kompleks, men stadig lille nok (ca. 30 nanometer i længden) til at den kunne passere gennem BBB.
Forskerne testede deres nanokapsel-leveringssystem i glioblastom-musemodeller. Hver blev givet en enkelt haleinjektion - nogle modtog det nyudviklede nanokapsel-leveringssystem, mens andre modtog en kontrol. Forskerne fandt ud af, at de mus, der fik den nye terapi, havde en gennemsnitlig overlevelsestid på 68 dage sammenlignet med 24 dage for kontrolgruppen. De fandt også en mindre end 0,5 % uønsket genetisk mutationsrate i andet hjernevæv.
Forskerne foreslår, at deres arbejde repræsenterer et nyt skridt mod ikke-invasive og nonvirale tilgange til behandling af glioblastomer, selvom de erkender, at der skal gøres meget mere arbejde, før det kan afgøres, om den samme tilgang vil være både sikker og effektiv hos mennesker. + Udforsk yderligere
Små kapsler tilbyder alternativ til viral levering af genterapi
© 2022 Science X Network
 Varme artikler
Varme artikler
-
 Forskere retter blikket mod chalcogenid nanostrukturerede skærmeIllustration af den antimontrisulfid programmerbare metasurface og dens reflektionsspektrum i flere tilstande. Kredit:SUTD En af nøglekomponenterne bag næste generation af videoskærme i høj opløsni
Forskere retter blikket mod chalcogenid nanostrukturerede skærmeIllustration af den antimontrisulfid programmerbare metasurface og dens reflektionsspektrum i flere tilstande. Kredit:SUTD En af nøglekomponenterne bag næste generation af videoskærme i høj opløsni -
 Voksende Europas nanotråde(PhysOrg.com) -- Europæiske forskere har udviklet avanceret nanotråds voksende teknologi, åbner vejen for hurtigere, mindre mikrochips og skabe en lovende ny vej for forskning og industriel udvikling
Voksende Europas nanotråde(PhysOrg.com) -- Europæiske forskere har udviklet avanceret nanotråds voksende teknologi, åbner vejen for hurtigere, mindre mikrochips og skabe en lovende ny vej for forskning og industriel udvikling -
 Push-Button Logic på nanoskalaen(PhysOrg.com)-Kredsløb, der kan udføre logiske operationer med et tryk på en knap, er en krone i dusin i disse dage, men et gennembrud af forskere i USA har betydet, at de kan være mindre og enklere e
Push-Button Logic på nanoskalaen(PhysOrg.com)-Kredsløb, der kan udføre logiske operationer med et tryk på en knap, er en krone i dusin i disse dage, men et gennembrud af forskere i USA har betydet, at de kan være mindre og enklere e -
 Klolignende nanotråde filtrerer bakterier fra blodFremstilling og karakterisering af en dialysator. en skematisk illustration af det komplekse blodmiljø i et blodkar, der viser udfordringen med bakterieindfangning. b Blodrensning ved at lede det bakt
Klolignende nanotråde filtrerer bakterier fra blodFremstilling og karakterisering af en dialysator. en skematisk illustration af det komplekse blodmiljø i et blodkar, der viser udfordringen med bakterieindfangning. b Blodrensning ved at lede det bakt
- varme somre, intense brænde sæsoner frø zombie brande:undersøgelse
- Hvad I alverden? Fragmenter af gammel havbund, Jordens indre kappe identificeret i Baltimore-område…
- Liberale og konservative har forskellige syn på retfærdighed, men deler protestantisk arbejdsmoral
- Indonesiens tsunami forværret af formen af Palu -bugten:forskere
- Udvikling af avanceret materialesynteseteknologi i metastabil fase
- Billede:Hubbles-galaksen NGC 4242


