Nanostrukturer med forbedret stabilitet til udvikling af mere effektiv cancer nanomedicin
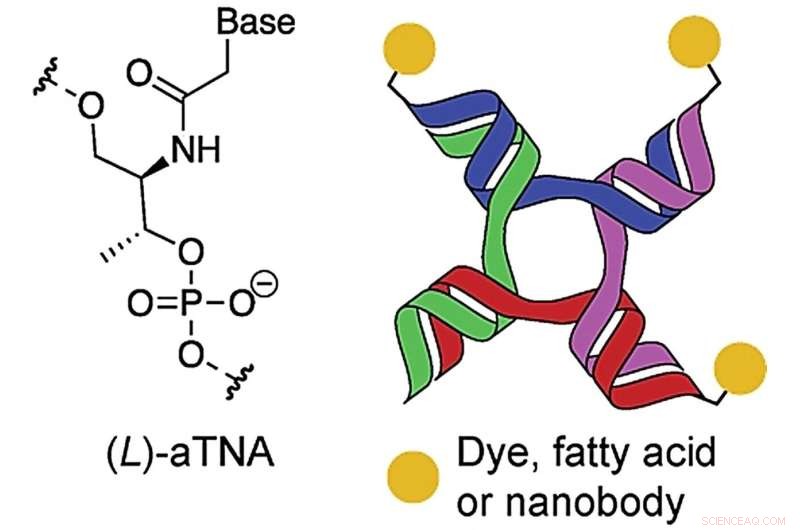
Forskere ved Aarhus Universitet har fundet en måde at skabe mere stabile nanostrukturer, der kan binde og samle biomolekyler med forskellige funktioner, som i kombination f.eks. kan give mere effektiv kræftmedicin. Illustrationen er fra den videnskabelige artikel i Angewandte Chemie Int. Ed., som skematisk viser nanostrukturen anvendt med kæder af den kunstige byggesten, acyklisk L-threoninol-nukleinsyre (aTNA). Kredit:Angew. Chem.Int. red.
I årtusinder har DNA spillet en central rolle i lagringen af hver celles genetiske information og består af strenge med en bestemt sekvens af fire forskellige byggesten. Disse DNA-strenge kopieres af cellen ved hver celledeling på en ekstremt velorkestreret måde, men utroligt nok er dette sofistikerede maskineri styret af meget simple regler.
I de senere år har det vist sig at bruge disse enkle regler ikke kun i forbindelse med genteknologi, men også til at konstruere nyttige DNA-nanostrukturer ved at designe DNA-strenge. Disse DNA-nanostrukturer har vist sig at have en række nyttige biomedicinske funktioner, såsom at kunne transportere kræftlægemidler til præcise steder i kroppen, hvor de er nødvendige. Dette kan øge effekten af medicinen samt give færre bivirkninger sammenlignet med konventionel kræftbehandling.
DNA nanostrukturer bruges også i stigende grad som et værktøj til at binde og samle biomolekyler til multifunktionelle strukturer. En af disse anvendte DNA-nanostrukturer danner en forgrenet struktur med fire ender, kaldet 4-vejs junctions (4WJ), som også findes naturligt.
Med specialdesignede versioner af disse 4WJ-strukturer har Harvard Medical School i Boston for eksempel formået at binde og opsamle forskellige antistoffer, som i kombination sikrede, at T-celler angreb aggressive kræftceller mere intensivt og dermed dræbte tumorer.
Forbedrede DNA-nanostrukturer med kunstige byggesten
Forskere, der er en del af Center for Multifunctional Biomolecular Drug Design (CEMBID) ved Aarhus Universitet, arbejder også på at finde nye måder at koble forskellige lægemidler sammen for at opnå flere og mere effektive virkningsmekanismer. Forskergruppen, ledet af professor Kurt Gothelf, har netop publiceret en artikel i tidsskriftet Angewandte Chemie Int. Red. med resultater, der involverer ovennævnte 4WJ-strukturer, men i en forbedret version. Værket er udført i samarbejde med grupperne af Jørgen Kjems og Ken Howard, som også er en del af CEMBID.
Disse DNA-nanostrukturer (4WJ) er ganske vist smarte, men der er den ulempe ved DNA-strukturer, at DNA de facto er en bionedbrydelig polymer. Det betyder, at strukturerne nedbrydes hurtigere i blodet end ønsket. Derudover kan strukturerne være så store, at de selv aktiverer immunforsvaret. For at strukturerne kan bruges til diagnostik eller i medicin, er det afgørende, at strukturerne er meget stabile, ugiftige og ikke i sig selv udløser en immunreaktion hos patienten.
Anders Märcher, postdoc i Kurt Gothelfs forskningsgruppe og en del af CEMBID, har nu sammen med sine forskerkolleger fundet en måde at øge stabiliteten af disse nanostrukturer på. Det har de opnået ved at bruge små kæder, kaldet oligonukleotider, af kunstige og modificerede byggesten til at danne nanostrukturen. De kunstige oligonukleotider, Märcher et al. brug kaldes acyklisk L-threoninol-nukleinsyre (aTNA) og virker på samme måde og lige så godt som de naturlige byggesten i DNA. Her erstattes sukkermolekylet (deoxyribose) i de naturlige byggesten med et kunstigt sukkermolekyle (acyklisk L-threoninol), som styrker den overordnede struktur.
De positive resultater viste, at 4WJ-strukturer med den kunstige byggesten, aTNA, er meget stabile, ikke nedbrydes i blodet, har vist sig at være ikke-toksiske for celler og ikke fremkalder et uspecifikt immunrespons. Da forskerne koblede en bestemt type biomolekyle, som vides at binde til en biomarkør i brystkræftceller med høj specificitet, til den nye 4WJ-struktur, viste det sig, at 4WJ-strukturen kan vise sig at være effektiv til at lede kræftmedicin til de ønskede celler . Derudover kan de ved at foretage yderligere ændringer af den nye 4WJ-struktur forlænge dens levetid i blodbanen og dermed også virkningen af lægemidlet, der kan kobles til DNA-nanostrukturen.
Forskerne forestiller sig, at deres 4WJ-struktur bygget med kunstige byggeklodser både kan bruges som et værktøj til at transportere lægemidler til den rigtige position i en patients krop. Derudover ser de, at det kan tjene som et værdifuldt værktøj i forskningen. Eksempelvis forestiller forskere sig, at virkningerne af forskellige kombinationer af kræftnedbrydende biomolekyler kan screenes hurtigere og mere effektivt, så den mest effektive kræftbehandling kan findes hurtigere. + Udforsk yderligere
Livets helix:Ny undersøgelse viser, hvordan RNA binder stabilt til kunstige nukleinsyrer
 Varme artikler
Varme artikler
-
 Titanat cigaretfilter kan være mere sikkert(PhysOrg.com) - Mens nuværende cigaretter er lavet med et filter skabt af celluloseacetat, der absorberer ting som nikotin, tjære, og polycykliske aromatiske kulbrinter, Kinesiske forskere har opdaget
Titanat cigaretfilter kan være mere sikkert(PhysOrg.com) - Mens nuværende cigaretter er lavet med et filter skabt af celluloseacetat, der absorberer ting som nikotin, tjære, og polycykliske aromatiske kulbrinter, Kinesiske forskere har opdaget -
 Hvordan man driver elektronik ved hjælp af mekanisk bevægelse(med uret fra nederst til højre):Forskerne Manisha Sahu, Sugato Hajra, Kyungtaek Lee sammen med professor Hoe Joon Kim, der har udviklet en kompositfilm, der kan bruges i energiopsamlingsgeneratorer K
Hvordan man driver elektronik ved hjælp af mekanisk bevægelse(med uret fra nederst til højre):Forskerne Manisha Sahu, Sugato Hajra, Kyungtaek Lee sammen med professor Hoe Joon Kim, der har udviklet en kompositfilm, der kan bruges i energiopsamlingsgeneratorer K -
 En usandsynlig brug for diamanterSmå diamanter giver videnskabsmænd nye muligheder for nøjagtige målinger af processer inde i levende celler med potentiale til at forbedre lægemiddellevering og kræftbehandling. Udgivet i Natur nano
En usandsynlig brug for diamanterSmå diamanter giver videnskabsmænd nye muligheder for nøjagtige målinger af processer inde i levende celler med potentiale til at forbedre lægemiddellevering og kræftbehandling. Udgivet i Natur nano -
 Multifunktionel nanofiber beskytter mod eksplosionerPara-aramid nanofiberplader oven på Twaron®-plader efter fragmentsimuleringsprojektiltestning. Kredit:Grant Gonzalez/Harvard SEAS Siden Første Verdenskrig, langt størstedelen af amerikanske kamp
Multifunktionel nanofiber beskytter mod eksplosionerPara-aramid nanofiberplader oven på Twaron®-plader efter fragmentsimuleringsprojektiltestning. Kredit:Grant Gonzalez/Harvard SEAS Siden Første Verdenskrig, langt størstedelen af amerikanske kamp
- Ikke mere trial-and-error, når du vælger en elektrolyt til metal-luft-batterier
- Krimer over afgiftsfradrag for elbiler, da Biden besøger Detroit-showet
- Kvantificering af gletsjeres økosystemtjenester fremhæver deres betydning for menneskeheden
- Forskere finder mekanismer, hvormed planterødder undgår iltfattig jord
- Syv døde i Spanien, da vinteren stormer langs kysten
- Undersøgelse bekræfter nye strategier for at reducere præstationsgabet


