Katte i et bur:Nye hybride nanocages for hurtigere katalyse
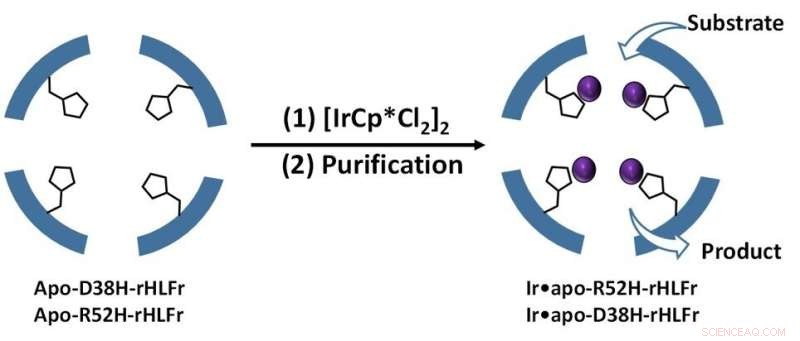
Figur 1. Buret blev konstrueret med aminosyreerstatninger ved at introducere stedspecifikke mutationer, der tillod mere IrCp*-optagelse. Kredit:Takafumi Ueno fra Tokyo Institute of Technology
En ny hybrid ferritin nanocage med histidinrester viser 1,5 gange højere metalionoptagelse og forbedret katalytisk effektivitet til alkoholproduktion, ifølge forskere fra Tokyo Tech i en ny undersøgelse. Deres resultater tyder på, at hybride bio-nanocages effektivt kunne katalysere reaktioner for at give industrielt vigtige produkter.
Biologiske polymerer kan spontant selv samles til komplekse strukturer, der ligner kar eller bure, men er meget mindre og omtales som "nano-bure." Disse strukturer kan rumme en bred vifte af molekyler inde i dem, der opfører sig som "gæster". Et populært eksempel er "ferritin nanocage", som er dannet ved selvsamling af 24 underenheder i proteinet ferritin og kan omslutte metalioner, der er vigtige katalysatorer. Ved hjælp af disse metalioner omdanner en katalytisk reaktion ethvert substrat til et produkt. Selvom det er almindeligt kendt, er ferritinburets potentielle anvendelser i industrien endnu ikke fuldt ud undersøgt.
Hidtil har de fleste bestræbelser på at øge metalionoptagelsen i ferritin resulteret i bure med lav stabilitet. For at få "gæsten" til at sidde godt i buret, er effektivt design nøglen. Med det i tankerne introducerede et team af forskere ledet af prof. Takafumi Ueno, fra Tokyo Institute of Technology, Japan (Tokyo Tech), stedspecifikke mutationer i kernen af ferritin-nanocage og øgede dets optagelse af iridiumkompleks (IrCp*) ). Deres resultater er offentliggjort i Angewandte Chemie . Iridium er en vigtig katalysator i alkoholproduktionsvejen og bruges kommercielt i den farmaceutiske, fødevare- og kemiske industri.
Prof. Ueno forklarer:"Baseret på tidligere litteratur vidste vi, at tilstedeværelsen af koordinationsaminosyrer i buret forbedrer iridiumaktiviteten, og at substituering af disse aminosyrer med passende rester kunne afhjælpe problemet. Da iridiumkomplekset opfører sig som en katalysator, vil koordination rester ville gøre arbejdet." Forfatterne brugte aminosyren histidin til at erstatte to rester, arginin og asparaginsyre i de almindelige (vildtype) ferritinbure og skabe mutanterne R52H og D38H. Bemærkelsesværdigt nok blev samlingsstrukturen eller burstørrelsen ikke påvirket af disse ændringer.
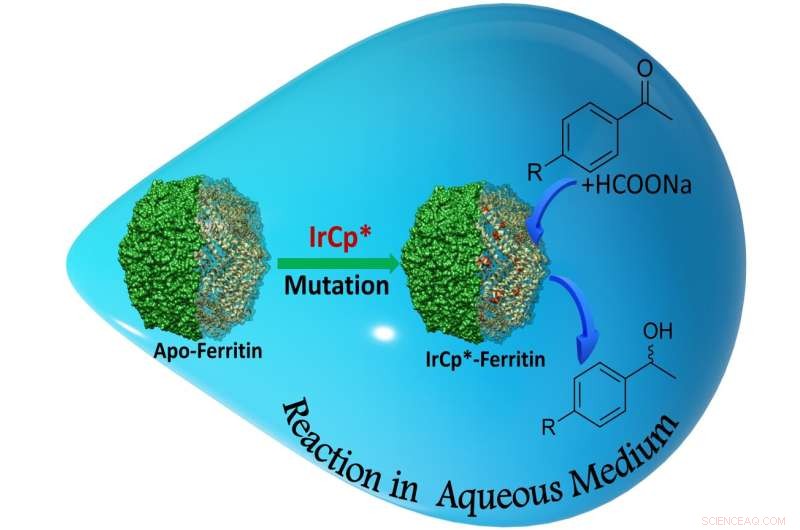
Figur 2. Nanocagen fungerer som en hybrid biokatalysator under omdannelsen af substrater til alkoholer med høj specificitet. Kredit:Takafumi Ueno fra Tokyo Institute of Technology
Dernæst tilføjede de IrCp* til mutanterne og fandt ud af, at R52H var i stand til at indlejre 1,5 gange flere iridiumatomer end vildtypeburet (figur 1). Men det, der slog dem, var D38H-mutanten, som opførte sig nøjagtigt som vildtypen. Så hvorfor havde begge mutationer ikke samme effekt? Ifølge prof. Ueno, "Dette indebærer, at det ikke kun er tilstedeværelsen af histidinresten, men også dens position, der er afgørende for at bestemme optagelseseffektiviteten i buret."
Ved at bruge de nye katalytiske bure var forskerne i stand til at opnå alkoholproduktionshastigheder så høje som 88%. Mutationerne begunstigede åbenbart en strukturel omarrangering af reaktionskomponenterne, hvilket øgede konverteringshastigheden (figur 2).
For at forstå, hvordan substratet opførte sig inde i buret, brugte forskerne simuleringer, hvor substratmolekylerne kunne bevæge sig frit inden for nanocage. De observerede nogle interaktioner mellem substratet og histidin i R52H-mutanten, som ikke var til stede i vildtype-buret, dvs. substratet viste præferencebinding i nanocage.
"Disse hybride bio-nanocages viste sig også at være yderst stabile, hvilket tyder på, at de kunne bruges som levedygtige katalysatorer i industrielle applikationer," konkluderer prof. Ueno. Det nuværende strukturbaserede design af metalionbindingsstedforskningen kunne avanceres til at skabe nye ferritinmutanter med selektiv optagelse af specifikke gæstemolekyler til forskellige katalytiske anvendelser i den kemiske og farmaceutiske industri. + Udforsk yderligere
Proteinbure til design af forskellige katalytiske reaktioner
 Varme artikler
Varme artikler
-
 Neuromorf databehandling med memristorerEn skematisk illustration af det menneskelige neurale hjernesystem og memristorbaserede elektroniske neuromorfe system. Den grundlæggende mekanisme for de typiske memristor-enheder til neuromorfe comp
Neuromorf databehandling med memristorerEn skematisk illustration af det menneskelige neurale hjernesystem og memristorbaserede elektroniske neuromorfe system. Den grundlæggende mekanisme for de typiske memristor-enheder til neuromorfe comp -
 Forskere tid plasmon-genererede elektroner bevæger sig fra nanorods til grafenPlasmonresonansen af guldnanoroder på grafen udvides sammenlignet med guldnanoroder på kvarts, ifølge en ny undersøgelse fra Rice University-forskere. Den ekstra spidsbredde blev tilskrevet spændt e
Forskere tid plasmon-genererede elektroner bevæger sig fra nanorods til grafenPlasmonresonansen af guldnanoroder på grafen udvides sammenlignet med guldnanoroder på kvarts, ifølge en ny undersøgelse fra Rice University-forskere. Den ekstra spidsbredde blev tilskrevet spændt e -
 Ny teknik gør det lettere at ætse halvledereDette er et scanningselektronmikroskopbillede af nanopillarer ætset i galliumarsenid via metalassisteret kemisk ætsning. Kredit:Xiuling Li At skabe halvlederstrukturer til avancerede optoelektroni
Ny teknik gør det lettere at ætse halvledereDette er et scanningselektronmikroskopbillede af nanopillarer ætset i galliumarsenid via metalassisteret kemisk ætsning. Kredit:Xiuling Li At skabe halvlederstrukturer til avancerede optoelektroni -
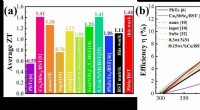 Høj termoelektrisk ydeevne opnået i P-type legeringerGennemsnitlig ZT (a) og konverteringseffektiviteten (b) i temperaturområdet fra 300K til 512K for PbSe/BST-kompositprøven med x=0,2 vol.%. Kredit:Ming Hongwei For nylig, forskere fra Institute of
Høj termoelektrisk ydeevne opnået i P-type legeringerGennemsnitlig ZT (a) og konverteringseffektiviteten (b) i temperaturområdet fra 300K til 512K for PbSe/BST-kompositprøven med x=0,2 vol.%. Kredit:Ming Hongwei For nylig, forskere fra Institute of
- ATLAS-eksperiment undersøger kvark-gluonplasma i en ny undersøgelse af fotoproducerede muonpar
- Udtalelse:Tiltag for fattigdom og trivsel ignorerer stadig miljøet-dette skal ændre sig
- En magnetisk metode til at kontrollere transporten af chirale Majorana fermioner
- Visuel målsøgning for mikroluftfartøjer ved hjælp af scenekendskab
- Hvad går der ind i Norges dommedagshvelv?
- Mulighed jager ned under støvstorm (opdatering)


