Ingeniører dæmper invaderende patogener med en molekylær maske
Vacciner er fortsat den gyldne standard for beskyttelse mod farlige patogener, men det tager lang tid og store ressourcer at udvikle. Hurtigt muterende vira såsom SARS-CoV-2 kan sløve deres effektivitet og endda gøre dem forældede.
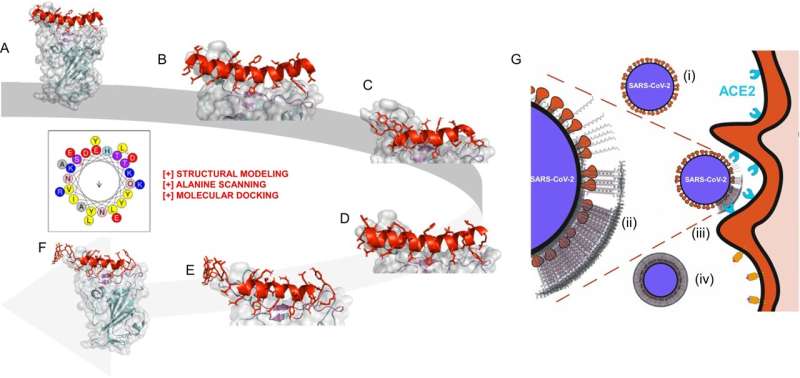
For at løse disse huller er et multi-universitetshold ledet af New Jersey Institute of Technologys Vivek Kumar ved at udvikle en hydrogelterapi, der fungerer som en første forsvarslinje mod vira og andre biologiske trusler. Peptiderne, der udgør denne gel, forhindrer virus som SARS-CoV-2, der forårsager COVID-19, i at binde sig til og trænge ind i celler. De gør dette ved at binde sig til en bestemt receptor på det invaderende patogen, mens de også aggregeres til en flerlags "molekylær maske", der dæmper dens virkning.
I løbet af deres forskning opdagede holdet, at den molekylære maske alene forhindrede infektioner. Den potentielle fordel ved denne nye teknologi, siger de, er dens evne til at bekæmpe forskellige patogener og sygdomsmutationer.
"Beskyttelse af mennesker i de indledende faser af et udbrud er vigtigt," sagde Kumar, en lektor i biomedicinsk teknik. "Vores nye mekanisme kan også hjælpe førstehjælpere i frontlinjen, militært personel, der støder på nye patogener, mennesker i fjerntliggende områder med mangel på ressourcer og dem, der ikke er i stand til at modtage vaccinationer."
Målet på kort sigt er at producere en næsespray mod luftbårne infektioner.
I en undersøgelse i tidsskriftet Nature Communications , beskrev holdet, hvordan masken binder uspecifikt til sit mål. Det er sammensat af beregningsmæssigt designede peptider (strenge af aminosyrer, der danner proteiner), der selv samles til fibrøse hydrogeler i nanoskala. Til sammenligning er antistoffer produceret af vacciner rettet mod bestemte receptorer, da mRNA-vaccinerne udviklede sig under pandemien, og som binder med specifikke proteiner på SARS-CoV-2-spidsen.
Holdets opdagelse opstod fra forskning i begyndelsen af pandemien på nye tilgange til at forhindre virussen i at invadere celler. Det oprindelige design, der involverede peptider, der var målrettet mod SARS-CoV-2-spidsen, så på meget specifikke domæner. Men de ikke-specifikke peptidgeler, de også designede, dannede en flerlagsfiber oven på virussen.
Gruppen har postuleret, at de negative ladninger i fibrene interagerer med forskelligt ladede proteiner på den virale overflade, maskerer dem og dermed forhindrer dem i at interagere med native celler.

Af den ikke-specifikke proteinmaske bemærkede Kumar:"Den danner en større struktur og bedre binding end et enkelt molekyle gør. Selvom den ikke har høj specificitet, kan den samle sig selv og forblive på målet længere og danne en fiber klistermærke på overfladen, der fungerer som molekylær velcro."
Han tilføjede:"Målet ville være et aktuelt middel, der binder til virussen. I tilfælde af SARS-CoV-2 ville vi sprøjte det ind i næsen, som er et stort infektionssted, måske endda profylaktisk."
Holdet testede først fibrene mod en række vira gennem computersimuleringer, der brugte kraftfulde NVIDIA-grafikkort, som almindeligvis bruges i konkurrencespil. De gennemførte senere vellykkede sikkerhedstest med mus og rotter ved hjælp af injektioner og næsespray, sagde Joseph Dodd-o, en Ph.D. studerende i Kumars laboratorium, som udførte meget af forskningen i terapien sammen med Abhishek Roy, også en ph.d. studerende. Behandlingen hæmmede alfa- og omicron-varianterne af SARS-CoV-2 in vitro, og varede i en dag uden at skade dyrene i testene in vivo.
Kumar har udviklet hydrogeler til en række terapeutiske anvendelser. Hans leveringsmekanisme kan tilpasses og består af Lego-lignende peptidstrenge med et bioaktivt middel fastgjort i den ene ende, som kan overleve i kroppen i uger og endda måneder, hvor andre biomaterialer nedbrydes hurtigt. Dens selvsamlende bindinger er designet til at være stærkere end kroppens dispersive kræfter; det danner stabile fibre, uden tegn på at fremkalde betændelse.
Hydrogelen er konstrueret til at udløse forskellige biologiske reaktioner afhængigt af den påsatte nyttelast. Kumars laboratorium har offentliggjort forskning om anvendelser lige fra terapier til at anspore eller forhindre oprettelsen af nye blodkarnetværk, for at reducere inflammation og til at bekæmpe mikrober.
"I dette tilfælde bruger vi elektriske ladninger, der interagerer med patogenet for at forstyrre det," sagde Kumar.
"Vi forsøger stadig at bestemme, hvordan fibrene interagerer:Er dette en mekanisk virkningsmåde? Lægemiddelresistente patogener muterer omkring biokemiske modulatorer, men er de mindre tilbøjelige til at mutere omkring et mekanisk spyd? Ved at forstå denne grundlæggende interaktion ønsker vi at finde ud af, hvordan man bruger det mod forskellige sygdomme."
I nye undersøgelser tester laboratoriet behandlingen mod lægemiddelresistente bakterier og svampe.
Medlemmer af teamet bringer varieret ekspertise:beregningsmæssigt design ved University of Illinois Chicago; bioanalytiske evner ved Georgia Tech og Baylor School of Medicine; virologistudier ved Rutgers University; og platform, analytisk og assay erfaring hos NJIT.
Flere oplysninger: Joseph Dodd-o et al., Antivirale fibriller af selvsamlede peptider med afstembare sammensætninger, Nature Communications (2024). DOI:10.1038/s41467-024-45193-3
Journaloplysninger: Nature Communications
Leveret af New Jersey Institute of Technology
 Varme artikler
Varme artikler
-
 Indfangning af kræft:Flydende biopsi kan forbedre kræftdiagnose og behandlingBlodprøver løber gennem mikrofluidchips. Guldmønstrene er for små til at kunne skelnes med det blotte øje i den arbejdende enhed, resulterer i en metallisk glans. Kredit:Joseph Xu, Michigan Engineerin
Indfangning af kræft:Flydende biopsi kan forbedre kræftdiagnose og behandlingBlodprøver løber gennem mikrofluidchips. Guldmønstrene er for små til at kunne skelnes med det blotte øje i den arbejdende enhed, resulterer i en metallisk glans. Kredit:Joseph Xu, Michigan Engineerin -
 Bobler er de nye linser til lysstråler i nanoskalaDette er laboratoriebilleder af en lysstråle uden en bobleobjektiv, efterfulgt af tre eksempler på forskellige boblelinser, der ændrede lyset. Kredit:Tony Jun Huang, Penn State At bøje lysstråler
Bobler er de nye linser til lysstråler i nanoskalaDette er laboratoriebilleder af en lysstråle uden en bobleobjektiv, efterfulgt af tre eksempler på forskellige boblelinser, der ændrede lyset. Kredit:Tony Jun Huang, Penn State At bøje lysstråler -
 Hvordan grafen og venner kunne udnytte Solens energiKunstnerisk indtryk af grafenmolekyler. Kredit:University of Manchester (Phys.org) — Ved at kombinere vidundermateriale grafen med andre forbløffende et-atom tykke materialer kunne skabe den næste
Hvordan grafen og venner kunne udnytte Solens energiKunstnerisk indtryk af grafenmolekyler. Kredit:University of Manchester (Phys.org) — Ved at kombinere vidundermateriale grafen med andre forbløffende et-atom tykke materialer kunne skabe den næste -
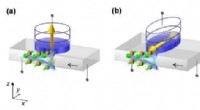 En magnetisk hukommelsesenhed med ny struktur udvikletSkema af strukturer for tre slags spin-orbit-drejningsmoment-induceret magnetiseringsskema. (a) Den første tidligere struktur, hvor magnetiseringen er vinkelret på filmplanet. (b) Den anden foregående
En magnetisk hukommelsesenhed med ny struktur udvikletSkema af strukturer for tre slags spin-orbit-drejningsmoment-induceret magnetiseringsskema. (a) Den første tidligere struktur, hvor magnetiseringen er vinkelret på filmplanet. (b) Den anden foregående
- Forskerteam udvikler metode til fremstilling af store ark metamaterialer
- Lerundergrund på Jordens tørreste sted kan signalere liv på Mars
- Negative virkninger af biomasse
- Hvad er en kalorimeter & Hvad er dens begrænsninger?
- Ny forskning løser robust en af evolutionærbiologiens mest ophedede stridigheder
- 5 ideer til fordobling af verdens fødevareforsyning


