DNA-nanorørringe:Forskerhold udvikler vigtig byggesten til kunstige celler
Under celledeling dannes en ring omkring celleækvator, som trækker sig sammen for at dele cellen i to datterceller. Sammen med forskere fra Heidelberg, Dresden, Tübingen og Harvard er det lykkedes professor Jan Kierfeld og Lukas Weise fra Institut for Fysik ved TU Dortmund Universitet for første gang at syntetisere en sådan kontraktil ring ved hjælp af DNA-nanoteknologi og afdække dens kontraktionsmekanisme. . Resultaterne er blevet offentliggjort i Nature Communications .
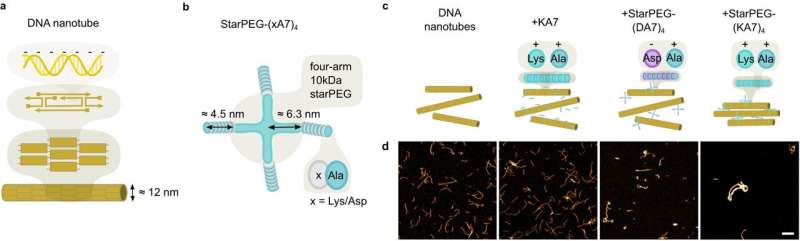
Inden for syntetisk biologi forsøger forskere at genskabe afgørende livsmekanismer in vitro, såsom celledeling. Målet er at kunne syntetisere minimale celler. Forskerholdet ledet af professor Kerstin Göpfrich fra Heidelberg Universitet har nu syntetisk reproduceret kontraktile ringe til celledeling ved hjælp af polymerringe sammensat af DNA-nanorør.
Dannelsen af en ring, der trækker sammen og adskiller delende celler, er et vigtigt skridt i naturlig celledeling. I naturen opnås dette af et maskineri af proteiner:motoriske proteiner drevet af kemisk energi fra ATP-hydrolyse trækker en ring af filamenter af proteinet actin sammen. Adenosintrifosfat, eller ATP, er et molekyle, der forekommer i alle levende celler og leverer energi til adskillige cellulære processer.
Sammentrækningsmekanismen for DNA-ringene udviklet af forskerne er ikke længere afhængig af motorproteiner drevet af ATP-hydrolyse. I stedet kan molekylær tiltrækning mellem ringsegmenter udløse sammentrækningen af polymerringene.
Denne molekylære tiltrækning kan induceres på to måder:enten ved at tværbinde molekyler med to "klæbrige" ender, der kan forbinde to polymersegmenter, eller ved hjælp af udtømningsinteraktionen, hvor polymererne er omgivet af "crowder" molekyler, der presser segmenterne sammen . Denne mekanisme bruger ingen kemisk energi, hvilket betyder, at ingen energikilde skal inkorporeres i den syntetiske celle for at mekanismen kan fungere.
Professor Jan Kierfeld, professor i teoretisk fysik, og doktorgradsforsker Lukas Weise arbejder inden for biologisk fysik. Som en del af deres forskningsarbejde har de udviklet en teoretisk beskrivelse og en molekylær dynamik-simulering af kontraktionsmekanismen, som matcher deres forskningspartneres eksperimentelle resultater.
Til dette formål udtænkte de specielle metoder til at simulere DNA-ringene i en realistisk skala. Teori og simulering gør det muligt at forklare kvantitativt, hvordan polymerringene dannes og trækker sig sammen.
"Det betyder, at vi ikke kun er i stand til at forudsige, at en øget koncentration af 'crowder'-molekyler vil gøre ringen mindre, men også med hvor meget mindre," siger professor Kierfeld. På denne måde er det muligt at bestemme, hvordan diameteren af DNA-ringen kan kontrolleres præcist, hvilket er meget vigtigt for fremtidige anvendelser af kontraktile ringe i syntetisk biologi.
Mekanismer for celledeling er et vigtigt skridt hen imod en kunstig celle, hvis konstruktion letter en bedre forståelse af de funktionelle mekanismer i naturlige celler og dermed af livets grundlag.
Flere oplysninger: Maja Illig et al., Triggered contraction of self-assembled micron-scale DNA nano tube-ringe, Nature Communications (2024). DOI:10.1038/s41467-024-46339-z
Journaloplysninger: Nature Communications
Leveret af TU Dortmund University
 Varme artikler
Varme artikler
-
 En ny mekanisme forbedrer effektiviteten af antibakterielle overfladerVladimir Baulin, forsker fra Institut for Kemiteknik ved Universitat Rovira i Virgili. Kredit:URV Resistens over for antibiotika er blevet et alvorligt folkesundhedsproblem. Hospitalsinfektioner,
En ny mekanisme forbedrer effektiviteten af antibakterielle overfladerVladimir Baulin, forsker fra Institut for Kemiteknik ved Universitat Rovira i Virgili. Kredit:URV Resistens over for antibiotika er blevet et alvorligt folkesundhedsproblem. Hospitalsinfektioner, -
 Grafen kan være nøglen til at kontrollere vandfordampningenDenne visualisering viser lag af grafen, der bruges til membraner. Kredit:University of Manchester Grafenbelægninger kan give mulighed for at kontrollere vandfordampningsprocessen fra forskellige
Grafen kan være nøglen til at kontrollere vandfordampningenDenne visualisering viser lag af grafen, der bruges til membraner. Kredit:University of Manchester Grafenbelægninger kan give mulighed for at kontrollere vandfordampningsprocessen fra forskellige -
 Kvægs blod holder guld nanopartikler stabileTo hætteglas i et Rice University -laboratorium viser guldnanopartikler i saltvand. Til venstre, nanopartiklerne er blevet stabiliseret i bovint serumalbumin og er dispergeret i opløsningen. Til højre
Kvægs blod holder guld nanopartikler stabileTo hætteglas i et Rice University -laboratorium viser guldnanopartikler i saltvand. Til venstre, nanopartiklerne er blevet stabiliseret i bovint serumalbumin og er dispergeret i opløsningen. Til højre -
 En kage på hovedet kaster nyt lys over solcellerKredit:PV-LAB, EPFL/SNSF Gør det bedre med mindre. Det er den udfordring, forskerne fra det schweiziske føderale teknologiske institut i Lausanne (EPFL) har stillet sig selv, støttet af Swiss Nati
En kage på hovedet kaster nyt lys over solcellerKredit:PV-LAB, EPFL/SNSF Gør det bedre med mindre. Det er den udfordring, forskerne fra det schweiziske føderale teknologiske institut i Lausanne (EPFL) har stillet sig selv, støttet af Swiss Nati
- Obligatoriske bygningsenergisyn alene overvinder ikke barrierer for energieffektivitet
- Hvorfor prisen på vand i San Diego er blæst forbi LA'er, ifølge en ny rapport
- Sådan bestemmer du Y-intercepten af en trendlinje
- Teknologi, internationale obligationer, og inspiration:Hvorfor astronomi betyder noget i krisetider
- Hvordan vejer man et enkelt molekyle?
- Hvordan grafen og venner kunne udnytte Solens energi


