Et nanoteknologibaseret CRISPR/Cas9 leveringssystem til genomredigering i kræftbehandling
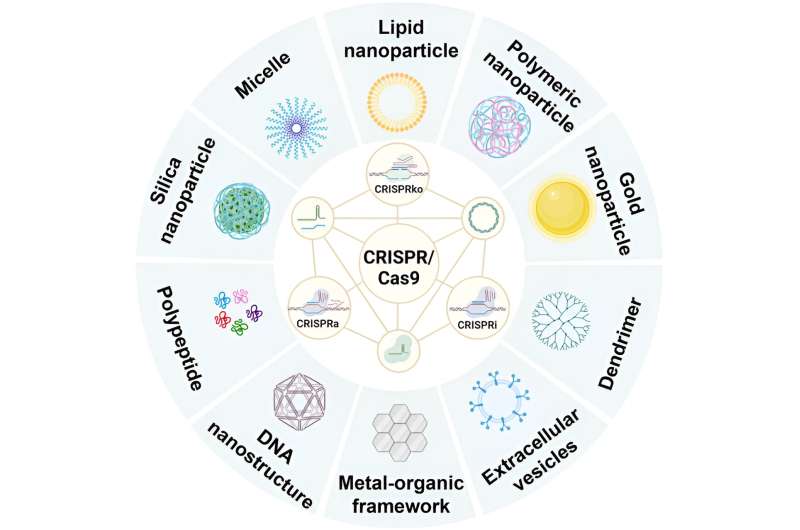
I en undersøgelse offentliggjort i MedComm—Biomaterials and Applications Professor Changyang Gong og hans ph.d. studerende Shiyao Zhou uddyber mekanismen i CRISPR/Cas9-systemet. CRISPR/Cas9-systemet består af Cas9-protein og enkeltstrenget dirigerende RNA (sgRNA).
I nærvær af protospacer-adjacent motiv (PAM) fører sgRNA nøjagtigt Cas9-endonukleasen til målregionerne, hvor det forårsager DNA-dobbeltstrengsbrud (DSB'er), hvilket resulterer i stedspecifik genomisk ændring. Endogen DNA-reparation kan finde sted efter oprettelsen af en DSB via to primære genomredigeringsveje:nonhomolog endesammenføjning (NHEJ) eller homologi-dirigeret reparation (HDR).
Ved at bruge de biologiske egenskaber ved Cas9, der målretter specifikke DNA-sekvenser under vejledning af sgRNA, har forskerne videreudviklet genmålretningsaktivering og genmålretningsinhiberingsværktøjer baseret på dCas9, kaldet henholdsvis CRISPRa og CRISPRi.
I papiret er karakteristika for tre former for CRISPR/Cas9-last skitseret. Tre leveringsformer af CRISPR/Cas9-systemet er plasmider, mRNA/sgRNA og ribonukleoprotein (RNP) komplekser, som hver har sine egne fordele og ulemper.
Ikke desto mindre, uanset nyttelastformen, er det udfordrende for CRISPR/Cas9 at trænge ind i målceller. Derfor er det vigtigt at udvikle en effektiv nanoteknologistrategi for CRISPR/Cas9-levering.
Nanoteknologi-baserede leveringsteknikker for disse tre kategorier til behandling af kræft er opsummeret i papiret. Selvom virale vektorer er de mest almindeligt anvendte leveringsvektorer til CRISPR/Cas9-systemet, har deres anvendelser været begrænset på grund af ulemper såsom begrænset pakkekapacitet, høj immunogenicitet og mangel på vævsmålretning.
Nanobærere, afsluttende kationiske lipid-baserede nanopartikler, kationiske polymer/polypeptid-baserede nanopartikler, uorganiske nanomaterialer, DNA-nanostrukturer, guldbaserede nanopartikler og exosomer eller ekstracellulære vesikler, er i øjeblikket håbefulde leveringsmetoder til CRISPR/Cas9-systemer.
Tager man kationiske lipid-baserede ikke-virale vektorer som et eksempel, kan kationiske lipidvektorer indlæse CRISPR/Cas9-systemet via elektrostatiske interaktioner. Derudover kan målretningen af vektorer forbedres ved ligandmodifikation eller strukturel modifikation for at fremme cellulær optagelse og forbedre leveringseffektiviteten.
Udløst af specifikke intracellulære miljøer eller ekstracellulære signaler, kan responsive nanocarriers også opnå specifik frigivelse af CRISPR/Cas9 til spatiotemporalt kontrollerbar genredigering. Disse nanoteknologibaserede smarte leveringssystemer forbedrer markant de tumorterapeutiske evner i CRISPR/Cas9-systemet og reducerer bemærkelsesværdigt dets off-target-effekter.
Forskerne giver ny indsigt i fremtidige forskningsretninger i den nanoteknologibaserede CRISPR/Cas9-systemlevering. Genredigering ved hjælp af CRISPR/Cas9 nanoteknologi er en ny daggry inden for kræftbehandling. Den kontinuerlige optimering og forbedring af CRISPR/Cas9 levering ikke-virale vektorer viser dets store potentiale for forskning og anvendelse inden for onkologisk terapi.
Ikke desto mindre er størstedelen af forskningen stadig i sin tidlige fase. CRISPR/Cas9 har mange uløste problemer på molekylært niveau. Som konklusion kan personlig målrettet terapi baseret på CRISPR/Cas9 være fremtiden for tumorterapi og bringe nyt håb for tumorbehandling.
Flere oplysninger: Shiyao Zhou et al, Nanoteknologi-baseret CRISPR/Cas9 leveringssystem til genomredigering i cancerbehandling, MedComm—Biomaterials and Applications (2024). DOI:10.1002/mba2.70
Leveret af Sichuan International Medical Exchange and Promotion Association
 Varme artikler
Varme artikler
-
 En ny strategi til syntese af krystallinske grafitiske nanobåndKredit:Center for High Pressure Science &Technology Advanced Research Nyt arbejde fra et team af forskere ledet af Dr. Kuo Li og Haiyan Zheng fra Center for High Pressure Science and Technology Ad
En ny strategi til syntese af krystallinske grafitiske nanobåndKredit:Center for High Pressure Science &Technology Advanced Research Nyt arbejde fra et team af forskere ledet af Dr. Kuo Li og Haiyan Zheng fra Center for High Pressure Science and Technology Ad -
 Nanopatch polio vaccine levererNanopatch -opfinder professor Mark Kendall. Kredit:University of Queensland Bestræbelserne på at befri verden for polio har taget et andet vigtigt skridt, takket være forskning ledet af bioscience
Nanopatch polio vaccine levererNanopatch -opfinder professor Mark Kendall. Kredit:University of Queensland Bestræbelserne på at befri verden for polio har taget et andet vigtigt skridt, takket være forskning ledet af bioscience -
 Kevlarbaseret kunstig brusk efterligner den magiske virkelighedDet kunstige brusk er meget fleksibelt, men alligevel modstandsdygtigt over for rivning. Kredit:Joseph Xu, Michigan Engineering Communications &Marketing Bruskens enestående væskestyrke, hvilket e
Kevlarbaseret kunstig brusk efterligner den magiske virkelighedDet kunstige brusk er meget fleksibelt, men alligevel modstandsdygtigt over for rivning. Kredit:Joseph Xu, Michigan Engineering Communications &Marketing Bruskens enestående væskestyrke, hvilket e -
 Følsom nanooscillator kan detektere patogenerEn illustration af den nanoelektromekaniske oscillator, med udhænget yderst til højre. Indsatsen er en skrå 3-D profil af strukturen, som viser siliciumdioxidposterne. Billede:Rob Ilic (PhysOrg.co
Følsom nanooscillator kan detektere patogenerEn illustration af den nanoelektromekaniske oscillator, med udhænget yderst til højre. Indsatsen er en skrå 3-D profil af strukturen, som viser siliciumdioxidposterne. Billede:Rob Ilic (PhysOrg.co
- NASA-missioner undersøger, hvad der kan være et 1-i-10.000-årigt gammastråleudbrud
- Hitchhiking nanorør viser hvordan celler omrører sig selv
- Hvad forårsager omvendt polaritet i AC?
- Undersøgelse finder forhindringer for kvinder og minoriteter i kemi
- Hvordan man bygger kunstige nanofabrikker til at drive vores fremtid
- Sådan administrerer du dit digitale efterliv, og hvorfor det betyder noget


