Forskere udvikler selvsamlende, selvoplysende terapeutiske proteiner
Når det kommer til at levere medicin til kroppen, er en stor udfordring at sikre, at de forbliver i det område, de behandler, og fortsætter med at levere deres nyttelast nøjagtigt. Selvom der er gjort store fremskridt med at levere lægemidler, er overvågning af dem en udfordring, der ofte kræver invasive procedurer som biopsier.
Forskere ved NYU Tandon ledet af Jin Kim Montclare, professor i kemisk og biomolekylær teknik, har udviklet proteiner, der kan samle sig selv til fibre, der skal bruges som terapeutiske midler til potentielle behandlinger af flere sygdomme.
Disse biomaterialer kan indkapsle og levere terapeutiske midler til en lang række sygdomme. Men mens Montclares laboratorium længe har arbejdet på at producere disse materialer, var der engang en udfordring, der var svær at overvinde – hvordan man sikrede sig, at disse proteiner fortsatte med at levere deres terapeutika på det korrekte sted i kroppen i den nødvendige mængde tid.
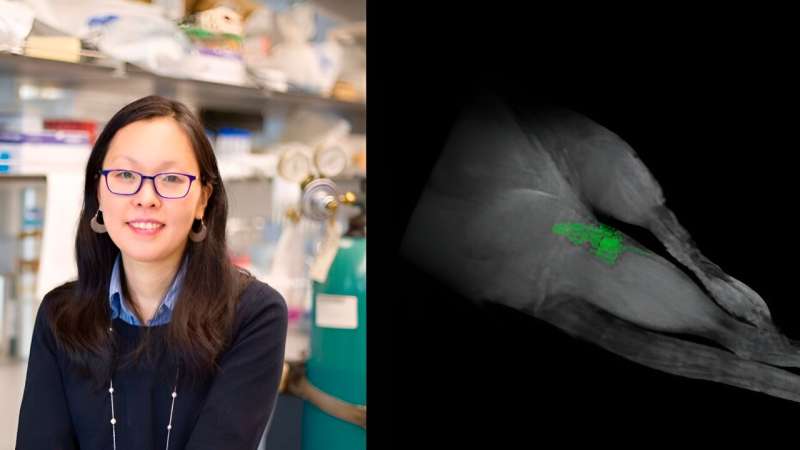
I en nylig undersøgelse offentliggjort af tidsskriftet ACS Applied Nano Materials , var hendes laboratorium i stand til at skabe biomaterialer, der var fluorerede. Takket være denne fluorering kan de overvåges ved simple FMRI-scanninger, hvilket gør det muligt for læger at sikre, at lægemidlerne forbliver på behandlingsområderne gennem ikke-invasiv billedteknologi.
Materialet består af naturlige proteiner, men forskerholdet introducerede den ikke-naturlige aminosyre, trifluoroleucin. Fordi fluor er sjælden i kroppen, giver det biomaterialerne mulighed for at lyse op som en ferievisning, når kroppen sættes i en 19FMRI-scanning.
"Som et terapeutisk middel kan det ikke kun levere et terapeutisk middel til for eksempel kræft eller ledsygdomme, men vi kan nu se, at det stadig er på plads i kroppen og frigiver medicinen, hvor det er meningen," siger Montclare. "Det fjerner behovet for invasive operationer eller biopsier for at se, hvad der foregår."
Montclares laboratorium udfører banebrydende forskning i ingeniørproteiner for at efterligne naturen og i nogle tilfælde fungere bedre end naturen. Hun arbejder på at tilpasse kunstige proteiner med det formål at målrette mod menneskelige lidelser, lægemiddellevering og vævsregenerering samt skabe nanomaterialer til elektronik. Gennem brug af kemi og genteknologi har hun ydet bidrag til sygdomme lige fra COVID-19 til slidgigt til mange flere.
Dette gennembrud bruger de samme aminosyrer og proteiner, som kendetegner meget af Montclares forskning. Fordi de er lavet af organiske materialer, når disse biomaterialer har fuldført deres job og leveret terapeutiske midler, kan kroppen nedbryde dem uden nogen form for negative virkninger.
Dette adskiller det fra andre behandlinger, der bruger ikke-organiske materialer, der kan forårsage et alvorligt immunrespons eller andre reaktioner. I kombination med fluoreringsteknikken kunne disse materialer give en behandling for lokaliserede sygdomme, der kan være langt mindre invasive end nuværende behandlinger og er langt lettere og mindre forstyrrende at overvåge.
Montclare arbejdede tæt sammen med fakultetet ved NYU School of Medicine om denne undersøgelse, herunder den medkorresponderende forfatter Youssef Z. Wadghiri i afdelingen for radiologi samt Richard Bonneau ved Flatiron Institute.
Montclares team viste deres forskning i musemodeller, men hun søger allerede at eksperimentere på mus med specifikke lidelser for at bevise proteinets evner til at behandle sygdomme.
De selvsamlende proteiner, som Montclares team brugte, er kun en delmængde af det, hun og hendes laboratorium arbejder på. I et andet papir offentliggjort i Biomacromolecules , var hendes laboratorium i stand til at bruge computerdesign til at skabe proteiner, der kunne danne hydrogeler, takket være et program skrevet af hendes ph.d. studerende Dustin Britton.
Disse hydrogeler har forskellige overgangstemperaturer - den temperatur, hvor gelerne kan forblive gelerede uden at opløses eller blive ustabile. Tidligere var den øvre grænse for gelering omkring 17° Celsius. Til biomedicinske anvendelser var dette suboptimalt, da det ville smelte, når det nærmede sig menneskelig kropstemperatur. Ved at bruge sine beregningsdesignede proteiner var Britton i stand til at flytte denne grænse op til 33,6° Celsius.
På grund af denne nye stabilitet kunne proteinerne, som Britton og Montclare designede, bruges til topiske behandlinger, herunder helende sår. Og ud over den øgede varmetolerance kan det nye protein gelere meget hurtigere end tidligere versioner, hvilket gør det langt mere effektivt og mere anvendeligt til medicinske anvendelser.
Mens temperaturen skiftede, var Britton også i stand til at designe et protein, der også er fluorescerende, hvilket betyder, at det har samme potentiale for visualisering som de fluorerede proteiner i deres anden undersøgelse. Det giver lægerne mulighed for at overvåge dens tilstedeværelse i sår og sikre, at den leverer sin terapeutiske nyttelast. Og gelen har de samme fordele som laboratoriets proteiner beregnet til internt brug, idet den vil være i stand til at nedbrydes og forsvinde i kroppen med få eller ingen skadelige virkninger.
Brittons computermodel gør mere end at designe dette specifikke protein. Ifølge Monclare har området for proteinfremstillede biomaterialer længe været domineret af trial-and-error-testning af hypotetiske designs i håb om at se, om de vil være stabile. Men Brittons model var i stand til at skabe konsekvent succesfulde geler, generere sekvenser med en ekstrem høj succesrate og skabe nye proteiner med nye egenskaber til potentielle terapeutiske anvendelser.
"For fremstilling af biomaterialer vil dette absolut accelerere, hvad vi er i stand til at lave," siger Montclare. "Som det traditionelt er gjort, laver man rationelle ændringer og ser, om det virker, og 90 procent af tiden gør det ikke. Med denne nye model fungerer de alle sammen, og vi kan så vælge blandt de bedste af dem. Det vil revolutionere den måde, vi laver biomaterialer på."
I Monclares laboratorium har dette ændret måden, de vil skabe nye proteiner og materialer på fremadrettet - der er ingen vej tilbage til den rationelle iterationspraksis, der havde så høj en fejlrate. Og det vil helt sikkert fremskynde produktionen af revolutionære biomaterialer, der snart vil helbrede nogle af de mest alvorlige medicinske tilstande i hele verden.
Flere oplysninger: Dustin Britton et al., Protein-Engineered Fibres For Drug Encapsulation Sporbare via 19F magnetisk resonans, ACS Applied Nano Materials (2023). DOI:10.1021/acsanm.3c04357
Dustin Britton et al., Computational Prediction of Coiled-Coil Protein Gelation Dynamics and Structure, Biomakromolekyler (2023). DOI:10.1021/acs.biomac.3c00968
Journaloplysninger: Biomakromolekyler
Leveret af NYU Tandon School of Engineering
 Varme artikler
Varme artikler
-
 Spejlbilleder af korannulenmolekyler kan føre til spændende nye muligheder inden for nanoteknologiFigur 1:Inversionen mellem asymmetriske ikke-superponerbare spejlbilleder af corannulener. De gule kugler repræsenterer forskellige kemiske grupper med uret eller mod uret set fra den konvekse side af
Spejlbilleder af korannulenmolekyler kan føre til spændende nye muligheder inden for nanoteknologiFigur 1:Inversionen mellem asymmetriske ikke-superponerbare spejlbilleder af corannulener. De gule kugler repræsenterer forskellige kemiske grupper med uret eller mod uret set fra den konvekse side af -
 Epitaksialt dyrket molybdænoxid udvikler sig som et bulk-lignende 2-D dielektrisk lagKredit:Seoul National University 3 eV har været påkrævet for UV-relaterede optoelektroniske enheder, kraftelektronik, og dielektriske lag. En af de lovende kandidater er overgangsmetaloxider (TMO
Epitaksialt dyrket molybdænoxid udvikler sig som et bulk-lignende 2-D dielektrisk lagKredit:Seoul National University 3 eV har været påkrævet for UV-relaterede optoelektroniske enheder, kraftelektronik, og dielektriske lag. En af de lovende kandidater er overgangsmetaloxider (TMO -
 Ny måde at lave 3-D kulstofkomponenter påKun (Kelvin) Fu, en adjunkt i maskinteknik ved University of Delaware, har brugt en 3D -printer til at lave ren carbon nanorør (CNT) arkitektur, der er lette, stærk, og meget porøs. Kredit:University
Ny måde at lave 3-D kulstofkomponenter påKun (Kelvin) Fu, en adjunkt i maskinteknik ved University of Delaware, har brugt en 3D -printer til at lave ren carbon nanorør (CNT) arkitektur, der er lette, stærk, og meget porøs. Kredit:University -
 Nanomateriale til at drive ny generation af solcellerDr. Kruk ved siden af et diagram over metamaterialestrukturen. Kredit:Stuart Hay, ANU Fysikere har opdaget radikale nye egenskaber i et nanomateriale, som åbner nye muligheder for meget effektiv
Nanomateriale til at drive ny generation af solcellerDr. Kruk ved siden af et diagram over metamaterialestrukturen. Kredit:Stuart Hay, ANU Fysikere har opdaget radikale nye egenskaber i et nanomateriale, som åbner nye muligheder for meget effektiv
- 70, 000 i det sydlige Californien for at evakuere, efter at branden vokser
- Usikre fleksibelt arbejde påvirker over fire millioner mennesker i Storbritannien - langt mere end …
- Ny indsigt i jordskorpen, kappe og ydre kerne interaktioner
- Sådan beregnes pH for en to-kemisk blanding
- Menneskets kulturelle evolution viste sig at være lige så langsom som den biologiske evolution
- Snakebites:Vi troede, at vi havde skabt et nyt vinder mod gift, men så floppede det. Hvorfor det vi…


